- 現在位置
- トップ > 政策・審議会 > 審議会情報 > 科学技術・学術審議会 > 資源調査分科会 > 資源調査分科会(第19回) 配付資料 > 参考資料5 平成20年度新たな健康の維持増進に関わる食品成分等に対するニーズ調査 > 5.成果 第1章 機能性成分等新たな健康の維持増進に関わる成分の分析に対するニーズ調査
5.成果 第1章 機能性成分等新たな健康の維持増進に関わる成分の分析に対するニーズ調査
1 機能性とは
1)機能性成分の概念
1.食の研究のはじまり
東洋では、栄養バランスのとれた食事は病気を予防するという考え方が古くからあり、古代中国においては、王の食事の管理を任されていた食医は、医者のなかでも最高位に位置していたという。20世紀に入ると、食は科学的な研究の対象となり、大学においては、食に関する研究は農学部で、薬に関する研究は医学部で行われた。日本では当時の内務省も「食薬区分」の政策をとることとなった。このような状況のなかで、種々の疾患が食事由来の物質の欠乏に起因することが明らかとなり、食の重要性が脚光を浴びる時代へと移行した。なかでも、1912年、脚気を予防する成分が米ぬかに含まれていることを突きとめた東京帝国大学農学部の鈴木梅太郎博士の研究は、日本が誇れる成果であるといえる。その後、この物質は生命の維持に不可欠な栄養素であることがわかり、ビタミンB1と命名された。その後、農学系の研究者は、後述する栄養学の発展に大きく貢献することになる。
2.栄養学の創始と発展
この頃、京都帝国大学医科学講座を卒業して、米国のエール大学留学から帰国したばかりの佐伯矩博士が、栄養を学問として位置づけ、医学の一分野として独立の学問にしたいとし、1914年、私立栄養研究所(後の国立栄養研究所)を北里研究所の敷地内に創設した。佐伯博士は栄養に関する研究を、生理学的、生化学的、食品科学的研究を体系化して統一し、栄養科学として位置づけた。1934年、日本医学会から「栄養学会」が分科会として独立することが認められ、世界に先駆けて栄養学が独立した学問として認められるに至った。その後、第二次世界大戦前後の日本では、食糧不足が深刻となったが、佐伯博士は栄養三色運動[赤(血や肉になる赤色の食品)・緑(体の調子を整える緑の食品)・黄(働く力になる黄色の食品)の三色をバランスよく食べることで、心の安定と健康な体を作ろうという運動]を展開するなど、国民に対する栄養教育も率先して実施した。一方、京都大学農学部の満田久輝博士によりビタミン強化米等が開発され、栄養学は実践にも大いに活用された。
この後、佐伯博士は国際連盟に世界中の食品の分析やビタミンの国際単位を定めること等を提案し、食品の分析を「人類の栄養問題を完全に解決する一つの因子」として位置づけ、1931年、「日本食品成分総覧」を発表した。これが日本食品標準成分表の始まりである。
3.食品の機能性の研究と機能性の概念
1960年代、日本は高度経済成長期となり、食物や食品は、生命の維持のためだけでなく、味や香りを楽しむとともに、美味しさが追求されるようになった。その結果、食の嗜好性が重要視されることとなり、様々な食品が市場に出回った。これにより、食品学、食品科学、食品工学が発展し、インスタント食品等も開発された。その後、日本は飽食の時代を迎え、食事の摂り過ぎと運動不足による生活習慣病の発症が問題となる時代へと移行する。このような状況の中、高齢化社会の到来と食品研究の進歩により、1980年代には、肥満、糖尿病、高血圧、高脂血症といった生活習慣病を予防する食品成分が注目されることとなった。そこで東京大学農学部の荒井綜一博士らは、疾病のリスクを軽減する食品を機能性食品と名付け、1984年、文部省重点領域「機能性食品」研究班を立ち上げた。この研究班では、食品の機能を次の3つに位置づけた。すなわち、栄養面でのはたらきを1次機能、嗜好面でのはたらきを2次機能、そして生活習慣病等の疾病の予防面でのはたらきを3次機能とし、この概念を「食品機能論」とした。この新しい概念を取り入れた「食品機能学」は、現在では多くの大学においてその講座が設けられている。この3つの食品機能の概念は、まさに食品と人との関わりの歴史と一致するものであるといえよう。
荒井博士らは、機能性食品の定義を「生活習慣病の一次予防のはたらきをもつ新食品」としている。この定義には1次機能と2次機能は含まれないのが原則である。すなわち、機能性食品は、食品の3次機能に着目した食品であるといえる。さらに、機能性成分は栄養素や嗜好成分ではなく、これまで栄養学のなかでは軽視されがちであった非栄養素成分であることが特徴であるとした。そして対象となる生体の機能は、免疫系、分泌系、神経系、循環系、消化系としている。
4.保健機能食品の創設
1980年代、市場には機能性を期待させる食品が出回り、なかには食品による健康被害も報告されるに至った。このような状況のなか、1991年、当時の厚生省は、国民が安心して食生活の状況に応じた選択ができるよう、機能性を表示する食品の類型化として、特定保健用食品を創設した。特定保健用食品とは、「身体の生理学的機能等に影響を与える保健機能成分を含んだ食品であって、健康の維持増進及び特定の保健の用途に資するもの」と定義された。この時、特定保健用食品は、食品の機能性のみに着目するのではなく、栄養機能や味覚機能も合わせもつ特別用途食品の一つとして位置づけられた。特定保健用食品は、食品の保健の用途に関して個別に評価され、ヒトにおける有効性と安全性が確認されていること、適切な摂取量が医学的、栄養学的に設定されていること、保健機能成分(関与成分)が定量的に把握できること等が許可条件である。さらに、2001年には、ミネラル類及びビタミン類という1次機能に着目した規格基準型の栄養機能食品を創設し、特定保健用食品と併せて保健機能食品制度を創設した。この改正により、食品の形態も錠剤型やカプセル型も許可されることになった。さらに、2005年には、条件付特定保健食品(科学的根拠が確立されていないが、一定の有効性が確認されている食品)の導入などの制度改正も行われている。これらの制度の詳細については参考として後述する。
5.本報告書で取扱う機能性成分と食品の選定について
以上、機能性の概念について、主に歴史的経緯から解説してきたが、本報告書で取扱う機能性成分と食品の範囲については、機能性成分の荒井博士らの定義による食品の3次機能に基づき、さらに、ヒトにおける有効性に関して科学的根拠は十分ではないが、機能性を示す可能性のある素材のうち、人びとの関心・知名度が高く、分析が可能で生産量が多い素材を含めて、これらを取り扱うこととした。なお、1次機能及び2次機能に関する成分は除外している。本調査で分析対象とした10種類(イソフラボン、カテキン、フェルラ酸、クロロゲン酸、フラボノール、フラボン、フラバノン、クルクミン、カロテノイド、γ‐アミノ酪酸)のうち、特定保健用食品の関与成分として認められているものは、イソフラボン、カテキンの2種類のみであり、それ以外のフラボン、カロテノイドなど8種類については行政上の位置づけがなされていない。一方、対象とする食品は、主にその素材が多く含まれる食品である。
また、本調査では、一般に流通している食品の成分表あるいは食品成分のデータベースの必要性という視点から、ある特定の成分(合成された成分も含む)を高濃度に含有する(意図的に含有させた)食品を意識した特定保健用食品などとは異なり、常在成分が通常の量含有されている食品の持つ機能性を対象とする。したがって、本調査で対象とする機能性食品の多くは生活習慣病や特定の疾病に対する予防や改善効果を有する化学物質と考えられる。
2)機能性成分の役割
食品成分の持つ機能性に関して、特定保健用食品では整腸作用、血糖値の上昇抑制など種々の機能(参考資料参照)が挙げられている。これらの食品とその機能性の関係は培養細胞を用いた試験、動物実験、ヒト臨床試験などにより確認され、そのメカニズムについての研究も数多くあって解明が進んでいる。また、特定保健用食品に限らず食品に含まれる成分の機能性に関しても非常に多くの報告がある。これらの報告の大部分が成分を多量に投与または摂取させることにより、得られた結果である。このような観点から眺めた各成分の機能性については、個々の成分の解説の中でその機能性に関して触れているので(「3 個別具体的な機能性成分に関する動向、1)代表的な機能性成分」)、これらを参考としていただきたい。
近年、生活習慣病の原因(リスク)となる栄養素の種類と摂取量に関する研究が盛んに行なわれている。そして、ここが強調されるべき点であるが、いわゆる機能性成分は、ヒトの生存や成長に決定的な役割を演じているわけではないが、生活習慣病のリスク(予防要因として働く場合の負のリスクもここに含める)となる可能性が基礎研究によって成立している。このような背景に基づいて、ヒト集団において、機能性成分の摂取量を推定し、生活習慣病の発生率や、生活習慣病に関連する健康指標(血清脂質濃度や血圧など)との関連を検討する、いわゆる栄養疫学的な研究が世界各地で精力的に進められている。この種の研究の基礎となるのが、ヒト集団において機能性成分の摂取量を推定する作業であり、そのために求められるのが食事アセスメント法の技術と、機能性成分に関する食品のデータベースの充実の程度である。
次章(2.日本食品標準成分表及びその他のデータベースへの活用、2)データベースの活用方法)で循環器疾患(心筋梗塞・脳卒中)とポリフェノール類及びイソフラボン類の摂取量の関係について解析された例を示すが、一部にその機能性が明らかとなった成分と疾病の組み合わせもあるものの明確な結論を導くことはかなり難しいことがわかる。食品に含まれる成分と生活習慣病との関係、すなわち生体内において機能性成分が演じている役割についての研究はその緒についたばかりである。その主な原因は、解析の基本となる食品に含まれる成分量のデータが少ないために、正確な摂取量を把握できないことにあると言っても良い。
2 日本食品標準成分表及びその他のデータベースへの活用
1)日本食品標準成分表への収載の可能性
1.日本食品標準成分表の用途
現在の五訂増補日本食品標準成分表には、18食品群について、標準的な成分値が掲載されている。現在収載されている食品成分としては、日本人の食事摂取基準で推奨量または目安量が策定されている栄養素が中心である(ビオチン、ヨウ素、クロム、セレン、モリブデンは収載予定)。日本食品標準成分表の用途は、学校給食を始めとする様々な集団給食の給食管理に用いられる他、厚生労働省が5年毎に策定している日本人の食事摂取基準並びに毎年実施している国民健康・栄養調査の基礎資料として、また、農林水産省の食料需給表の作成、食料需給率の目標設定のための基礎資料等にも活用されている。さらに、教育、研究面では、高等学校や大学における栄養教育や栄養学、食品学、医学、農学の分野の研究等においても広く活用されている。
2.機能性成分の日本食品標準成分表への収載に対するニーズ(アンケート結果)
今回、本事業では、機能性成分の日本食品標準成分表への収載に対するニーズを調査するため、日本栄養士会に依頼し、栄養士を対象としてアンケート調査を実施した(参考資料)。その結果、日本食品標準成分表に機能性成分の収載を希望する者は、希望しない者を上回る結果となった。収載を希望する理由としては、機能性食品が数多く市場に出回っていることから、質問や問い合わせへの対応として活用したいこと、あるいは教育や情報提供のソースとして有用であるためとの回答が多かった(表1‐1)。しかし、機能性成分に関する情報を病気の予防や栄養指導に役立てたいとの回答もあり、現時点では必ずしも利用目的が適切であるとは言い難い回答もあった。また、機能性成分イコール特定保健用食品の関与成分と考えている回答もあった。一方、反対の理由としては、摂取の基準が策定されていない機能性成分を収載しても数値を活用できないこと、また、収載成分が増えることにより、使い勝手や利便性が悪くなるためという回答が多くを占めた。ただ、これらの回答者の中には参考資料として別表に収載することを希望する者も多かった。なお、今回の調査で収載希望が最も多かった食品成分は、ポリフェノールで、次いでイソフラボン、カテキンであった。
表1‐1.アンケート結果
(質問;日本食品標準成分表に機能性成分の含有量を収載することを希望しますか)
| 結果 | 主な理由 |
|---|---|
| 希望する (111名) |
・機能性成分への関心が高まり、問い合わせが多いため。 ・情報が氾濫しており、過剰摂取を避けるためにも正しい情報が必要。 ・健康維持や病気予防に役立つ機能性成分が明らかになってきており、栄養指導等に活かせる。 ・機能性成分の機能を知りたい。 ・機能性成分や特定保健用食品、特別用途食品の収載はあったほうが便利。 |
| 希望しない (66名) |
・科学的根拠が十分でなく、摂取基準量が不明である。 ・日本食品標準成分表が複雑になり、その活用に不便をきたす可能性がある。 ・特に必要性を感じない。現状で対応できる。 ・食品の機能性に注目が集まり、食事のバランスに影響を及ぼす可能性がある。 ・食品の機能性に対する誤解を生むことが危惧される。 |
その他、記載なし3名、判別不能3名、どちらとも言えない1名。
3.機能性成分の日本食品標準成分表への収載の可能性
a)本調査における機能性成分分析の意義
食品の機能性成分と疾病との関係に関する調査研究や分析法の進歩、並びに社会的ニーズの高まりから、機能性成分のデータベースの需要が増えていることは前述した。ところが、これまでのデータベースは特定の食品に限られた食品毎のものが多いことに加え、統一された分析法による食品間の比較が可能なものは少ない。そこで、今回、将来のデータベース構築のための予備段階として、後述する機能性成分について、統一された分析法により、食品中の成分分析を実施することとした。さらに、分析方法に関する問題点を挙げ、分析精度に影響する因子の検討を行うとともに、方法論の妥当性に関する検証もあわせて行うこととした。
b)本調査における分析結果の活用
本調査は、将来のデータベース構築のための予備的調査であり、食品の選定のための調査及び分析法の妥当性の検討も兼ねている。ただし、本事業で採用した食品は、品種、収穫時期、サンプリング方法を考慮していないため、その食品の代表値として取扱うことは出来ない。
c)機能性成分の日本食品標準成分表への収載の妥当性
機能性成分の日本食品標準成分表への収載の可能性に関して、前述した日本食品標準成分表の用途のうち、集団給食の管理においては、摂取目安量等が明確ではない機能性成分の日本食品標準成分表への収載は、現時点では適切でないと考えられる。この点については、今回実施した栄養士を対象としたアンケートにおいても同様の指摘がなされている。ただし、参考値として別表に掲載することは差し支えないと考えられる。
一方、厚生労働省で実施している日本人の食事摂取基準は、国民の健康の維持・増進、生活習慣病の予防を目的としてエネルギー及び栄養素の摂取量の基準を示すものであるため、現時点で基準を設定するための十分な科学的根拠が確立していない機能性成分の分析値に対する期待は低いものと考えられる。国民健康・栄養調査においては、国民の身体の状況並びに栄養素等摂取量の状況を明らかにし、国民の健康の増進の総合的な推進を図るための基礎資料を得ることを目的としていることから、機能性成分に関する情報は場合によっては健康影響も含めて有用なものになると考えられる。農林水産省が発表している食料需給表は、わが国で供給される食料の生産から最終消費に至るまでの、総量を明らかにしたものであり、食料自給率の算出の基礎となるものである。これに関しては、食品成分の摂取量の調査研究において有用である可能性がある。
他方、教育及び研究面からは、食品の機能性成分に関する情報は、有効性に関する科学的根拠の蓄積と健康影響の評価において大変重要であると考えられる。特に、機能性成分の摂取状況と生活習慣病との関連を明らかにする疫学的な調査研究や健康影響との関連を評価する際にも大いに寄与するものと考えられる。
以上のこと及び一部ではあるが、栄養士を対象としたアンケートの結果を総合的に勘案すると、知名度の高い広義の機能性成分のうち、分析が可能な成分について、将来的には日本食品標準成分表の別表として収載することが期待されているといえる。大豆イソフラボンについては、特定保健用食品の関与成分であることからヒトでの有効性と安全性が確認されていること、食品安全委員会で摂取目安量と上限量に関する報告がなされていること、アンケート調査において収載希望が多数であったことから、本表へ収載する条件は整っていると考えられる。ただし、大豆イソフラボンには15種類の成分が存在することや成分によって生物活性が異なる可能性があること、人における生体利用性の違い等について十分に議論する必要がある。
2)その他のデータベースの必要性
1.必要性に関する基本的な考え方
基本的には、食品成分データベースは、食品中に含まれる成分と健康との関連について、人を用いて検討する際の重要な基礎資料であると考えられる。
しかしながら、必ずしもそうでない場合もありうる。例えば、通常の食品に含まれないほどに多量を摂取させて、その健康影響を検討するような研究手法も存在する。具体的には、ある機能性成分を高用量含むサプリメントを開発し、その健康効果を検討するような場合である。このような場合にはデータベースは必要ではない。
一方、人が通常の食品から日常的に摂取している機能性成分の量と健康との関連を明らかにしたい場合には、日常的に摂取している食品の種類と量を調査し、そのデータと機能性成分データベースとを組み合わせて、機能性成分の摂取量を推定し、それと健康との関連を検討する。このような研究手法においては、機能性成分データベースが必須の基礎データベースであることは容易に理解されるであろう。
サプリメント(=補足)という語から容易に理解されるように、人が通常の食品から摂取している機能性成分が人の健康にどのように、そして、どの程度関与(または寄与)しているのかを明らかにする研究が、サプリメントのように、ある機能性成分を高用量、人に与えた場合の健康効果を明らかにする研究に先んじるべきであることは自明である。ここに、機能性成分データベースの必要性がある。
2.脂肪酸成分データベースとイソフラボン成分データベースにみる先行事例
脂肪酸成分データベースとイソフラボン成分データベースについて触れてみる。1989年に日本食品脂溶性成分表(四訂フォローアップ脂溶性成分表)が公開されたことによって、わが国でも、脂肪酸摂取量の推定が可能になった。脂肪酸と血清脂質など、健康状態との関連は1965年ごろに明らかにされ、世界的に数多くの研究が進んだが、わが国では日本食品標準成分表の確立が遅れたため、人レベルでの研究は大きな遅れをとった。この四訂フォローアップ脂溶性成分表によって、この分野の研究がわが国でも進められる準備ができたわけであったが、残念ながら、欠損値(未測定食品)が多く、現実的には利用に耐えるレベルではなかった。そこで、佐々木らが欠損値の補完作業を行い、栄養疫学研究に用い得るレベルの成分表を1999年に作成した(Sasaki et al., 1999)。この日本食品標準成分表を用いた研究が複数の研究グループによって行われ、わが国においても脂肪酸摂取量と健康との関連を明らかにした報告数が増加した。そして、これらの報告はその後の健康政策の立案などに寄与した。
また、1999年には若井らが、続いて、2000年には荒井らが代表的な食品中のイソフラボン含有量を明らかにし、その成分表を作成した(Wakai et al., 1999、Arai et al., 2000)。これらの食品成分データベースも複数の研究グループによって用いられ、イソフラボン摂取量と健康状態との関連を明らかにするために寄与した。
これら数例をみても理解されるように、機能性成分データベースは、その食品成分の摂取量と健康状態との関連を明らかにするためには不可欠のものであり、その機能性成分の有効利用を図ることを目指すうえで、極めて重要なものであると考えられる。
3)機能性成分データベースの活用方法
1.活用目的
機能性成分データベースはさまざまな活用の可能性が考えられるが、中心となるものは、次の3つであると考えられる:a)機能性成分の摂取量調査や、摂取量と健康などとの関連を明らかにするための調査・研究目的で用いる場合、b)病院などで行われる食事指導で通常の栄養素に加えて、機能性成分の摂取量も把握して指導に用いる場合、c)消費者や生産者、食品加工業者・食品開発企業などが、興味をもっている食品に含まれている機能性成分の量を知るために用いる場合。
2.活用目的を考慮した機能性成分データベース開発の留意点
機能性成分データベースを用いる場合には、
機能性成分摂取量 = 食品1 g当たり機能性成分含有量 × 食品摂取量(g)
であるため、含有量の多い食品のみについて、成分値を収載するのではなく、食品摂取量も考慮して、機能性成分データベースに収載する食品を決定することが重要である。
上記のc)の目的に用いる場合は、ある種類の機能性成分を突出して大量に含有するような食品がもれることのないように注意して収載食品を決定すべきであろう。また、機能性成分データベース上はひとつの種類の食品でも、産地や収穫季節、栽培条件等、食品の部位など、さまざまな条件によって含有量は異なる。この数値のばらつきは、現在の日本食品標準成分表にすでに収載されている栄養素に比べてさらに大きいのではないかと推測される。その一方、ひとつの食品についてそれほど数多くの検体を測定することは不可能であろう。そこで、成分含有量のばらつきをあらかじめ考慮した測定方法が計画されなければならないとともに、その事実と、できればその程度について、機能性成分データベースに注意書きなどが添えられる必要があるかもしれない。
また、機能性成分はひとつではない。そして、機能性成分によってそれを含む食品は異なる。この事実を考えると、機能性成分データベースを一度に完成させることは不可能に近く、また、賢明なことではないであろう。現在の日本人における各機能性成分の推定摂取量や既存研究における健康効果など、さまざまな要素を勘案した上で、優先順位を設け、徐々に測定食品数や機能性成分の種類を増やし、一定の年月(例えば5年間から10年間)をかけて機能性成分データベースを完成させるような計画の立案が必要であると思われる。そのためのしっかりした長期ビジョンを早期に確立することが重要であると考えられる。
3 個別具体的な機能性成分に関する動向
1)代表的な機能性成分
1.フラボノイド
フラボノイドは、植物が生産する主要な二次代謝産物の一つであり、これまでに8,000を超える新規化合物が報告されている多様な物質である。
フラボノイドは、ギリシャ語の黄色を表す言葉であるフラバス(flavus)を語源としており、これまでは花色を形成する水溶性色素として注目され研究が行われてきた。この花色に関する研究分野の発展には、わが国の研究者が大きく関与しており、紫ツユクサの鮮やかな青色色素コンメリンは、アントシアニンのアシル化配糖体が亜鉛などの金属、さらには他のフラボノール類と複合体を形成し、安定化していることを明らかにしている。また、幻とまでいわれていた「青色のバラ」が、遺伝子組換え技術によりアントシアニン構造のB環に水酸基が連続して3個結合したデルフィニジンの生産を高めることによって育成されるなど、世界初の成果が得られている。
このような色素としての役割に関する研究に続き、フラボノイドは生物間相互作用における情報伝達物質の一つとしても注目を集めた。たとえば、植物を餌とする昆虫の摂食因子としての機能はカイコと桑の葉あるいはイネの葉とイナゴにおいて解明され、逆に忌避物質としての機能や産卵刺激物質としての機能なども数多く解明されている。また、植物と病原菌に対しても、フラボノイドは抗菌物質や抗ウイルス物質としての役割を果たしていることが知られている。さらに、マメ科の根粒形成における根粒菌の宿主認識物質としての機能、花粉に含有するフラボノイドの管伸長促進機能なども注目され、フラボノイドが植物においては、単なる老廃物として存在するのではなく、進化の過程における戦略物質として生産される重要な物質であることが認識されることとなった。こうした、生物間におけるフラボノイドの機能の解明は、動物を始めとするわれわれヒトに対する作用も連想させるものであるが、これまでは消化酵素の活性を阻害する物質あるいは苦味や渋味を示す物質として、飼料や農産物の分野ではむしろ低減化が図られるなど、マイナス要因として認識されてきた。
しかし一方、食品分野においては、フラボノイドが油脂類の酸化を防ぐ天然の抗酸化剤になり得るものとして、抗酸化性やラジカル消去作用など、その有用性に関する研究も古くから行われていた。そうした状況の中で、1984年に「食品機能」の概念が提唱され、食品成分による生体調節機能に関する研究が活発に行われるようになり、フラボノイドには試験管レベルにおける評価から、ラジカル消去作用のみならず、抗変異原性、抗腫瘍作用、抗炎症作用などが認められること、さらには動物実験による評価からがんリスク低減作用や動脈硬化リスク低減作用、脂質代謝改善作用、記憶学習能向上作用、アレルギー炎症低減化作用などが認められることが次々に明らかになり、現在は、これらの機能のヒトにおける実証とその作用機構の検証作業が活発に行われている。
以下に天然に存在する主なフラボノイドの分布について記載する。
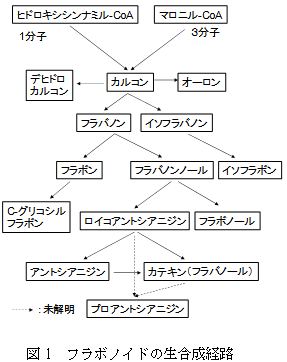
a)フラボノイドの種類と食品への分布
フラボノイドは、藻類を始めとするほとんどの植物に分布しており、液胞内に可溶性の状態で存在するのみならず、そのアグリコンが植物の表面や細胞壁に存在する場合や細胞質あるいはオイルボディーに存在する場合、さらには細胞内の核やタンパク質と結合して存在する場合など、様々な存在形態が明らかにされている。フラボノイドの生合成経路は、図1に示したとおりかなり複雑であるが、プロアントシアニジンの合成系を除いてほぼ明らかにされている。このうち、生理的機能性に関する研究が行われているものとしては、フラバノン、フラボン、フラボノール、カテキン、アントシアニンをあげることができる。これらについては、米国USDAによるフラボノイドデータベースが最も規模が大きい。わが国では、文部科学省プロジェクト(食品の非栄養性機能物質の解析と体系化に関する研究)において、機能性食品因子データベースが構築され、カロテノイドなどとともに掲載されているが、産地や収穫時期などにも対応した、より充実したデータベースの構築が待たれている。
a)‐1 フラバノン(ナリンゲニン、ヘスペリジン等)
フラバノンは、温州ミカンやグレープフルーツ、レモンなど全ての柑橘類果実中に苦味成分として存在しており、ナリンゲニンとその配糖体であるナリンジン、ヘスペレチンとその配糖体であるヘスペリジン、エリオジクチオールとその配糖体であるエリオシトリンなど、数多くの化合物が見いだされている。一方、ナッツ類ではアーモンドに少量、また野菜類の中ではトマト果実にナリンジンが存在することが分かっている。
代表的成分:ナリンジン(グレープフルーツ)、ヘスペリジン(マンダリン系柑橘)
a)‐2 フラボン(アピゲニン、ルテオリン等)、C‐グルコシルフラボン(ビテキシン、オリエンチン等)
食材に存在する主要なフラボンはアピゲニンやルテオリン、ジオスメチンをアグリコンとする配糖体であり、パセリやセロリなどのセリ科野菜がその供給源となっている。特にセロリにはアピゲニンの配糖体であるアピインが主要な配糖体として比較的多量に存在する。その他、ピーマンやパプリカ、唐辛子、レタスにもフラボン配糖体が存在する。一方、水酸基が高度にメチル化されたメチル化フラボンである、ノビレチン(ヘキサメトキシフラボン)やタンジェレチン(ペンタメトキシフラボン)が柑橘果実に存在し、マウスにおけるアディポネクチン産生増強作用などを示すことで注目されている。
一方、C‐グルコシルフラボンは、ビセニン‐2(vicenin 2 )、ビテキシンやイソビテキシン、オリエンチン、イソオリエンチンなどとして、柑橘果実果皮や雑穀類に含有されている。
代表的成分:アピイン(パセリ、セロリ)、ノビレチン(シークワーサー)、ビテキシンとイソビテキシン(柑橘果皮)
a)‐3 フラボノール(ケルセチン、ケンフェロール等)
フラボノールは、天然に最も広く存在するフラボノイドであり、ケンフェロールやケルセチン、ミリセチン、イソラムネチン、ラムネチンなどをアグリコンとする配糖体として、果実や野菜、穀類などほとんどの食材に含有されている。その中でも特に、ケルセチンをアグリコンとする配糖体であるルチンやイソケルシトリン、ケルシトリンなどは農産物の主要なフラボノイドであり、リンゴやクランベリー等のベリー類、ケールやレタス等野菜に比較的多量に含有されている。一方、タマネギやエシャロットに含有されるケルセチン配糖体は、B環の4'位の水酸基にグルコースが結合したスピラエオシド(Spiraeoside)と呼ばれる化合物および3、4'‐ジグルコシドが主体であり、他の食材とその性質がやや異なる特徴を持っている。ケンフェロールの主要な供給源としては、ニラやエンダイブ、ブロッコリー、ケールなどをあげることができる。
代表的成分:ケルセチン配糖体(タマネギ、リンゴ)、ケンフェロール配糖体(ニラ、ブロッコリー)
a)‐4 イソフラボン(ダイゼイン、ゲニステイン等)
イソフラボンは、大豆の主要なフラボノイドである。大豆のイソフラボンのアグリコンは、ダイゼインやゲニステイン、グリシテインをアグリコンとする配糖体であるダイジンやゲニスチン、グリシチンの糖部位にマロン酸が結合した形で存在する。イソフラボンは、ソラマメやピーナッツ、ヒヨコマメ等にも微量ながら存在する。また、デンプン原料であるクズにも少量存在する。
代表的成分:ダイゼイン配糖体とゲニステイン配糖体(大豆、クズ)
a)‐5 カテキン(エピカテキン、エピガロカテキンガレート(EGCG)等)
カテキンは樹木性植物に広く分布しており、B環の水酸基がカテコール型(カテキン)かあるいはピロガロール型(ガロカテキン)である場合が多い。また、2位と3位が不斉炭素であるため、4種類の立体構造をとり得るが、その多くは2R、3R型であり、マイナス値の旋光度を示す。わが国の食材の中では、緑茶がその主要な供給源になっている。緑茶には(‐)エピガロカテキンガレート((‐)EGCG)を主体とし、(‐)エピカテキンガレート((‐)ECG)、(‐)エピガロカテキン((‐)EGC)、(‐)エピカテキン((‐)EC)の4種類が主なカテキンとして存在し、乾物重量の15〜20%にも達する。この他、ブドウやリンゴ、モモ、ナシ、マンゴー、ネクタリン、プラム、ラズベリーなどの樹木性果実にも含有されているが、緑茶のカテキンと異なり、(+)カテキンや(‐)エピカテキン、(‐)エピガロカテキン等の遊離型カテキンが主体になっている。この他、イチゴには(+)カテキン、ルバーブには(+)カテキンと(‐)エピカテキン、ソラマメには(‐)エピカテキンや(‐)エピガロカテキン、(+)カテキン、ササゲとリョクトウには(‐)エピガロカテキンと(‐)エピガロカテキンガレートが存在することなどが知られている。
代表的成分:エピガロカテキンガレート(緑茶)、エピカテキン(緑茶、リンゴ)
a)‐6 アントシアニン(シアニジン、デルフィニジン、マルビジン等)
アントシアニンはロイコアントシアニンにアントシアニン合成酵素が作用して生じる。食素材中に存在する主なアントシアニンアグリコンは、B環の修飾状況が異なるペラルゴニジン、シアニジン、ペオニジン、デルフィニジン、ペチュニジン、マルビジンの6種類である。ビルベリーやブルーベリーは、このうち5種類のアグリコンを含有する食素材であり、この5種類がそれぞれグルコース、ガラクトース、アラビノースの配糖体となっていることから、合計15種類が果実中に存在することが分かっている。この他、黒豆や黒トウモロコシの黒色色素も実はアントシアニンのシアニジン‐3‐グルコシドであり、この他リンゴやモモ、サクランボ、桑の実など多くの果実の表皮にはアントシアニンが含有されている。最近では、このアントシアニンを含有する農産物の育成が盛んに行われており、紫黒米や紫サツマイモ、紫ジャガイモなどがすでに様々な加工品として製造・販売されるまでになっている。
代表的成分:シアニジン配糖体(黒豆、紫サツマイモ、黒トウモロコシ、リンゴ)、マルビジン配糖体(桑の実、ブルーベリー)
b) フラボノイドの生理的な機能性
フラボノイドが示す生体調節機能の多くは、その抗酸化作用とタンパク質との相互作用に基づくものである。抗酸化作用については、分子内のベンゼン環に隣り合った2個の水酸基を持つカテコール型と3個の水酸基を持つピロガロール型のフラボノイドが強い活性を持つことから、例えばケルセチンやカテキン類に関する研究が盛んに行われている。一方、タンパク質の相互作用についても、最近様々な研究報告が行われるようになり、フラボノイドが示す生体調節機能の本質を理解するための端緒になるものとして注目されて始めている。
b)‐1 各種酵素との相互作用
フラボノイドは、ATP‐結合タンパク質の機能を阻害することが知られており、ATPaseはもとより、PKCやPI3‐K、MAPKなどATPが関与する種々のキナーゼが影響を受ける。これら機能タンパク質のATP結合部位とフラボノイドの相互作用がその原因であるといわれている。一方、体内ではグルクロン酸や硫酸の抱合体として存在することから、この抱合体での阻害作用に関する研究も行われている。一般的には、これら抱合体の阻害活性はアグリコンより低くなるが、珍しい例としてケルセチン‐3‐グルクロニドは、アグリコンであるケルセチンよりも血管平滑筋細胞のMAPキナーゼを強く抑制するとの報告がある。
さらに、フラボノイドは各種酸化還元酵素の活性に影響を与えることが知られており、不飽和脂肪酸代謝に関与するリポキシゲナーゼやアラキドン酸カスケードに関与するシクロオキシゲナーゼ、さらにはメラニンの生産に関与するチロシナーゼ、活性酸素の生産系であるキサンチンオキシダーゼ、解毒などに関与するチトクロームP450などがその例である。
b)‐2 レセプターとの相互作用
アデノシンレセプターは、免疫系や心血管系、神経系などのホメオスタシスに関与するレセプターであるが、ある種のフラボノイドはこのレセプターとの相互作用を示す。また、副交感神経伝達物質であるGABAのAレセプター(塩素イオンチャンネル)との相互作用も見いだされている。こうした様々なレセプターとの相互作用からフラボノイドの生理的な機能性を解明するための研究に加えて、最近はフラボノイドが結合するレセプターを積極的に探索する研究も行われ、緑茶の主要なフラボノイドであるEGCGが、分子量67,000のラミニンレセプター(67LR)と結合し、このレセプターを介してがん細胞の増殖抑制作用や抗アレルギー作用を発現することを明らかにした。これに刺激を受け、今後はこのような比較的特異性の高いフラボノイドレセプターの探索が活性化するものと予想される。
b)‐3 受容体型転写因子等との相互作用
イソフラボンが核内受容体であるエストロジェンレセプター(ERα、ERβ)に強く結合し、女性ホルモン作用を示すことは良く知られている。大豆のイソフラボンであるゲニステインは、フラボンのアピゲニンやフラボノールのケンフェロールの6〜7倍強い結合性を持っているといわれている。また、抱合体化されたイソフラボンはERβとの結合性を示すが、その作用はアグリコンの10〜40分の1程度といわれている。ゲニステインのエストロジェン活性はERαとERβについてそれぞれ0.025%、0.8%と計算されている。また、フラボノイドは副交感神経伝達物質であるGABAのAレセプター(塩素イオンチャンネル)や、A1アデノシンレセプターとの相互作用を持つことが知られている。
一方、アリル炭化水素レセプター(AhR)は、ダイオキシンのレセプターとして注目される哺乳動物などの細胞、組織内に存在する受容体型転写因子であり、薬物代謝関連の酵素誘導などに関わっているが、このレセプターにフラボノイドが結合することが明らかにされ、受容体機能の発現と阻害の両面から詳細な研究が行われている。
この他、核内受容体であるペルオキシソーム増殖因子活性化受容体(PPAR)α、γとの相互作用も脂質代謝制御の観点から注目されている。
c)まとめ
フラボノイドの生理的な機能性に関する研究報告は、この10年間で急激に増加している。ケルセチンがヒーラー細胞や大腸ガン細胞の熱ショックタンパク質の生産を抑制し、がんの温熱療法抵抗性を緩和する作用を持つことが推定されてから15年が経過した。これは、食事として摂取した食品成分が、われわれの体組織に運ばれ、そこで遺伝子発現に影響を与え、様々な機能を発現する可能性を持つことを示した興味深い報告であった。最近は、DNAマイクロアレーを用いた遺伝子発現の網羅的な解析が可能になっている。数万の遺伝子に対する様々な食品成分の影響を解析することは個人の研究者にとっては容易なことではなく、市販の解析ソフトがグレードアップするまでは、得られた遺伝子発現データを正しく解析するため、メタボリックマップの全体を把握できるグループの形成が必要とされている。今後は、食品全体あるいは食事全体を評価するシステムとしてこのDNAマイクロアレー評価系を中心とするニュートリゲノミクス研究が発展することを期待している。
2.フェニルプロパノイド(カフェ酸、クロロゲン酸等)
a)フェニルプロパノイドの食品への分布
フェニルプロパノイドはフラボノイド合成の前駆体であるが、野菜や果実、穀類の主要なポリフェノール成分の一つとして、カフェ酸やフェルラ酸、クロロゲン酸として含有されている。このうち、フェルラ酸は細胞壁の構成成分としてほとんどの植物性食品に存在する普遍的な抗酸化成分であるが、特に含有量の多い素材は米糠であり、米糠のフェルラ酸は既に、抗酸化物質として市販されるまでになっている。
一方、カフェ酸とクロロゲン酸も分布範囲の広い抗酸化物質であり、クロロゲン酸はリンゴやナス、サツマイモ、ジャガイモの褐変に関与する成分として、古くは品質低下要因とされていた。最近は、これら成分の抗酸化作用が注目されるようになり、コーヒー生豆には5〜8%/乾物に達する程の含量が確認され、レギュラーコーヒーでは15 mgから325 mg、インスタントコーヒーで55〜240 mg程度含有されている。なお、代替コーヒーとして知られるチコリーやタンポポの根にもクロロゲン酸が含有されている。
b)カフェ酸、クロロゲン酸の生理的機能性
クロロゲン酸は腸管でカフェ酸とキナ酸に加水分解された後に吸収されることが分かっている。カフェ酸は吸収後に抱合体に変換されるとともに、さらにフェルラ酸やその抱合体として血液に存在する。
クロロゲン酸200 mgをヒトに摂取させると、胃酸の分泌が刺激され、カフェ酸も同様の作用を示す。また、クロロゲン酸はがん転移において重要な役割を果たすマトリックスメタロプロテアーゼ‐9の阻害作用を示すことや培養細胞系においてがん細胞の浸潤を抑制することが知られている。
一方、カフェ酸は炎症に関与する5‐リポキシゲナーゼ阻害活性を示すとともに、血栓溶解酵素を活性化する作用が報告されている。また、2型糖尿病のモデルマウスによる試験では、血糖値の低下作用とインスリン濃度上昇作用が確認されたことから、無作為試験によるヒト試験も実施され、クロロゲン酸を多く含む植物抽出物の摂取により、血糖値の低下が報告された。クロロゲン酸の抗糖尿作用については、グルコース‐6‐リン酸トランスロカーゼ活性阻害作用によるグルコース吸収の阻害やグルコース6フォルファターゼ阻害作用を介した肝臓でのグルコース吸収阻害などが推定されているが、より詳細な研究が必要とされている。
3.カロテノイド
野菜や果実を彩る脂溶性の色素成分がカロテノイドであり、天然界には600種類が存在するといわれている。このうち、われわれが日常の食生活の中で摂取する種類は約40種類で、ヒト血漿からは10種以上のカロテノイドやその代謝物が検出されている。
カロテノイドの語源は、最初に発見されたニンジン(キャロット)に由来しており、炭素と水素のみからなるカロテンと炭素と水素の他に酸素が構成元素となるキサントフィル類に分類されている。カロテノイドの最も重要な生理的機能はプロビタミンA活性であり、β‐カロテンやα‐カロテン、β‐クリプトキサンチンがビタミンAに変換される。
カロテノイドについては、食品機能性研究が開始される1984年よりも前から抗がん作用に関する研究が行われており、1980年代には既に大規模ヒト介入試験が行われた。その一例として中国の林県で行われた研究(Linxian Study)が良く取り上げられるが、この研究ではβ‐カロテンの摂取が発がんを抑制することを示唆する結果が得られている。しかし、その後に実施された大規模介入試験では、発がん抑制については否定的な結果が得られており、単一のβ‐カロテンを過剰に摂取することは、食品から摂取する場合と異なり、体内への蓄積濃度が違うなどとする議論がなされている。
最近では、クリプトキサンチンやアスタキサンチン、リコペン、ルテインなどβ‐カロテン以外のカロテノイドの生理機能に対する関心が寄せられ、多くの研究が行われているので、以下に記載する。
a)カロテノイドの種類と食品への分布
食品には多数のカロテノイドが含有されているが、生理的な機能に関する研究が行われているものは限られており、α‐カロテン、β‐カロテン、β‐クリプトキサンチン、リコペン、ルテイン、ゼアキサンチン、アスタキサンチン、フコキサンチンなどが良く取り上げられている。この他、ヒトエンやζ‐カロテン、ネオキサンチン、ビオラキサンチン、カンタキサンチンなども健康の維持増進に寄与している可能性が高いが、今後の研究をまたなければならない状況である。
これらの化合物に関するデータベースとしては、米国USDAによるカロテノイドデータベースが最も規模が大きい。欧州では、英国、アイルランド、スペイン、フランス、オランダの関係者の協力によるデータベースが良く知られている。一方、わが国では、五訂増補日本食品標準成分表に、α‐カロテン、β‐カロテン、β‐クリプトキサンチンのデータが収載されている。また、フラボノイドと同様、文部科学省のプロジェクト研究によって作成された機能性食品因子データベースがあるが、その他に寺尾等の報告、渡辺らの報告も、Yanoらの報告、Aizawaらの報告が、わが国の食品におけるカロテノイド含量の実態を把握する上で役立っている。
a)‐1 α‐カロテン
ニンジン、アプリコット、カボチャ、野菜ジュースに0.1 mg/100g以上含まれる。食品の摂取量と含量から予測すると、最も重要な摂取源はニンジンで総摂取量の80〜90%を占めると言われている。
a)‐2 β‐カロテン
ニンジン、メロン(赤肉種)、アプリコット、グアバ、ビワ、マンゴー、パパイア、ブロッコリー、ケール、レタス、ピーマン、カボチャ、ホウレンソウ、サツマイモなどには1 mg/100g以上含まれる。最も重要な摂取源はニンジンで、総摂取量の半分を占める。次いでホウレンソウなど緑色の濃い葉菜類、ピーマン、カボチャなどの果菜類の順である。
a)‐3 β‐クリプトキサンチン
温州ミカン、ビワ、柑橘類、柿、パパイア、モモには、0.1 mg/100g以上含まれる。重要な摂取源は、わが国では温州ミカンである。
a)‐4 リコペン
トマト、スイカ、グレープフルーツ(赤肉腫)、柿、グアバ、パパイアには0.1 mg/100g以上含まれる。最も重要な摂取源はトマトである。
a)‐5 ルテイン
カブラナ、ホウレンソウ、ズッキーニ、レタス、ケール、芽キャベツ、ブロッコリーには0.1 mg/100g以上含まれる。ホウレンソウなど緑色の濃い野菜とブロッコリーが重要な摂取源で約80%を占める。
a)‐6 ゼアキサンチン
トウモロコシ、ネクタリン、ネーブルオレンジ、パパイア、モモ、温州ミカン、タンカン、柿などには0.1 mg/100g以上含まれる。特に目立った摂取源はない。
a)‐7 アスタキサンチン
アスタキサンチンは、鮭や鱒、鯛、イクラに存在するが、藻類から大量に調製可能であるため、最近はサプリメントなどとして市販されている。
a)‐8 フコキサンチン
フコキサンチンは海草に含まれるため、わが国では重要なカロテノイドの一つである。カットワカメに0.989 mg/100g含まれる。
b)カロテノイドの代謝と疾病リスク低減作用
b)‐1 がん予防
カロテノイドのがん予防作用については、多くの疫学調査研究によって有効性が推定されており、その主な作用メカニズムとしては、1.細胞周期の阻害、2.分化誘導作用、3.アポトーシス誘導作用などが報告されている。
カロテノイド摂取と肺がんとの関係について実施された、1993年から2004年までの疫学調査研究の結果では、1998年に実施されたスペインにおける症例対照研究と2002年に実施されたカナダコホート研究において、カロテノイド摂取との相関性は認められていないが、2003年に報告された日本におけるコホート研究も含め9件については、何らかの効果が認められている。
表1‐2.カロテノイドの疾病リスク低減に関するこれまでの疫学調査研究
| 調査(年) | 対 象 | 主な成果 |
|---|---|---|
| ハワイコホート研究(1993) | 患者332名 対象者855名 |
α-カロテン、β-カロテン、ルテインを多く食べたグループは肺がんのリスクが低い。 |
| 米国メリーランド州ワシントン(1997) | 患者258名 対象者515名 |
患者群は対照者に比べて血中のβ-カロテン、ルテイン/ゼアキサンチン、クリプトキサンチン濃度が低い |
| スペイン症例 対照研究(1998) |
患者103名 対象者515名 |
α-カロテン、β-カロテン、ルテインの摂取と肺がんリスクとの相関がない。 |
| ウルグアイ症例対照研究 | 患者541名 対象者540名 |
総カロテノイド摂取量の多いグループでの肺がんリスクは有意に低下。 |
| フィンランドコホート研究(1999) | 患者138名 | α-カロテン摂取量の多いグループでの肺がんリスクは有意に低下。β-カロテンもリスクを低減するが有意差はなし。 |
| 米国コホート研究(2000) | 患者797名 | α-カロテン、リコペン、総カロテノイドともに摂取量の多いグループは、肺がんのリスクが有意に低下。 |
| 中国上海コホート研究(2001) | 患者209名 対象者622名 |
血清β-クリプトキサンチンの高いグループは肺がんのリスクが低い。 |
| カナダコホート研究(2002) | 患者155名 対象者5631名 |
α-カロテン、β-カロテン、β-クリプトキサンチン、リコペン、ルテインと肺がんリスクとの相関はない。 |
| 日本コホート研究(2003) | 患者147名 対象者311名 |
α-カロテン、β-カロテン、カンタキサンチン、総カロテノイドの高いグループは肺がん死率が有意に低い。リコペン、β-クリプトキサンチンも肺がんリスクを低減するが有意差はない。 |
| シンガポール居住の中国人(2003) | 患者482名 | 食事性β-クリプトキサンチンが低いグループは肺がんリスクが有意に高い。他のカロテノイドには有意差なし。 |
| 米国とヨーロッパの7つのコホート研究分析(2004) | 患者数482名 対象者3155名 |
食事性β-クリプトキサンチンが低いと肺がんリスクが有意に高い。他のカロテノイドは有意差なし。 |
これらの結果は、カロテノイドの摂取が肺がんの予防に貢献する可能性を示すものであるが、しかし1985年から1993年にかけて実施されたフィンランド喫煙男性に対する大規模なβ‐カロテンとビタミンEの介入試験と1988年から1998年にかけて実施された米国の喫煙者・アスベスト暴露者に対するβ‐カロテンとビタミンEの介入試験では、むしろ肺がんリスクが増加する可能性が示された。これら二つの介入試験においては、カロテノイドの摂取推奨量3 mg/日の10倍近い投与が行われていたことから、血中での濃度が過剰になり、むしろ酸化が促進されたのではないかとの推定がなされている。脂溶性成分は摂取後に肝臓などの組織に蓄積されるが、単一成分を多量に摂取することにより、他の脂溶性成分の組織分布が低下する可能性も指摘されており、脂溶性成分の適切な摂取のあり方に関する知見が必要になっている。
野菜や果物には、β‐カロテンの他にリコペンやα‐カロテンなど多様なカロテノイドが存在し、それらの中にはβ‐カロテンよりも強い抗腫瘍活性を示すものもある。リコペンは、トマトとスイカの色素成分であるが、経口摂取後に精巣に分布する性質を持つことから前立腺がんリスクの低減作用に関する研究が多く実施されており、2007年の世界がん予防協会がとりまとめた報告書によると、前立腺がんの予防作用は「ほぼ確実(Provable)」であるとされている。
この他、海藻に含有されるカロテノイドのフコキサンチンのアポトーシス誘導作用が明らかになり、動物実験においても抗腫瘍作用が確認されている。また、複数のカロテノイドミックスの投与がヒトにおいて肝硬変から肝がんへの移行を予防するとの研究成果も得られており、がん予防に対するカロテノイドの効果的な摂取方法の開発が期待されている。
b)‐2 血管系疾患の予防
カロテノイドは、血中のLDLやHDLなどのリポタンパクと共存していることが分かっており、酸化LDLが関与する動脈硬化の発症の予防作用が期待されている。これまでの疫学調査研究によると、野菜に多く含有されるカロテノイドであるルテイン摂取と虚血性心疾患リスクが負の相関を示すこと、喫煙者のクモ膜下出血のリスクはβ‐カロテンやリコペンとルテインの同時摂取で低下するなど、総カロテノイドやβ‐カロテンの摂取や血清濃度と心臓血管系疾患リスク低減との関連性が強いことが数多く報告されている。例えば、1.フィンランド人を対象とした食事歴調査から、カロテノイド摂取と心臓疾患死が負の相関を示すこと、2.オランダのロッテルダムにおける4年間の追跡調査では、β‐カロテンの高摂取群において心臓疾患リスクが低いこと、3.米国における追跡調査では、血清総カロテノイドの高い群と冠状動脈性心疾患リスク低減に相関が見られ、非喫煙者で明らかであったなどの報告がある。しかし、発がん予防と同様に、介入試験によるβ‐カロテン摂取の有効性はまだ認められておらず、これまでの研究では投与したβ‐カロテンの濃度が高すぎたのではないかなどの推定がなされている。
b)‐3 加齢性網膜黄斑変性病と白内障
加齢性網膜黄斑変性病は欧米の高齢者で高率に発症する疾病であるが、最近はわが国でも増加傾向にあるといわれている。
人間の網膜とレンズには、ルテインとゼアキサンチンが特異的に存在し、光による組織の酸化を抑制しているものと推定されているため、これらの摂取が目の健康維持に有効であるとの視点に立った多くの研究が行われている。最近、ユタ大学のグループが網膜細胞にルテインや他のキサントフィル類に親和性の高い結合タンパク質XBPを見いだし、これが網膜におけるルテインとゼアキサンチンの輸送と代謝に深く関わっていることが明らかになってきたことから、これらの成分の保護効果に対する期待が高まっている。
ルテインやゼアキサンチンが網膜とレンズに蓄積して視覚機能を保護する作用については、これをビタミン作用と位置づける研究者もでてきた。実際に、ヒト代替モデル動物としてのベンガルザルにルテインフリー食を与えると、網膜から色素が抜け網膜黄班症となり、これにルテインを摂取すると回復することが明らかになっている。ビタミンであることの証明には、代替成分の存在などさらに試験を行う必要があるものの、ビタミンAがロドプシンの構成成分であることに加え、さらに類似成分のルテインやゼアキサンチンも目の必須成分として働いている可能性に対する興味が高まっている。
表1‐3.カロテノイドの眼性疾患に対するこれまでの疫学調査研究
| 対照者(報告年) | 投与方法 | 結果 |
|---|---|---|
| 加齢性網膜黄班(AMD)疾患者 男性14人 | ホウレンソウ140g(ルテイン14mg含有)または精製ルテイン14mgを投与 | 視力機能の改善 |
| 色素性網膜炎患者 16人 |
ルテイン40mg/9週間、続いて20mgを17週間 | 視力の改善 |
| AMD患者 50人 | ルテイン15mg/日を含む抗酸化カクテルを毎日、18ヶ月摂取 | プラセボに比べて視力が2倍回復 |
| AMD患者 90人 | ルテイン10mg/日または(ルテイン10 mg+混合抗酸化剤)/日、12ヶ月 | 網膜色素量、眩輝(眩しさ)、感受性及び視力の改善 |
| 白内障患者 5人 | ルテイン15mg/日を2年間摂取 | 視力、眩輝の改善 |
b)‐4 皮膚障害
ミカンの摂取に伴い、皮膚が黄色になることは多くの人々が体験しているとおり、カロテノイドは皮膚に蓄積する性質を持っている。このことから、抗酸化成分であるカロテノイドは、光暴露によって生成する活性酸素を消去し、皮膚を保護する役割を持っているものと推定されている。
実際、藻類のドナリエラ由来のカロテノイド(94%がβ‐カロテン)を1日あたり24 mgあるいは段階的に投与量を増加して摂取した場合、紫外線暴露により生成する紫斑が抑制され、血清中の過酸化脂質量が減少することが示されている。また、トマトペーストを1日あたり40 g(リコペンとして16 mg)を10週間食することにより、紫外線により誘導される紫斑が非摂取群に比べて抑制されることも明らかになっている。
b)‐5 その他免疫機能など
カンタキサンチンやルテイン、リコペン、アスタキサンチンは、免疫機能を司るヘルパーT細胞や、がん細胞の増殖を抑制するナチュラルキラー細胞を活性化することが知られている。ヒトに対する介入試験では、低カロテノイド食ではTリンパやヘルパーT細胞のマーカーが減少し、トマトジュース摂取により回復するなどの報告が行われている。また、アレルギーについては、β‐カロテンとα‐トコフェロールの同時摂取がIgE産生を抑制することも明らかになっている。
また、最近の研究では温州ミカンに含有されるβ‐クリプトキサンチンの血清濃度が高いグループは低骨密度者の割合が低いことなども疫学調査研究で示されており、カロテノイドの多様な生理機能が注目され始めている。
4.イソチオシアネート
イソチオシアネートは、アブラナ科野菜に含有されるグルコシノレートが野菜組織の傷害などに伴い、ミロシナーゼによって分解されて生じる化合物であり、ワサビや辛子の辛味物質の本体であるアリルイソチオシアネートは、グルコシノレートのシニグリンにミロシナーゼが作用して生じる典型的なイソチオシアネートである。
これまでに、多くの疫学調査研究によってキャベツなどのアブラナ科野菜の摂取が、肺がんなどを抑制することが示されてきたが、この作用の多くは、キャベツから生成したイソチオシアネートが肝臓の解毒酵素であるグルタチオンS‐トランスフェラーゼやキノンレダクターゼを誘導し、発がん物質の毒性を低下させることによってもたらされるものと推定されている。
a)イソチオシアネートの種類と食品への分布
これまでに、16科の双子葉植物に120種以上のグルコシノレートが見いだされている。その中で、われわれが日常的に良く摂取するアブラナ科野菜について、多くの研究が行われている。
主な、アブラナ科野菜に含有されるグルコシノレートを表に示した。グルコシノレート組成は品種間差異があり、キャベツではアリル、3‐メチルスルフィニルブチルなど、ブチル基を修飾したグルコシノレートが、白菜には4‐ペンテニルグルコシノレートなどペンチル基を修飾したグルコシノレートが多く含有されるとの報告がある。
なお、一般的にイソチオシアネートは、野菜に存在するミロシナーゼが作用することによって生じることが知られているが、最近は、腸内細菌もこのミロシナーゼ活性を持っていることが明らかになり、野菜に存在するグルコシノレートが腸内で腸内細菌によってイソチオシアネートに変換されることも明らかになっている。
これまでに研究されてきた代表的なイソチオシアネートは、ワサビや辛子油の辛味の本体である1.アリルイソチオシアネートと2.6‐メチルスルフィニルヘキシル‐ITC(6‐HITC)、キャベツやクレソンに含有される3.ブチル‐ITC(BITC)や4.フェニル‐ITC(PEITC)、ブロッコリーから生じる5.スルフォラファンなどである。
表1‐4.各種野菜に存在するグルコシノレート類
| 野菜名 | グルコシノレート残基 | グルコシノレートの慣用名 →イソチオシアネート名 |
|---|---|---|
| カブ | (R)-2-hydroxy-3-butenyl- 3-indolylmethl- 2-phenylethyl- |
プロゴイトリン(progoitorin) グルコブラシシン(glucobrassicin) グルコナスツルティイン(gulucona-sturtiin) |
| キャベツ ブロッコリー 芽キャベツ カリフラワー |
allyl- 3-methylsulfinylpropyl- (R)-2-hydroxy-3-butenyl- 4-methylsulfinylbutyl- 2-phenylethyl- 3-indolylmethyl- |
シニグリン(sinigrin)→アリルイソチオシアネート グルコイベリン(glucoiberin) プロゴイトリン(progoitorin) グルコラファニン(glucoraphanin)→スルフォラファン グルコナスツルティイン(gulucona-sturtiin) グルコブラシシン(glucobrassicin) |
| ダイコン | 4-methylthio-3-butenyl- 3-indolylmethyl- |
4MTB グルコブラシシン(glucobrassicin) |
| ワサビダイコン | allyl- 2-phenylethyl- |
シニグリン(sinigrin) →アリルイソチオシアネート グルコナスツルティイン(gulucona-sturtiin) |
| ワサビ | allyl- 1-methylpropyl- |
シニグリン(sinigrin) →アリルイソチオシアネート |
| カラシ | allyl- 3-butenyl- |
シニグリン(sinigrin) →アリルイソチオシアネート グルコナピン(gluconapin) |
| シロカラシ | p-hydroxybenzyl- | シナルビン(sinalbin) |
b) イソチオシアネートの生理的機能性
b)‐1 がん発症リスクの低減作用
生体に侵入した異物の多くは、異物代謝酵素によって修飾を受け、水溶性を増して体外へ排泄される。この異物代謝は2段階に分けられ、第一段階はチトクロームP450に代表される第1相解毒酵素群による生体異物酸化反応、還元反応または加水分解反応である。第2相反応は、グルタチオンS‐トランスフェラーゼ、UDP‐グルクロノシルトランスフェラーゼ、スルフォトランスフェラーゼなどの抱合酵素による抱合・転移反応や、NAD(P)H:キノンオキシドレダクターゼやアルデヒドデヒドロゲナーゼなどによる還元反応である。これまでの研究によると、第一段階の反応は発がん物質を活性化する反応であり、第二段階反応が解毒に関与する反応であることが分かっている。従って、第一段階の反応を抑制し、第二段階の反応を活性化することができれば、発がんのリスクを低減することが可能になる。
これまでの研究によるとブロッコリーから生じるイソチオシアネートのスルフォラファンは、この第二段階反応酵素(第2相酵素)の遺伝子発現に関与するNrf2/Keap1に作用し、転写因子でありNrf2のkeap1からの遊離を促進して転写活性化を行うものと推定されているが、その後の研究により、スルフォラファンのみならず、6‐HITCやBITC、PEITCにも同様の活性が存在することが分かっている。
また、これまでの研究によると、BITCやPEITCは大腸がん由来の培養細胞においてアポトーシスを誘導することが報告されている。AITCでは、特定の細胞株に対して顕著なアポトーシス誘導を行うことが分かっていることから、このアポトーシス誘導作用もがん発症のリスク低減に関与するものと推定されている。
これまでの疫学調査研究では、ニュージーランドのマオリ族と非マオリ族の比較研究があり、マオリ族は脂肪や赤身肉、アルコールの摂取が多く、一般の野菜類の摂取量も少ないにもかかわらず大腸がんが有意に少なく、これはマオリ族が特異的に摂取するクレソンのPEITCに由来するものであると推定されている。
このPEITCについては、タバコ特異的ニトロソアミンの代謝活性化に直接関与する第一相酵素のチトクロームP450、2A6、2A13を抑制し、肺がんリスクの低減に寄与している可能性のあることが示された。
b)‐2 血液凝固抑制作用
血液凝固の亢進は、エコノミー症候群のみならず心筋梗塞や脳梗塞などの引き金になることから、生活習慣病予防の視点からはその抑制作用が検討されている。これまでに、ニンニクやタマネギのアリルメチルトリスリフィドやジアリルジスルフィド等の含硫化合物の抑制作用が知られているが、イソチオシアネート類にも同様の作用が確認されており、特にキャベツやブロッコリーなどに含有されるメチルチオアルキルイソチオシアネート(ω‐MSITC)の作用が強く、アスピリンの約10倍に匹敵するとされている。これらは、まだ動物実験レベルでの確認ではあるが、摂取後に吸収され血液中に存在することも既に確認されており、人間への有効性が期待されている。
2)その他の機能性成分
1.リグナン
リグナンは、C6‐C4‐C6の構造を持つポリフェノール類で、最も有名な化合物はゴマに存在する脂溶性のセサミンとセサモリン、水溶性のセサミノール配糖体であり、セサミンとセサモリンはゴマ種子中にそれぞれ0.3〜0.5%含有されている。セサミン、セサモリン、セサミノールの構造は水酸基がメチレン基を介して閉じた構造になっているが、生体に吸収された後は代謝され、これが開裂してメトキシ基と水酸基となり、抗酸化性を示すことが知られている。
a)ゴマリグナンの生理的機能
a)‐1 セサミンの生理的機能
セサミンは動物実験により血清コレステロールの低減化や脂肪代謝の亢進を行うことが知られている。この作用については、ラットやマウスを用いた詳細な生化学実験が実施されており、セサミンは肝臓の脂肪酸代謝合成酵素の活性を抑制するとともに、肝臓や脂肪細胞のミトコンドリアやペルオキシゾームの脂肪酸酸化酵素系を活性化し、体内の脂肪を燃焼させる方向に導くことが明らかになっている。この作用についてはDNAマイクロアレーに研究も進められており、肝臓における脂肪酸合成酵素遺伝子の発現抑制と脂肪細胞における脂肪酸分解酵素遺伝子の発現抑制作用が確認され、その作用はペルオキシゾーム誘導剤活性化受容体(PPAR)に対するリガンドとして作用することによるものであるとされている。
このセサミンの脂質代謝活性化作用は、魚油に豊富なDHAなどの高度不飽和脂肪酸と同時摂取することにより、その作用はさらに高まることも分かっており、抗酸化物質であるポリフェノールと酸化されやすい高度不飽和脂肪酸の組み合わせが有効であることを示している。この他、セサミンにはアルコール分解促進作用、血圧上昇抑制作用なども動物実験で確認されている。
なお、セサミンの一部はゴマ油の精製過程でエピセサミンに変換するが、このエピセサミンの方がセサミンよりも脂肪酸合成抑制や脂肪酸代謝促進作用が強いことが最近の研究によって明らかにされている。
a)‐2 セサモリンの生理的機能性
動物実験においては、セサモリンもセサミンと同様に生体内抗酸化作用が報告されているが、セサミンに比べて研究例は少ない。最近の研究によると、セサモリンはセサミンよりも脂肪酸合成抑制作用と脂肪酸分解促進作用が強く、さらにエピセサミンを凌ぐ活性を持つことが明らかになった。これは、セサモリンがセサミンに比べて消化管からの吸収が良く、また肝臓での分解代謝が遅いため、生体内で濃度が高く維持されるためであることが分かった。エピセサミンがセサミンよりも強い機能を示す理由も、セサモリンと同様に腸管吸収が良くさらに分解代謝が遅いためであると推定されている。
a)‐3 セサミノールの生理的機能性
セサミノールは大量精製が遅れていたことから、これを実験材料として用いる研究者がいないため、その機能性に関する研究は遅れていた。最近、ようやく研究が行われるようになり、セサミノールはセサミン等よりも生体内での抗酸化作用が強いことなどが明らかにされつつある。LDLの酸化抑制についても、ゴマリグナンの中では最も強い作用を示すことから、セサミノールは今後抗酸化成分として利用が期待されている。
2.スチルベノイド(レスベラトロール等)
スチルベノイドはC6‐C2‐C6の構造を持つポリフェノールの仲間であり、食品においてはブドウ果実やワイン、ピーナッツに存在することが分かっている。ワインにレスベラトロールが存在することが明らかになったのは1992年のことで、比較的新しい。ブドウ樹体では葉に最も多く、次が果皮であり、元々は有害微生物の侵入を阻止するためにブドウ樹体が生産するファイトアレキシンであると認識されていた物質である。
これまでに、レスベラトロールは、LDLの酸化を抑制し動脈硬化のリスクを低減する可能性があること、血小板凝集を抑制して血栓の形成を予防することなどが報告されている。この他、がん発症のイニシエーションやプロモーション、プログレッションも抑制することや、マウスの実験では皮膚がんを最大98%抑制するなどの研究成果が得られている。また、レスベラトロールはMAPキナーゼを活性化し、記憶や学習能を向上させる可能性があることが示され、レスベラトロールを含有するワインの認知症やアルツハイマー病のリスク低減作用に関する疫学研究が行われている。
3.ジンゲロール、クルクミン
ジンゲロールとクルクミンはショウガ科に特有な成分であり、ともに機能性成分として生活習慣病のリスク低減作用を示すものとして期待されている。
a)ジンゲロールの生理的機能性
ショウガの辛味成分は、o‐メトキシフェノール構造を持つ6‐ジンゲロールであり、この化合物の水酸基が脱水されたものはショーガオールと呼ばれる。これらショウガ由来のポリフェノールの機能性については、1.抗酸化作用や2.抗血栓作用が最も良く研究されている。他に、3.抗炎症作用や4.発がんプロモーション抑制作用、5.抗高脂血症、6.血管新生抑制作用などが知られている。最近、最も研究されている生理的機能は、交感神経系の活性化による7.熱産生作用である。ジンゲロールは、ベンゼン環部分の構造がバニリンと同じであるため、バニロイドレセプターのアゴニスト(類似作用を示す物質)としての働きを持ち、体熱産生亢進機能を示すことが分かっている。
b)クルクミンの生理的機能性
クルクミンはショウガ科のウコンに存在する黄色色素であり、ターメリックとしてカレー料理に用いられる。ウコンは漢方薬としては止血剤や健胃剤として用いられ、抗菌作用や抗炎症作用も知られている。最近は、ウコンエキスの肝機能改善効果が特に有名になっており、飲酒の前に摂取することが民間伝承的に行われるまでになっている。
ウコンは、東南アジア諸国では化粧品としても利用されている。これは、クルクミンの1.皮膚発がんや紫外線による皮膚障害予防効果を期待したものであり、動物実験では有効性が確認されている。一方、経口摂取ではがん発症リスク低減効果が検討されており、2.前胃、十二指腸、大腸などの消化器官や肝臓、肺、軟口蓋での発がん抑制作用が動物実験で確認された。この分子機構の一つとして、肝臓の薬物代謝に関与する第1相酵素の阻害と第2相酵素の活性化が報告されている。
また、生体内におけるクルクミンの強い抗酸化作用とともに、アポリポタンパク質EとLDLレセプターの二重ノックアウトマウスを用いた実験による3.動脈硬化症のリスク低減作用も確認されており、幅広い薬理学的応用が期待されている。
さらに、クルクミンには強力な抗炎症作用が確認されており、その分子機構としてはIκB燐酸化酵素経路の活性化によるNFκBの不活性化によるシクロオキシゲナーゼ‐2遺伝子の発現抑制作用が推定されている。NFκBは生体内の様々な機能亢進に関与することから、クルクミンはその抑制剤としての潜在性が期待されるようになっている。
一方、クルクミンは生体内利用性は低いものと推定されており、クルクミンを摂取した際に生体で生じるテトラデヒドロクルクミンが注目を集めている。このテトラデヒドロクルクミンは、大腸がん、腎臓がん、白内障、血清コレステロール低減作用を示すことが動物実験などにより明らかにされている。
3)機能性成分の分析方法
1.定量分析法の妥当性確認の必要性
行政により使用される分析法の要件として、同じ分析用試料について、どこの試験室の人でも一定の技能をもった人が測定した時には、一定の範囲内で結果が一致(同等性)することが求められる。そのためには、試験室間共同試験(以下、室間共同試験)によって分析法の妥当性確認を行う必要がある。分析法の妥当性確認とは、意図する特定の用途に対して個々の要求事項が満たされていることを調査によって確認し、客観的な証拠を用意することである(ISO/IEC17025)。
a)試験室間共同試験による妥当性確認のための国際調和プロトコル
IUPAC(国際純正応用化学連合)等の国際機関による室間共同試験のプロトコルでは、外れ値検定後に残る最少試験室数を8、室間共同試験に用いられる最少試験材料数を5と規定している。
a)‐1 試験材料の調製
最少5種類の材料は、マトリックスと濃度の組合せで考え、マトリックスは規制(規格)の対象食品の定義にあうものを包含し、濃度は規制(規格)濃度付近で十分な精度が得られることを確認できるように設定する。
試験室内での分析精度を調べるための材料の推奨順位は、1.濃度が5%未満の違いがある材料(ユーデン対)、2.ユーデン対と非明示反復の組み合わせ、3.非明示反復、4.明示反復、5.独立測定である。非明示反復は、同一の材料をそれと分からないようにして2回測定させる意味である。
a)‐2 室間共同試験の実施
8以上(外れ値を報告する試験室がでることを想定して、できれば10〜14)の試験室に、最少5種類の材料を配付する。この時、室内での分析精度の情報を得るためには、例えば、5種類の材料が非明示で2点ずつなら、計10点がコード番号のみを付けて配付される。
各試験室において配付試料の分析は、1点につき1回の分析のみ行い、複数回の分析は行わない。試験室は、手順書通りに分析を行うことが極めて重要であり、変更は許されない。
a)‐3 統計解析
報告されたデータに異常が認められ、聞き取り調査の結果、それが手順書の逸脱などによる場合は、その試験室の分析値を全て除外する。残った試験室のデータについて、統計解析で外れ値検定を行う。コクラン、シングルグラッブス及びペアグラッブス検定を、外れ値が出なくなるか、検定開始時(異常値を報告した試験室を除外した後)の試験室数の2/9(22.2%)を超える手前まで、順次、繰返して行う。
外れ値検定を終了したデータで、室間再現相対標準偏差を求める。
化学分析値の室間再現相対標準偏差の評価には、HorRat(Horwitz Ratio)が用いられている。これは、実施した室間共同試験による再現相対標準偏差とHorwitz 式で計算された予測再現相対標準偏差との比を用いるもので、コーデックス委員会では、2以下であれば、受け入れられるとしている。
HorRat = RSDR,%(試験値) / PRSDR,%(Horwitz 式からの予測値)
Horwitz 式は、分析対象成分の濃度から、使用した分析法の室間再現相対標準偏差を予測するもので、予測室間再現相対標準偏差(PRSDR%)は、次式で示される。
PRSDR(%) = 2C ‐0.1505
C に、分析対象成分の濃度が100%であれば1を、1%なら0.01を、1 ppmなら10‐6 を代入すれば、その濃度における再現相対標準偏差の予測値が求められる。
高濃度及び低濃度については、Thompson により次の修正式が提案されている。
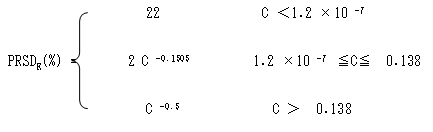
b)単一試験室による妥当性確認
b)‐1 コーデックス委員会の手続きマニュアル
試験室間共同試験によって妥当性が確認された方法が、必ずしも利用できるとは限らない。単一試験室によって妥当性確認された方法は次の規準を満たさなければならない。
- 方法は、国際的に認知されたプロトコルに従って妥当性が確認される。
- 方法の使用は、ISO/IEC17025あるいはGLPの原則に適合した品質システムの中で行われる。
- 方法は精確さに関する情報を補足するべきである。
- 可能なら、定期的なproficiency schemes への参加。
- 可能なら、認証標準物質を使用する校正。
- 分析種の想定濃度における回収率試験。
- 可能なら、他の妥当性が確認された方法による結果の検証。
[General Criteria for the Selection of Single‐Laboratory Validated Methods of Analysis(Procedural Manual, 14th edition, CAC)]
b)‐2 単一試験室による妥当性確認の国際調和プロトコル
単一試験室による分析法の妥当性確認は、次のようなものを含むいくつかの状況で適切である。
- 費用がかかる本式の共同試験前の分析法の実行可能性を確実にする。
- 共同試験のデータがないか、共同試験の実施が現実的でない場合に、分析法の信頼性の証拠を提示する
- 既存の妥当性が確認された分析法が正しく使用されていることを確実にする。
b)‐2‐1 妥当性確認試験の範囲
分析法の典型的な性能特性は、適用性、選択性、検量線、真度、精度、回収率、操作範囲、定量限界、検出限界、感度および堅牢性である。これらに、測定の不確かさと目的適合性を加えることができる。
試験室が、新しい、改良した、あるいは慣れていない分析法の妥当性確認をしなければならない範囲は、分析法の現在の地位および試験室の能力の程度による。異なる状況のための妥当性確認や検証の量目の範囲に関する提案は、以下の通りである。特別に言及しなければ、分析法は経常的な使用を意図していると仮定している。
[1] 試験室は十分に妥当性確認された分析法を使用する予定である。
分析法は共同試験で検討されており、試験室は分析法の公表された性能特性を遂行することができること(あるいは、分析の仕事の要求を満たすことができること)を検証しなければならない。試験室は、精度、かたより(マトリックスによる変動を含む)、できるなら検量線の直線性を検討すべきである。堅牢性に関するようないくつかの検討は外すことができる。
[2] 試験室は十分に妥当性確認された分析法を使用するが、新しいマトリックスに適用する予定である。
分析法は共同試験で検討されており、試験室は新しいマトリックスが分析システムに新しい誤差の原因を持ち込まないことを検証しなければならない。前者と同じ妥当性確認の範囲が要求される。
[3] 試験室はよく確立されているが、共同試験は行っていない分析法を使用する予定である。
前者と同じ妥当性確認の範囲が要求される。
[4] 分析法が科学文献に公表され、分析特性が記述されている。
試験室は、精度、かたより(マトリックスによる変動を含む)、堅牢性および検量線の直線性を検討すべきである。
[5] 分析法は科学文献に公表されているが、分析特性の記述がない。または、分析法は、試験室(in house)で開発された。
試験室は、精度、かたより(マトリックスによる変動を含む)、堅牢性および検量線の直線性を検討すべきである。
[6] 分析法が経験的なものである。
経験的な方法というのは、推定量が単に定まった手順に従って見いだした結果であるものである。これは、試料中の特定の分析種の濃度のような分析法に依存する量を査定することを意図した測定とは異なり、分析法のかたよりは慣習的にゼロであり、マトリックス変動は(定義されたクラス内で)重要ではない。試験室のかたよりは無視することはできないが、単一試験室の試験では推定することはおそらく難しい。さらに、標準物質は入手できそうにない。共同試験のデータがない場合は、室間再現性の推定は、特別に考案された堅牢性の試験によって得られるか、Horwitz 式を使用して推定できる。
[7] 分析がその場限りである。
その場限りの分析が、時折、大きな出費をしないで、批評性が低くても、値の大体の範囲を確定するために必要である。従って、妥当性確認に向かう努力はかなり限定される。かたよりが回収率の推定や分析種の添加のような方法で、また、反復によって精度が検討されるべきである。
[8] 要員及び器具を変更する。
重要な例は、主要な機器の変更、非常に変動しやすい試薬の新しいバッチ(例えば、ポリクロナール抗体)、試験室の家屋になされた変更、新しい要因によって始めて使用される方法、長期間使われなかった後に、採用された妥当性確認された方法を含む。ここで、必須の行動は、有害な変化は起こっていないことを示すことである。最低限のチェックは1回のかたよりテストである。典型的な試験材料あるいは管理試料の「変更前後」実験である。一般的に、行われたテストは、分析手順の変更の起こりうる影響を反映すべきである。
b)‐2‐2 推奨事項
次のような推奨が単一試験室による分析法の妥当性確認の使用に関してなされる。
- 可能かつ実用的なところでは、国際的なプロトコルに従って実施された共同試験によって評価された性能特性をもつ分析法を使用すべきである。
- そのような方法がない場合には、分析法を顧客に分析値を出すために用いる前に、in‐house で妥当性確認をしなければならない。
- 単一試験室による妥当性確認においては、評価のための適切な特性(適用性、選択性、校正、精確さ、精度、濃度範囲、定量限界、検出限界、感度、堅牢性)を選択することが要求される。試験室は、どの特性が測定されるかを選ぶときに、顧客の要求を考慮に入れなければならない。
- 査定された特性の証拠は、要求された場合には、顧客に入手可能にしなければならない。
c)今後の対応
開発された方法については、その開発の程度に応じて、プロトコルによるもの、複数の試験室によるもの、あるいは単一試験室によるものを選択して、なんらかの妥当性確認を行う必要がある。コンプライアンス(法令遵守)に係わる分析法は、室間再現性が高いことが必要であり、室間再現性のない方法は使用できないので、室間共同試験を行って、妥当性を確認することが必要である。分析法の開発者は、その方法がどこでも使えるように分析手順書を整備し、最低限複数の試験室による共同試験を計画・実施して方法の確立を図ることが望まれる。
2.機能性成分の分析例
a)イソフラボン
a)‐1 イソフラボンの種類と分布
イソフラボンは、大豆やクズに含有される機能性成分であり、女性ホルモン作用を有することからファイトエストロジェンとも呼ばれ、骨密度の低下を予防する成分として、特定保健用食品の関与成分として認定されている。
日本人にとって主要なイソフラボン供給源である大豆には、アグリコンであるダイゼイン、ゲニステインおよびグリシテインとそれらの配糖体が12種類含有されている。これらは、主に大豆の杯芽(杯軸)に多く含有されており、種皮には存在しないことが分かっている。表1‐5に大豆および大豆加工食品中の大豆イソフラボン含有量(mg/100g)を示した。
表1‐5.大豆および大豆加工食品中の大豆イソフラボン含有量
| 食品名 | 検体数 | 含有量 | 平均含有量 |
|---|---|---|---|
| 大豆 | 11 | 88、3〜207.7 | 140.4 |
| 煮大豆 | 3 | 69.0〜74.07 | 72.1 |
| きな粉 | 2 | 211.1〜321.4 | 266.2 |
| 豆腐 | 4 | 17.1〜24.3 | 20.3 |
| 油揚げ | 3 | 23.8〜53.4 | 39.2 |
| 納豆 | 2 | 65.6〜81.3 | 73.5 |
| みそ | 8 | 12.8〜81.4 | 49.7 |
| しょうゆ | 8 | 1.0〜1.7 | 0.9 |
| 豆乳 | 3 | 7.6〜59.4 | 24.8 |
(厚生労働省ホームページより)
a)‐2 イソフラボンの分析
[試料の調製]
大豆およびきな粉、豆腐、豆乳、湯葉、みそ、しょうゆ、納豆、油揚げなどの大豆加工品を試料として用いる。水分を含む試料については、凍結乾燥後0.5〜1.0gを計りとり、70%エタノールあるいは80%メタノール50mlを加えて室温下でホモジナイザーで十分摩砕後、ろ紙でろ過し、残さを再度50mlのアルコール水溶液で攪拌抽出、ろ過を行い、得られた2回分のろ液をあわせて、ロータリーエバポレータで2〜3mlに濃縮し、70%エタノールあるいは80%メタノールに溶解し、10mlの全量フラスコに移して定容する。これを0.45μmのメンブレンフィルターでろ過し、測定用試料溶液とする。水分の多い試料を凍結乾燥せずにそのまま用いる場合は、50mlのメタノールあるいはエタノールを10gの試料に加え、同様の操作を行い、測定用試料溶液を調製する。
[イソフラボン標準溶液の作成]
1.ダイジン、2.ダイゼイン、3.グリシチン、4.グリシテイン、5.ゲニスチン、6.ゲニステイン、7.、8.、9.各アグリコンの6”‐O‐マロニル体、10.、11.、12.各アグリコンの6”‐O‐アセチル体を100 mg計りとり、メタノール100mlに溶解する。これを100μg/mlとなるようにメタノールで希釈してHPLC分析に供する。
[分析操作]
通常のHPLC用ODSカラムを用い、異動相としてA液:0.1%酢酸含有15%アセトニトリル、B液:0.1%酢酸含有35%アセトニトリル溶液を作製し、A液からスタートして50分間でアセトニトリル濃度が15%から30%まで増加するグラジエント法により溶出する。注入する測定用試料溶液あるいは標準溶液は10μl、流量は1.0ml/min、カラム温度は25℃、検出波長はUV260nmを用いる。
以上によって得られたHPLCのピーク面積から検量線の作成ならびに各試料のイソフラボン含量を算出する。
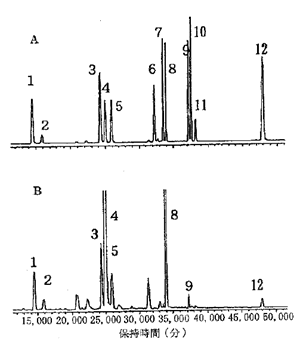
図2.大豆イソフラボン類のHPLCによる分析例
A:標準物質、B:大豆
1:ダイジン、2:グリシチン、3:ゲニスチン、4:6”‐O‐マロニルダイジン、5:6”‐O‐マロニルグリシチン、6:6”‐O‐アセチルダイジン、7:6”‐O‐アセチルグリシチン、8:6”‐O‐マロニルゲニスチン、9:ダイゼイン、10:6”‐O‐アセチルゲニスチン、11:グリシテイン、12:ゲニステイン
(扇谷ら:札幌市衛生研年報29、83(2002))
b)フラボノール
b)‐1 フラボノールの種類と構造
b)‐1‐1 フラボノールのアグリコンの種類
天然に存在するフラボノールの多くは、その基本骨格であるアグリコンに糖が結合した配糖体として存在するが、その概要を理解することを目的としてアグリコンについて述べる。図3に天然に存在する主なフラボノールアグリコンの構造を示した。これらのうち、ガランギンとケンフェロール、ケルセチン、ミリセチンの4種はフラボン骨格のA環の5位と7位の炭素に水酸基が存在する基本的な構造を持つ成分であり、ガランギン以外は分布範囲が広いことなどからフラボノールの主要な成分となっている。
この他、ケルセチンのB環の水酸基がメチル化されたイソラムネチンとタマリキセチンも野菜等に含有されるフラボノールとして重要であるが、特にケルセチンが動物の体内に吸収された後、これらの成分に代謝変換されることから、生体との関係で注目される成分である。
一方、これらの標準的構造を持つ成分とはA環の水酸基の結合状況の異なるアグリコンについて図4に示した。このうち、モリンやフィゼチンは樹木から調製されたフラボノールとしてなじみ深い成分であり、モリンは、強い黄色を示す色素であることから食品添加物として利用されている。スピナセチンとパツレチンはホウレンソウに存在する主要なフラボノールである。
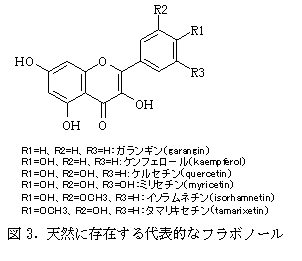
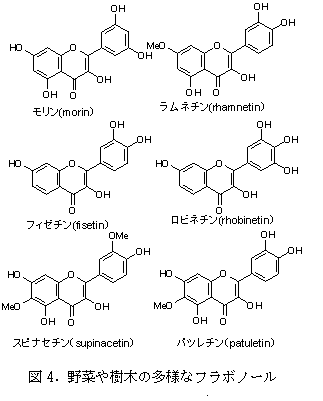
b)‐1‐2 フラボノール配糖体について
タマネギの褐色外果皮あるいはハーブ類の天日乾燥物のように組織が乾燥過程を経る素材や樹木の幹や根には、アグリコンが優先的に存在するものの、これら以外の多くの生鮮農産物では、フラボノール配糖体として存在するのが普通である。上記アグリコンに結合する糖としては、グルコースが最も頻度が高く、次いでガラクトースやラムノース、アラビノース、キシロースなどが知られている。これらのほとんどはアグリコンの水酸基部位で炭素骨格とβ結合によって繋がっている。また、ルチノシドのように2量体の糖が結合した配糖体も多く、多種多様な成分が存在する。
これら配糖体のうち著名なものについては慣用名がつけられている。例えば、フラボノールの代表格であるケルセチンの3‐ルチノシドはルチン、3‐グルコシドはイソケルシトリン、3‐ラムノシドはケルシトリン、3‐ガラクトシドはハイペリン4'‐グルコシドはスピラエオシドと呼ばれているが、慣用名を持つ化合物は全体のほんのわずかに過ぎない。
b)‐2 フラボノールの農産物・食品における分布と含有量
フラボノールを始めとするフラボノイドの農産物の含有量を検索するためには、わが国において作成された「機能性食品因子データベース」(http://www.nihn.go.jp/FFF/)や米国農務省(USDA)の「フラボノイドデータベース(Flavonoid data base)」
(http://www.nal.usda.gov/fnic/foodcomp/Data/Flav/Flav02‐1.pdf)が利用できる。
フラボノールは、フラバノン(柑橘に多い)やフラボンに比べてその分布範囲は極めて広いが、特にフラボノールを多く含有する農産物・食品について例示すると表1‐6のようになる。
表1‐6.フラボノールを高度に含有する食材(USDA)
| 食材名 | フラボノール(含量(mg/100g)) |
|---|---|
| ソバ ニラ クレソン フェンネル タマネギ(赤) タマネギ(黄色) 唐辛子 ディル サツマイモ葉 |
ケルセチン(23.05) ケンフェロール(10)、ケルセチン(4.77)、イソラムネチン(6.75) ケンフェロール(13.0)、イソラムネチン(1.0) ケンフェロール(6.5)、ケルセチン(48.8)、ミリセチン(19.8) ケルセチン(19.93) ケルセチン(13.27) ケルセチン(16.80) ケンフェロール(13.33)、ケルセチン(55.15) ケルセチン(20.54)、ミリセチン(9.74) |
b)‐3 フラボノールの分析
b)‐3‐1 フラボノール配糖体の分析に関する前処理
[試料の調製]
野菜や果実などにおいて分析をしようとする部位(皮や可食部など)を切り分けた後に、適宜裁断・混合し、一定量を採取・秤量してすぐに抽出用試料として用いることも可能である。しかし、この方法では収穫後の試料の鮮度低下が生じ、保存に伴い水分含量が変動する場合もあることを充分考慮した測定値の活用を図る必要がある。この方法で得られたデータは、生鮮物重量あたりのフラボノール含量として表示することになる。
野菜や果実本来の特性を正しく評価することを目的として、最近最も良く用いられる方法は、凍結乾燥物を調製し、それを分析用試料として用いる方法である。果実や野菜を適宜裁断した後に液体窒素を加えて凍結し、そのまま凍結乾燥器で乾燥し、凍結乾燥物を粉末にした後、‐80 ℃に保存すれば、必要な時にいつでも分析が可能になる。
[試料液の調製方法]
野菜や果実など農産物からのフラボノールの抽出は、メタノールやエタノールのアルコール水溶液を試料に5倍量程度加え、ホモジナイザーで摩砕し、遠心分離によって上澄液を回収する方法により行われる。この方法では、1回の操作では回収率が不十分であるため、遠心分離残さに抽出溶媒を加えてホモジナイザーによる摩砕抽出を再度行い、2回目の上澄液を回収し、得られた上澄液を合わせて一定量に定容する方法が一般的である。この際、抽出時の加温操作や超音波処理は抽出率を上げるために極めて有効であり、最近は超音波処理が多用されるようになった。なお、アルコール濃度の範囲は40%から90%が用いられ、40%以下ではポリフェノール酸化酵素が失活せずに作用するため、抽出率が低下するといわれている。この他、アセトンや酢酸エチルも用いられるが、組織の膨潤化が進まないことなどにより抽出率は劣る。ただし、フラボノールを始めとするフラボノイドの抽出は、抽出しようとする化合物の溶媒溶解特性や農産物・食品のマトリックスの影響を強く受けるといわれており、最良の抽出法については個別の試料について精査する必要がある。例えば、著しい違いのある例としてブドウ種子のプロアントシアニンの場合は、モノマーとダイマーがクロロホルムで良く抽出され、トリマー(3量体)はアセトンで、それ以上の重合体はメタノールで良く抽出されるといわれている。
b)‐3‐2 フラボノールの分離・分析方法
フラボノールの定量を目的とし分析方法には、ODS(Octadecyl silane)カラムを用いた高速液体クロマトグラフィー(HPLC)が多用されている。高速液体クロマトグラフの一般的な仕様として、グラジエント溶出用ポンプ、オートサンプラー、UV検出器、カラムオーブンが必要である。今回、分析例にとりあげるタマネギのように複数の配糖体が存在する場合は、HPLCのカラム溶出液の有機溶媒濃度を時間とともに上昇させる方法(グラジエント溶出)が用いられるが、分析対象が単純である場合はカラム溶出液を一定にした分析も可能である。グラジエント溶出の際は、常時用いるA液と疎水性を高めるための有機溶媒B液が用いられ、A液としては10mmol/lリン酸溶液、0.1%リン酸溶液、2%酢酸溶液、0.1%ギ酸溶液などの使用例がある。一方B液としては主としてメタノールが多用されており、フラボノールの特性に合わせアセトニトリルが使用される場合もある。なお、フラボノールは250nm付近と360nm付近に極大吸収が認められるが、一般的には360nmを検出波長とする場合が多い。ただし、他のポリフェノールと同時測定を行う場合は、ベンゼン環に由来する共通の吸収波長である280nmを検出波長として選定することが多い。カラム温度は35℃や40℃が使用される。
b)‐3‐3 タマネギのフラボノール配糖体を例とした分析法
[試料液の調製]
タマネギを縦に4等分し、その1つを包丁で1cm程度に細断して混合する。その混合物を約10g採取・秤量して200mlのビーカに移し、100mlの80%メタノールを添加し、ヒスコトロンを用いて摩砕し、フラボノールを抽出する。この摩砕物を遠心分離して上澄液を200mlの全量フラスコに移し、残さに80mlの80%メタノールを加えて再びヒスコトロンで摩砕抽出を行い、遠心分離によって得られた上澄液を200mlの全量フラスコに注ぐ。次いで200mlの全量フラスコの不足分を80%メタノールで補い定容とする。この溶液を試料溶液として用いる。
[HPLCの条件]
HPLCにODS‐C18(粒径5μm)カラム(25cm×5mm)を取り付け、2%酢酸を含有する25%メタノール溶液を流しカラムを平衡化する。次に0.45μmのフィルターでろ過した試料溶液10μLをHPLCに注入し、平衡化に用いた溶液を初発溶液とし、そのメタノール濃度を40分間に80%まで上昇させる濃度勾配溶出で分析を行う。カラムの温度は40℃、ポンプの流量は1.0ml/min、検出波長は360nmとする。
[HPLCのクロマトグラム]
図5に上記条件で分析して得られたクロマトグラムを示した。検出されたピークを溶出順にそれぞれHP‐1からHP‐7として示した。これらのピークは別途分離精製後、NMRなどを用いた構造解析により以下のような構造であることが分かった。
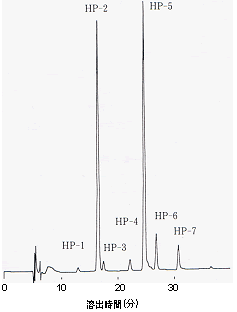
HP‐1:ケルセチン7、4'‐O‐β‐ジグルコシド
HP‐2:ケルセチン3、4'‐O‐β‐ジグルコシド
HP‐3:ケルセチン7‐O‐β‐グルコシド
HP‐4:ケルセチン3‐O‐β‐ジグルコシド
HP‐5:ケルセチン4'‐O‐β‐グルコシド
HP‐6:イソラムネチン4'‐O‐β‐グルコシド
HP‐7:ケルセチン
図5. タマネギのフラボノール配糖体のHPLCクロマトグラム
これらの結果から、フラボノール骨格の7位に糖が結合した配糖体の溶出が早く、次いで3位、4'位となっていることが分かった。
b)‐3‐4 フラボノールアグリコンの分析
[配糖体からのアグリコンの調製]
A. 酸やアルカリによる加水分解
フラボノイド配糖体の酸加水分解には、硫酸よりも塩酸の方が優れているといわれている。一般的には、試料溶液中の塩酸の最終濃度を1.2 mol/lに調整し、90 ℃で2時間加水分解する方法が用いられる。塩酸を1 mol/lの濃度に調整し85 ℃で30分加水分解する方法もブロッコリーなどで用いられている。この際フラボノイドの酸化が生じることから、BHTやアスコルビン酸(2 mg/ml)などを添加すると回収率が向上する。加水分解によって生じたフラボノイドアグリコンは、酢酸エチルに転溶するか、あるいは加水分解が終了した溶液にメタノールを加えて溶解を完全に行いHPLC等を用いて定量する。
一方、アルコール性抽出液に同量の4 mol/l‐NaOHを加え最終濃度を2 mol/lに調整し、窒素ガスで封入したバイアル中で16時間室温にて加水分解を行い、塩酸で中和し定量する方法も用いられている。
B. 酵素による加水分解
フラボノールを始めとするフラボノイドに結合する糖は、グルコース、ガラクトース、ラムノース、アラビノース、キシロースなど様々である。そのため、これらの糖を全て一種類の酵素で加水分解するための手法が検討されている。これまでにペクチナーゼやセルラーゼを用いた加水分解試験が行われ、ベルガモット果皮のフラボノイドでは酵素単独では70%から80%、両者を組み合わせた方向では90%以上の回収率が得られている。
一方、配糖体がタマネギのケルセチン配糖体のようにβ‐グルコシドの場合は、被験液に200 mmol/lの酢酸緩衝液(pH5.0)を加えてpHを調整し、最終的にアーモンドのβ‐グルコシダーゼを1 mg/mlの濃度になるよう添加することによって良好な加水分解が行われる。
[アグリコンのHPLCによる分析]
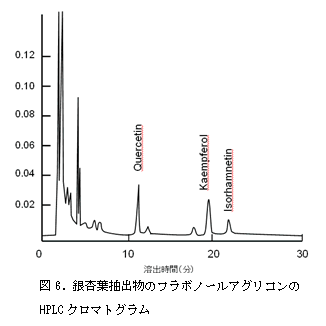
フラボノールアグリコンの分析としては、HPLCにODSカラムを取り付け、0.1%あるいは0.5%リン酸とメタノールの50:50(V/V)溶液を移動相とするアイソクラティック溶出が用いられている。銀杏葉抽出物のアグリコンを分析した例を図6に示した。フラボノールの主要なアグリコン3種については、ケルセチン、ケンフェロール、イソラムネチンの順に溶出される。これら3種のフラボノールの標準物質は市販されているので、既知濃度の標準溶液を作製し、同じ条件で分析を実施し試料溶液のアグリコン濃度を算出する。
c)フラボン
c)‐1 フラボンの種類と構造
c)‐1‐1 フラボンのアグリコンの種類
天然に存在するフラボンの多くは、フラボノールと同様にその基本骨格であるアグリコンに糖が結合した配糖体として存在している。図7に天然に存在する主なフラボンのアグリコンの構造を示した。これらクリシンとアピゲニン、ルテオリン、ジオスメチン、トリセチンの5種はフラボン骨格のA環の5位と7位の炭素に水酸基が存在する基本的な構造を持つ成分である。この他、文献等に比較的良く取り上げられるアグリコンを図8に示した。このうち、ノビレチンとタンジェレチンはポリメトキシフラボンとしてグループ化される柑橘果実の特徴的なフラボンアグリコンである。これらは、特に沖縄の在来柑橘であるシークワーサーに豊富に含有される機能性成分として注目され、研究が活発に行われている。
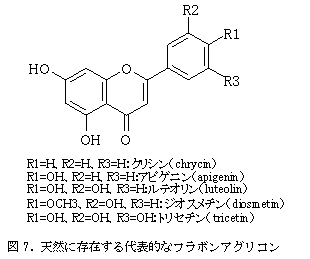
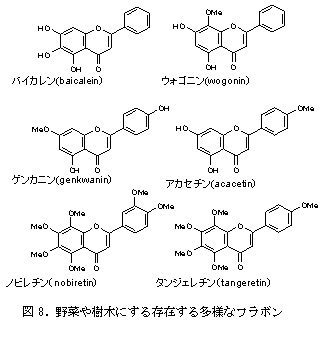
c)‐1‐2 フラボン配糖体について
フラボン配糖体を含有する農産物・食品としては、セリ科野菜をその代表としてあげることができる。セリ科のミツバやパセリにはフラボンのアピゲニンとルテオリンが高度に含有されており、ヒトに対するフラボンの供給源として重要な役割を果たしている。
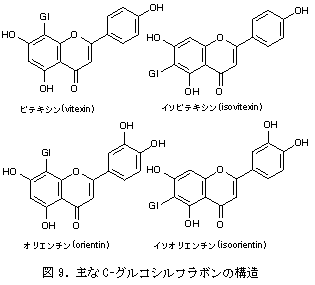
フラボンには、フラボン骨格の炭素に糖の炭素が直接結合したC‐グルコシルフラボンが存在しており、その代表的な成分の構造を図9に示した。
c)‐2 フラボノールの農産物における分布と含有量
フラボンは、セリ科植物に主要なフラボノイドとして含有される特徴を持っている。また、ハーブ類における含有量も多い。一方、その他の野菜類では唐辛子や、ピーマン、春菊に存在する。米国の農務省のデータベースから比較的フラボンを多く含有する農産物を例示すると表1‐7のようになる。
表1‐7.フラボンを高度に含有する農産物(USDA)
| 食材名 | フラボン含量(mg/100g) |
|---|---|
| セレリアック セロリ(緑) セロリ コールラビ オレガノ パセリ 唐辛子 ローズマリー タイム |
アピゲニン(2.41) アピゲニン(19.0)、ルテオリン(3.5) アピゲニン(4.61)、ルテオリン(1.31) ルテオリン(1.30) アピゲニン(3.0)、ルテオリン(1.5) アピゲニン(302.0)、ルテオリン(1.24)) ルテオリン(5.11) ルテオリン(4.0) アピゲニン(5.0)、ルテオリン(51.0) |
c)‐3 フラボンの分析
c)‐3‐1 フラボン配糖体の分析に関する前処理
フラボンの配糖体を分析するための方法は、b) フラボノールに準じて行う。
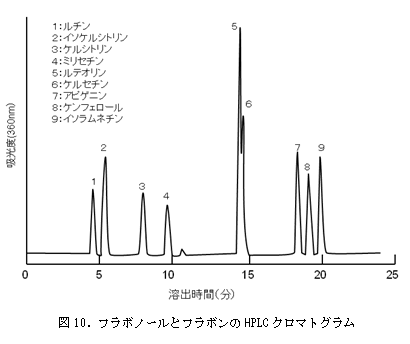
フラボンとフラボノールのHPLCによる溶出位置は、ほとんど変わらないためにフラボノイドの分析においては、それらを区別することなく目的とする素材のフラボノイド組成を考慮してHPLCの条件を設定する必要がある。図10は、主要なフラボンであるアピゲニンとルテオリン並びに主要なフラボノールであるケンフェロールとケルセチン、ミリセチン、イソラムネチンをHPLCで同時に分析した場合のクロマトグラムを示したものである。溶出条件は、150 mm×4.6 mm(4μm ODS:C18 Genesis)カラムを用い、TFAでpH2.5に調整したアセトニトリル溶液のアセトニトリル濃度を20分間で20%から40%に直線的に増加させる方法である。流速は1.0 ml/min、検出波長は365 nmである。これから分かるように、ルテオリンとケルセチンの溶出位置が重なっており、その分離が問題になる。
C‐グルコシルフラボンについても、HPLCによる分析条件は同様にODSカラムを用いて行われている。具体的には1%酢酸溶液(A溶液)とメタノール(B溶液)を用い、15%メタノール溶液からスタートし、30分間でメタノール濃度を30%に直線的に上昇させる溶出法が用いられている。
c)‐3‐2 フラボン配糖体の分析例
[試料液調製の概要]
セロリを細片とした後に液体窒素を注いで凍結し、凍結乾燥機で乾燥後に粉砕し、その一部を採取・計量して試料として用いる。残りは‐80℃で保存し、適宜使用する。試料50mgに60%(V/V)のメタノール溶液5mlを加え、室温にて超音波を照射し抽出する。試料懸濁液を遠心分離して得られた上澄液を0.45μmのフィルターでろ過し、HPLC用試料溶液とする。
[HPLCの条件]
HPLCにODS‐C18(粒径5μm)カラム(25cm×5mm)を取り付け、0.1%ギ酸溶液(A液)と0.1%ギ酸を含むアセトニトリル(B液)を用いて、アセトニトリルの濃度を直線的に上昇させる方法によりフラボン配糖体を分析する。具体的には、10%の濃度でB液を流してカラムを平衡化した後、40分間で26%までB液の濃度を上昇させ、次いで70分までに65%までB液の濃度を上昇させる方法によって分析する。カラムの温度は25℃、ポンプの流量は1.0ml/min、検出波長は350nmである。
[HPLCのクロマトグラム]
図11にLinらによるセロリのフラボン配糖体の分析結果を示した。彼らは、室温でセロリを乾燥しているが、マロニル基の離脱や配糖体の加水分解がほとんど生じていない。この研究により、セロリには、アピインの他にルテオリン7‐O‐マロニルアピオシルグルコシドなど多くのマロニル体が存在していることが明らかになっている。
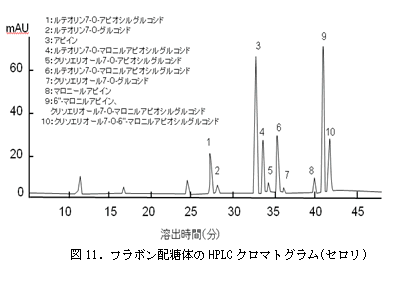
c)‐3‐3 フラボンアグリコンの分析
フラボン配糖体からアグリコンを調製する方法は、フラボノールと同様である。
[動物生体試料中のフラボンの分析]
動物実験によって得られた血漿あるいは臓器ホモジネートに2倍量の0.1mol/l酢酸含有アセトンを加えて撹拌し、タンパク質などの高分子を沈殿させる。遠心分離(13,000×g、10分、4℃)によって得られた上澄液に添加したアセトンの1/2容量の水を加え、再度遠心分離を行い、0.45μmのフィルターでろ過してHPLCに注入分析することにより分析が可能である。
3.機能性成分の分析法における問題点
機能性成分の評価法は、多くの研究者が様々な方法を開発して、評価に使用してきたが、相対評価の段階に留まっており、方法の室間再現性を検討するまでには至っていない。そのために、論文や報告間での比較が出来ないのが、現状である。表示に用いるためには、室間再現性が確保される必要があり、ようやくそれを評価する論文の発表や活動が行われるようになってきている。島村らは、「酸化防止剤力価評価のための各種抗酸化活性測定法の共同試験」を行っている。抗酸化活性評価の代表的なものとして、ラジカル消去活性を分光学的に測定する1、1‐diphenyl‐2‐picrylhydrazyl(DPPH)法、2、2’‐azinobis(3‐ethylbenzo thizoline‐6‐sulphonic acid)(ABTS)法、活性酸素種消去活性の評価法として、スーパーオキシドアニオンラジカル消去活性を分光学的に測定する2‐(4‐iodophenyl)‐3‐ (4‐nitrophenyl)‐5‐(2、4‐disulfophenyl)‐2H‐tetrazolium、 monosodium salt(WST‐1)法を、公定法の候補として選び、9種類の酸化防止剤(カテキン、ケルセチン、セサモール、フェルラ酸、没食子酸、モリン、エラグ酸、D‐α‐トコフェロール、D‐δ‐トコフェロール)の抗酸化性について、3試験室による共同試験を行なった。DPPH法ではTrolox等価活性の室間再現性精度はD‐α‐トコフェロールを除いた8種類の酸化防止剤について20%以下であった。ABTS法では、Trolox等価活性の室間再現精度は、カテキン、ケルセチン、フェルラ酸を除いた6種類の酸化防止剤について20%以下であった。WST‐1法では、トコフェロール類を除いた7種類の酸化防止剤を評価したが、いずれも室間再現精度は、20%以上となった。DPPH法とABTS法の公定法化の可能性が示唆されている。しかし、ここでは、酸化防止剤そのものの評価であり、マトリックスをもつ実際試料での検討はこれからである。
また、Oxygen Radical Absorbance Capacity (ORAC:活性酸素吸収能力)法について、妥当性確認のための共同試験が行われている。(+)‐カテキン、Trolox、フェルラ酸、ヘスペレチン、コーヒー酸について、11試験室が参加した。溶液試料と粉末試料を用いてTrolox等量(μmolTE)で評価を行っている。溶液試料では、各10.0 mg/L 濃度を評価し、室間再現精度は(+)‐カテキンとヘスペレチンは20%を大きく超えた。粉末試料は、各試験室で1 g/L の溶液を調製し、評価したが、室間再現精度は、17〜33%と比較的高い数値を示している。ここでも評価の対象は純物質であり、マトリックスをもつ実際試料での検討はこれからである。
変動の要因として、マイクロプレートリーダーを用いる測定法では、ウェル間の変動、プレート間の変動があり、これらの低減を図ることが重要である。
また、化学分析における室間再現精度の評価には、HorRat が用いられるが、物質濃度で評価する方法であるため、抗酸化活性は、そのままでは適用できない。特定の物質への換算が可能であれば適用でき、ORAC法 ではTrolox等量を用いているが、例えば、(+)‐カテキンは、Troloxそのものの10倍以上の活性を持つため、どのように換算するかの検討が必要である。
4 食品の機能性に関する将来の課題
1)機能性食品への将来的ニーズ
近年、少子高齢化が一層進むなかで、医療費の削減を考慮しながら、人びとの健康寿命を延伸するため、また、生活習慣病の予防を目的として、運動や食事を中心とした生活習慣の改善が一層重要な課題となってきており、平成20年4月からは、40歳以上を対象に、特定健診・保健指導が始まったところである。こうした状況のなかで、ビタミン・ミネラルなどの栄養素及び機能性成分等を含む機能性食品に対する国民のニーズが一層高まることが予想される。
2)従来の栄養成分表になじまない機能性に対する将来的対応
機能性成分としてのフラボノイドやイソフラボン、プロアントシアニジン、カロテノイドについては、米国のUSDAがいち早くホームページに公開しているが、従来の栄養成分表に収載するまでにはなっていない。フランスでも、フラボノイドについてのデータベースの作製を行っているとのことで、各国とも栄養成分に次いで非栄養素である機能性成分のデータベースの構築を急いでいるが、それらは、知名度が高く分析可能な機能性成分に属するものであり、栄養成分表の別表として補完的な役割を果たすものとして期待されている。
一方、膨大な数の他の機能性成分については、科学的な視点からその重要性に焦点を当て、以下の考えかたに基づき計画的な取り組みを行うことが重要であると考えられる。
1.マイナー成分のデータベース化への取り組み
- 従来の栄養成分表の資料データとして、現状では知名度が低く収載になじまない機能性成分(マイナー成分)に関する分析法が多様であるため、最適な分析法の決定とその妥当性の確認を行う必要がある。
- 妥当性を確認した分析法の普及に努める。
- 日本全土における代表的な産地におけるマイナー成分の分析値の経年変動データ等の蓄積などの業務を実施することにより、次期の取り組みが必要な成分として位置づけるべきマイナーな機能性成分が明らかになるものと考えられる。
2.機能性評価法の標準化と表示に向けた活動
各種食品やその成分の抗酸化性について、評価法の標準化を図り、その方法によって測定した値を食品に表示する取り組みが世界的に期待されるようになっている。米国ではすでに、277品目の野菜・果実のORAC法によって測定した抗酸化性機能に関するデータ(ORAC値)をホームページで公表している。また、米国の民間企業の一部では、果実ジュースにORAC値を表示して販売しており、韓国でも同様の取り組みが開始された。 我が国でも民間企業のグループから同様の要望があり、ORAC法を我が国の抗酸化性評価法の標準法として選定し、それを普及させ、将来的に食品表示につなげたいとする活動も行われている。
3)分析方法の課題
機能性成分の評価は、抗酸化活性のように「活性」として評価されている。前述したように「表示」に関わってくると、方法の妥当性確認が必要となってくるが、純物質を用いても室間共同試験による再現精度は、よくない。マトリックスを持つ実際試料では、さらに抽出操作が入るため、再現精度はより大きくなることが予想される。
大きな変動要因と考えられるマイクロプレートリーダーのウェル、プレートによる変動の低減法が、必要であろう。
また、活性そのものでは、共同試験の再現精度を評価する基準がないので、あらたに構築する必要がある。例えば、PCRを用いるGMOの定量分析法の室間再現精度の判断基準は、25%である。
なお、日本食品標準成分表の掲載成分の考え方は、活性ではなくて、物質量として掲載する方向で、これまでは、ビタミンは国際単位での表示があったが、物質量のみの記載になっている(一部、当量による記載がある)。また、摂取基準などの基準がある場合に、掲載する方向である。機能性成分の掲載についての検討は、まだ行われておらず、今後の課題と考えられる。
1.特定保健用食品、栄養機能食品について
1)特定保健用食品
1980年代後半、市場には食品の機能性を期待させる「いわゆる健康食品」が出回り、なかには食品による健康被害を報告されるようになった。このような状況のなか、1991年、厚生省は、国民が安心して食生活の状況に応じた選択ができるよう、機能性を表示する食品の類型化として、特別用途食品のなかに、特定保健用食品を創設した。特定保健用食品は、「食生活において特定の保健の目的で摂取する者に対し、その摂取により当該保健の目的が期待できる旨の表示をする食品」と健康増進法において定められている。特定保健用食品は、食品の保健の用途に関して個別に評価するもので、申請には、ヒトにおける有効性と安全性が確認されていること、適切な摂取量が医学的、栄養学的に設定されていること、機能性成分(関与成分)が定量的に把握できること等が必要である。2001年と2005年に制度の改正が行われた(後述)。現在表示が許可されている保健の効果を表1‐8に示した。平成21年3月現在で847品目が許可されている
表1‐8.現在許可されている特定保健用食品の保健の効果と関与成分
(平成20年7月現在 783品目)
| 保健の用途の表示内容 | 代表的な関与成分 | 許可件数 (件) |
既許可783 品目に対する 割合(%) |
|---|---|---|---|
| お腹の調子を整える、便通改善等 | 各種オリゴ糖、ラクチュロース、ビフィズス菌、各種乳酸菌、食物繊維(難消化性デキストリン、ポリデキストロース、グアーガム、サイリウム種皮等) | 298 | 38.0 |
| 血糖値関係 | 難消化性デキストリン、小麦アルブミン、グアバ葉ポリフェノール、アラビノース等 | 107 | 13.7 |
| 血圧関係 | ラクトトリペプチド、カゼインドデカペプチド、杜仲葉配糖体(ゲニポシド酸)、サーデンペプチド等 | 98 | 12.5 |
| コレステロール関係 | キトサン、大豆たんぱく質、低分子化アルギン酸ナトリウム | 93 | 11.9 |
| 歯関係 | パラチノース、マルチトース、エリスリトール等 | 61 | 7.8 |
| コレステロール&お腹の調子、コレステロール&脂肪関係等 | 低分子化アルギン酸ナトリウム、サイリウム種皮の食物繊維等 | 32 | 4.1 |
| 骨関係 | 大豆イソフラボン、乳塩基性タンパク質、ビタミンK2 | 30 | 3.8 |
| 脂肪関係 | ジアシルグリセロール、グロビン蛋白分解物等 | 50 | 6.4 |
| ミネラルの吸収関係 | クエン酸リンゴ酸カルシウム、カゼインホスホペプチド、ヘム鉄、フラクトオリゴ糖等 | 6 | 0.8 |
| 疾病リスク低減 | カルシウム葉酸 | 5 | 0.6 |
| ミネラル&お腹の調子 | フラクトオリゴ糖 | 3 | 0.4 |
2)保健機能食品制度の創設
1998年、食薬区分の見直しが行われ、それまで医薬品であったビタミンやミネラル、及びハーブ等が食品成分として認められることとなり、これを受けて、2001年、厚生労働省は、保健機能食品制度を創設し、ある一定の規格基準を定めて許可する「栄養機能食品」と表示する内容によって個別に評価する「特定保健用食品」とを合わせて、「保健機能食品」とした。特定保健用食品は、明らかな食品の形態をしていることが重要な許可要件であったが、制度の改正に伴い、食品の形態は錠剤型やカプセル剤型も許可されることとなった。なお、これらの食品は、食品衛生法の他、健康増進法によって規定されることとなった(図12)。
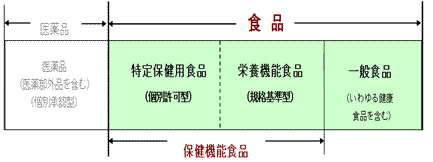
図12.保健機能食品制度
栄養機能食品は、「身体の健全な成長、発達、健康の維持に必要な栄養成分(ビタミン、ミネラル等)の補給・補完に資する食品であり、食生活において特定の栄養成分の補給を主たる目的として摂取をする者に対して表示をするもの」と定義されている。現在、栄養機能食品の栄養成分として規格基準が設定されているのは、日本人の食事摂取基準(2005年版)において値が設定された26項目のビタミンのうち、12種類のビタミンと5種類のミネラルである。各々について、上限値と下限値が設定されており、1日当たりの用量がこの範囲に設定されていれば、厚生労働省の許可を受けることなく栄養機能食品の表示ができる。その他のビタミン、ミネラル、アミノ酸、ハーブについては、科学的根拠に基づき可能なものから順次規格基準と検討することとされた。表1‐9に栄養機能食品の栄養成分と許可表示を示した。
表1‐9.栄養機能食品の栄養成分と栄養機能表示
| 栄養成分 | 栄養機能表示 |
|---|---|
| 亜鉛 | 亜鉛は、味覚を正常に保つのに必要な栄養素です。 亜鉛は、皮膚や粘膜の健康維持を助ける栄養素です。 亜鉛は、たんぱく質・核酸の代謝に関与して、健康の維持に役立つ栄養素です。 |
| カルシウム | カルシウムは、骨や歯の形成に必要な栄養素です。 |
| 鉄 | 鉄は、赤血球を作るのに必要な栄養素です。 |
| 銅 | 銅は、赤血球の形成を助ける栄養素です。 銅は、多くの体内酵素の正常な働きと骨の形成を助ける栄養素です。 |
| マグネシウム | マグネシウムは、骨の形成や歯の形成に必要な栄養素です。 マグネシウムは、多くの体内酵素の正常な働きとエネルギー産生を助けるとともに、血液循環を正常に保つのに必要な栄養素です。 |
| ナイアシン | ナイアシンは、皮膚や粘膜の健康維持を助ける栄養素です。 |
| パントテン酸 | パントテン酸は、皮膚や粘膜の健康維持を助ける栄養素です。 |
| ビオチン | ビオチンは、皮膚や粘膜の健康維持を助ける栄養素です。 |
| ビタミンA注) | ビタミンAは、夜間の視力の維持を助ける栄養素です。 ビタミンAは、皮膚や粘膜の健康維持を助ける栄養素です。 |
| ビタミンB1 | ビタミンB1は、炭水化物からのエネルギー産生と皮膚や粘膜の健康維持を助ける栄養素です。 |
| ビタミンB2 | ビタミンB2は、皮膚や粘膜の健康維持を助ける栄養素です。 |
| ビタミンB6 | ビタミンB6は、たんぱく質からのエネルギーの産生と皮膚や粘膜の健康維持を助ける栄養素です。 |
| ビタミンB12 | ビタミンB12は、赤血球の形成を助ける栄養素です。 |
| ビタミンC | ビタミンCは、皮膚や粘膜の健康維持を助けるとともに、抗酸化作用を持つ栄養素です。 |
| ビタミンD | ビタミンDは、腸管のカルシウムの吸収を促進し、骨の形成を助ける栄養素です。 |
| ビタミンE | ビタミンEは、抗酸化作用により、体内の脂質を酸化から守り、細胞の健康維持を助ける栄養素です。 |
| 葉酸 | 葉酸は、赤血球の形成を助ける栄養素です。葉酸は、胎児の正常な発育に寄与する栄養素です。 |
注)ビタミンAの前駆体であるβ‐カロテンについては、ビタミンA源の栄養機能食品として認める。この場合、「妊娠3ヶ月以内又は妊娠を希望する女性は過剰摂取にならないように注意してください。」旨の注意喚起表示は、不要とする。
3)特定保健用食品制度の改正
2005年、特定保健用食品制度が改正され、条件付き特定保健用食品の導入、規格基準型特定保健用食品の創設、疾病リスク低減表示の容認が施行されることとなった。条件付き特定保健用食品は、科学的根拠が確立されていないが、一定の有効性が確認される食品である。規格基準型特定保健用食品は、特保としての許可実績が十分である等、科学的根拠が蓄積されており、事務局審査が可能な食品について規格基準を定め、審議会の個別審査なく許可する食品である。疾病リスク低減表示は、関与成分の疾病リスク低減効果が医学的・栄養学的に確立されている場合、特保の許可において表示を認めるもので、「カルシウムと骨粗鬆症」「葉酸と胎児の神経管閉鎖障害」についてリスク低減表示が許可されている。
表1‐10.特定保健用食品の区分別許可数(平成20年11月7日現在)
| 品目数 | (%) | |
|---|---|---|
| 特定保健用食品(再許可等253品目を含む) | 781 | 96.9 |
| 規格基準型特定保健用食品 | 18 | 2.3 |
| 条件付き特定保健用食品 | 1 | 0.1 |
| 疾病リスク低減表示特定保健用食品 | 6 | 0.7 |
| 合計 | 806 | 100 |
2.疫学的な調査研究に食品データベースが活用された事例
1)各国における機能性物質摂取量と循環器疾患発症との関連における栄養疫学研究の動向
栄養素摂取量と循環器疾患(脳卒中・心筋梗塞)の発症・死亡との関連を検討するための疫学研究(ここではコホート研究に限定されている)の方法に関する系統的レビューにおいて、どのような栄養素が研究の対象とされているかに関する集計が行われている。1993〜2001年に掲載された論文を対象としているため、情報がやや古くなるが、対象栄養素別に研究数をまとめると表1‐11のようになっている。なお、これらの研究論文は医学系論文のデータベースであるPubMedから系統的に抽出された1,361論文からそれぞれの内容を吟味して抽出された論文を検討対象としている。
表1-11 栄養素摂取量等と循環器疾患との関連を検討するために計画されたコホート研究で検討対象とされた栄養素のまとめ(1993〜2001年に学術雑誌に掲載された論文を対象)
| 栄養素群 | 栄養素等の詳細 | 研究数(かっこ内は日本)、% | |
|---|---|---|---|
| 心筋梗塞 | 脳卒中 | ||
| マクロ栄養素 | 総脂質、各種脂肪酸、コレステロール、たんぱく質、これらを豊富に含む食品・食品群 | 26(0)32% | 5(0)19% |
| 食物繊維 | 食物繊維、食物繊維を豊富に含む食品・食品群 | 8(0)10% | 1(0)4% |
| ミネラル類 | ミネラル類、ミネラル類を豊富に含む食品・食品群 | 8(0)10% | 6(0)23% |
| 抗酸化栄養素類※、ホモシステイン関連栄養素、 | 抗酸化栄養素類、ホモシステイン関連栄養素、これらを豊富に含む食品・食品群 | 28(0)35% | 14(0)54% |
| その他の食品 | --- | 4(0)5% | 0(0)0% |
| Glycemic index | Glycemic index, glycemic load | 2(0)2% | 0(0)0% |
| 食パターン | --- | 5(0)6% | 0(0)0% |
| 合計 | --- | 81(0) | 26(0) |
※ビタミンE(各種トコフェロールを含む)、ビタミンA(カロテノイド類を含む)、フラボノイド類、フラボン類、カテキン類。
参考文献1)を参考にして作成した。
心筋梗塞、脳卒中それぞれ81、26の研究が存在し、そのうち、心筋梗塞では35%の28研究で、脳卒中では54%の14研究で、抗酸化栄養素類、ホモシステイン関連栄養素を対象栄養素としていた。これらの研究はすべてコホート研究であることから、そのベースライン調査が行われ、対象者の栄養素等摂取量が推定されたのは、研究完了時の数年から十数年前であり、さらに、研究完了からデータの整理ならびに解析、論文の投稿から受理に要する合計時間が通常数年間に及ぶことを考えると、抗酸化栄養素への関心がかなり早い時期に高まっていたことと、この種の研究を行うために必須である日本食品標準成分表の開発作業がすでにかなり早期に進められていたことがわかる。
2) 機能性物質摂取量と生活習慣病リスクとの関連(ポリフェノール類)
1.目的と方法
ここでは、ポリフェノール類に焦点を当て、ポリフェノール類摂取量と生活習慣病との関連を疫学研究の手法によって検討した研究論文を収集し、現時点における結果を示すことにする。なお、質的量的に利用可能な日本食品標準成分表が存在していることがこの種の研究の必要条件であることを考えると、わが国からの報告は存在せず、すべての報告が欧米諸国からのものである。そのため、ここで示す結果(ポリフェノール類摂取量と生活習慣病との関連)をそのまま日本人に適用して、疾病予防に用いることには問題が残されていることは明らかである。しかしながら、ここでは、この種の研究がどの国で先進的に行われ、どの種類のポリフェノール類に焦点が当てられているのか、そして、その結果はどのようになっているのかを知ることを目的として以下に記すことにする。
ポリフェノール類はその構造式により細かく分類されるが、ここでは、フラボノイド、フラボン、カテキンの3種類についてそれぞれと生活習慣病との関連を整理する。また、疫学の研究手法はさまざまであるが、ここでは、長期間の生活習慣が疾病の発症やそれによる死亡に与える影響を観察しやすい研究手法であるコホート研究による結果に限った。なお、生活習慣病との関連が示唆されるポリフェノールにリグナンがあるが、リグナンは摂取量の把握が困難であるため、今回の検討から除外した。また、イソフラボンは摂取量が日本人を含む東アジア人と欧米人とのあいだで大きく異なるため、欧米での研究結果は日本人には参考にしにくいと考え、この集計からは除外した。なお、類似の目的で世界中の研究成果をArtsらがまとめ、2005年に発表した論文に最近の知見を加えてまとめた。
2.循環器疾患
フラボノイド摂取量と循環器疾患(冠動脈性疾患と脳卒中)との関連を検討したコホート研究のまとめを表1‐12に示す。
表1-12 フラボノイド摂取量と循環器疾患(冠動脈性疾患と脳卒中)との関連を検討したコホート研究のまとめ
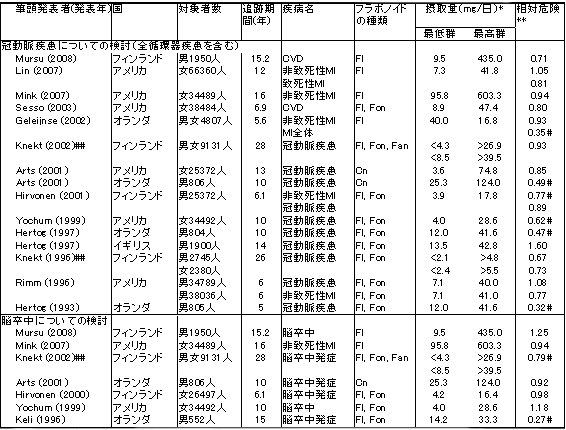
略号: Fl=フラボノール、Fon=フラボン、Fan=フラバン、Cn=カテキン、CVD=全循環器疾患、MI=心筋梗塞。
※数値は平均値、中央値、郡を区切るための値のいずれか。
※※低摂取群に対する高摂取群のリスク
#有意な増加または減少を示した場合。
##摂取量は上段が男性、下段が女性。
参考文献2)から改変、引用。
ここでいうところの冠動脈性疾患は心筋梗塞とほぼ同義である。冠動脈性疾患については、15の報告があり、サブ解析も含めると合計で20の結果が示されており、そのうち、7つの解析で有意なリスクの低下が観察されている。逆に有意なリスクの上昇を観察した結果はなかった。脳卒中については、7つの報告があり、そのうち、2つの解析で有意なリスクの低下が観察されている。有意なリスクの上昇を観察した結果はなかった。多くの研究の結果が有意ではなかったものの、リスクの低下を報告していることから推測されるように、これらのデータを数量的に統合したメタ解析によると、相対リスクは0.80であり、有意なリスク低下であったと報告している。
以上より、フラボノイドの積極的な摂取が冠動脈性疾患(心筋梗塞)への予防効果を有する可能性は高いものと思われる。一方、脳卒中についての結果はあまり安定しておらず、また、研究数も少ないため、結論を下すのは困難だと思われる。
しかしながら、ポリフェノールの中のどの物質が特に強い予防効果を有するのかに答えるには、研究数がまだ乏しく、今後の研究成果が待たれるところである。
3.癌
フラボノイド摂取量と癌の発症との関連を検討したコホート研究のまとめを表1‐13に示す。36の研究報告があり、サブ解析を別に数えると、40の報告があった。その中で、部位を問わない全癌については6つの報告があり、癌発症とのあいだに有意な関連を示した報告はなかった。
部位別に検討した報告は、サブ解析も含めると全部で36あったが、有意な関連(リスクの減少)が観察されたのはわずかに3つであった。そのうち、2つが肺癌で残りの1つは直腸であった。部位別に観察結果では、肺癌だけが、すべての報告において(有意でないものの)、リスクの低下が認められた。肺癌以外の癌については、特に予防効果が認められた部位はないようであった。
肺癌については、大規模な症例対照研究の結果が報告されており、フラボノイドの総摂取量は肺癌リスクと有意な関連を認めなかったものの、フラボノイドを詳細に分類し、さらに喫煙習慣別に解析すると、喫煙者群でのみ、カテキン、ケルセチン、ケンフェロールで予防効果が認められた。この種の詳細な解析を行った報告はまだ乏しいため、結論を急いではいけないが、喫煙者と非喫煙者でフラボノイドの効果が異なる可能性を示したこと、また、フラボノイドの詳細分類によって結果が異なる可能性を示唆した点は興味深い。
表1-13 フラボノイド摂取量と癌の発症との関連を検討したコホート研究のまとめ
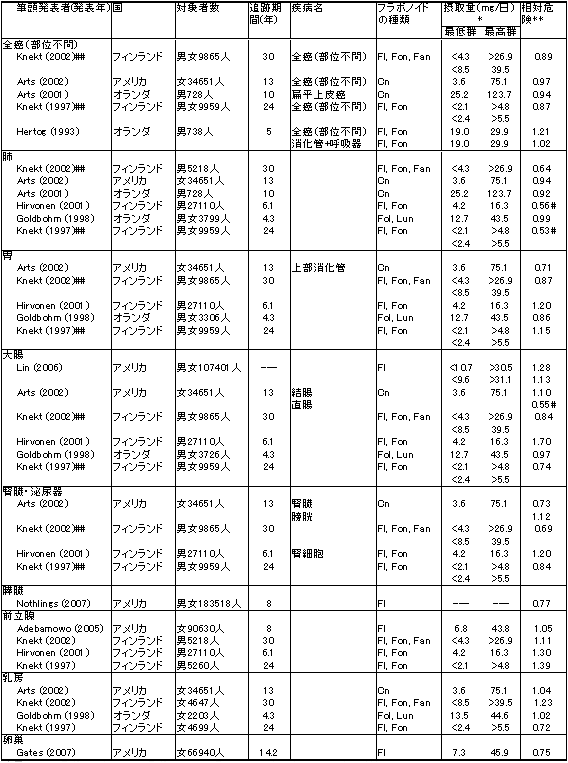
略号: Fl=フラボノール、Fon=フラボン、Fan=フラバン、Cn=カテキン、Lun=ルテオリン。
※数値は平均値、中央値、郡を区切るための値のいずれか。
※※低摂取群に対する高摂取群のリスク
#有意な増加または減少を示した場合。
##摂取量は上段が男性、下段が女性。
参考文献2)から改変、引用。
4.結果を解釈する上での問題点
表1‐12および表1‐13が示すように、研究間で摂取量の分布が大きく異なっている。そのため、それぞれの結果を単純に比較することはできないであろう。現在の日本人がポリフェノール摂取量を増やした場合、減らした場合に、それぞれの疾患の発症がどのように増減するかを知りたいわけであって、その目的のためには、現在の日本人のポリフェノール摂取量に近い集団から得られた結果を特に尊重したいところである。ところが、現在の日本人のポリフェノール摂取量の分布に関する信頼できる報告は乏しく、その詳細は未知である。
たとえば、フィンランド人2007人のポリフェノール摂取量を調べた研究によると、平均摂取量は男女合計で863 mg/日であり、そのうちの63%がコーヒーに、12%が穀類に、9%が紅茶に由来しており、果物は6%に過ぎず、野菜にいたってはわずか2%でしかなかった。ポリフェノールに含まれる物質の健康効果は必ずしも同じでないと考えられるため、ここで行ったような重量を用いた単純な食品摂取源の比較は必ずしも正しくないかもしれないが、この結果は、表1‐12ならびに表1‐13の結果を見ても、どの食品を食べればよいかについての情報を直接に与えてくれるものではないことを示している。ところで、日本人のポリフェノール摂取量を調べた報告では、平均摂取量は17 mg/日となっている。ここではイソフラボンが別に集計されており、それを含めると67 mg/日となるが、それでも、フィンランドの報告に比べると著しく低い。アメリカ人の平均摂取量は190 mg/日、オーストラリア人は454 mg/日との報告があり、日本人の摂取量はこれらすべてよりも著しく低い。問題は、日本人の摂取量は世界の中で著しく低いのだという解釈だけでなく、ポリフェノール含有量に関する日本食品標準成分表の開発が日本で遅れており、そのために実際よりも極端に過小に評価されてしまったのだという解釈もなりたつことである。
このような状態では、たとえ、ポリフェノールまたは、その中の一部の物質に生活習慣病を予防する可能性が示されたとしても、日本人において、その摂取量を増やしたときの効果を見積もることができず、実際の予防対策に用いることは困難であろう。
5.まとめ
『ポリフェノールで生活習慣病は予防できるか』に科学的に回答するためには、世界各国の研究成果を集めるだけでは十分でないばかりでなく、その前に、日本人におけるポリフェノール摂取量の実態を詳細に調べることから始めねばならない。このような基礎研究なくして、ポリフェノールの健康効果を、人間のレベルで、そして、より実際的にはわれわれ日本人の食生活への適用というレベルで議論しようとするのは困難であろう。
3)機能性物質摂取量と生活習慣病リスクとの関連(イソフラボン)
1.目的と方法
次に、比較的に研究数が多いと考えられるイソフラボンに焦点を当て、食品からのイソフラボン摂取量と生活習慣病、特に女性乳癌と男性前立腺癌との関連を疫学研究の手法によって検討した研究論文を収集し、現時点における結果を示すことにした。この目的には、最近報告された2つのメタ・アナリシスが参考になると考えられたため、それらの結果を中心にまとめることにした。
2.女性乳癌
イソフラボン摂取量のほとんどがダイズに由来し、ダイズ摂取量はアジア諸国で特異的に高いため、アジア諸国でアジア人種を対象として、イソフラボン摂取量と女性乳癌の発症リスクとの関連を検討した8つの疫学研究(1つのコホート研究及び7つの症例・対照研究、日本人を対象としたものは2つ)をまとめたメタ・アナリシスを参考にした。8つの研究の結果を数量的にまとめたオッズ比は、低摂取群に比べて、中摂取群でも0.88倍、高摂取群では0.71倍となっていて、ともに有意なリスク低下を示している(図13)。一方、集団としてのイソフラボン摂取量が低い欧米諸国で行われた11の研究を同じようにまとめた結果によると、高摂取群(0.8mg/日前後)と低摂取群(0.15mg/日以下)の乳癌発症リスクに有意な差は認められていない。
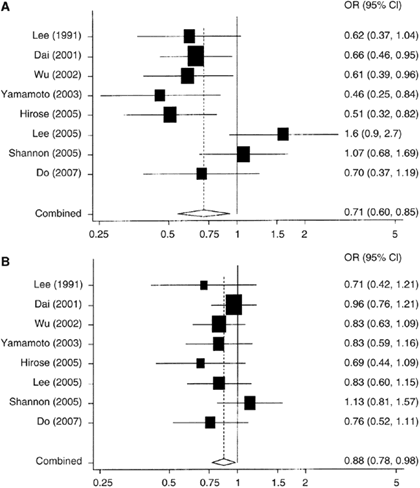
図13 アジア諸国でアジア人種を対象として、イソフラボン摂取量と女性乳癌の発症リスクとの関連を検討した8つの疫学研究(1つのコホート研究及び7つの症例・対照研究)をまとめたメタ・アナリシス
(A)高摂取群(20 mg/日以上)に比べた低摂取群(5 mg/日以下)の乳癌発症リスク。
(B)中摂取群(10 mg/日前後)に比べた低摂取群(5 mg/日以下)の乳癌発症リスク。低摂取群に比べて、中摂取群でも0.88倍(95%信頼区間:0.60〜0.85)、高摂取群では0.71倍(95%信頼区間:0.78〜0.98)のリスクとなっていて、ともに有意なリスク低下を示している。
3.男性前立腺癌
イソフラボン摂取量と男性前立腺癌発症リスクとの関連を検討した8つの疫学研究(コホート研究、症例対照研究)のメタ・アナリシスが存在するため、この報告を参考にした。検討対象にされた8つの研究のうち、2つが日本人を対象とした研究であった(表1‐14)。
表1-14 イソフラボン摂取量と男性前立腺癌発症リスクとの関連を検討した8つの疫学研究(コホート研究、症例対照研究)
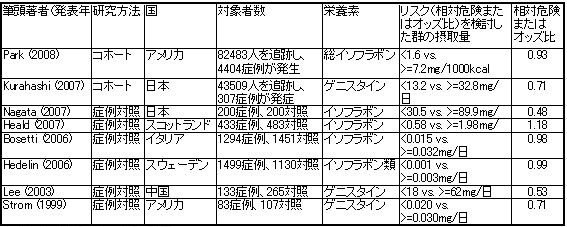
参考文献3)から改変のうえ、引用。
数量的に統合された相対危険またはオッズは、0.76(95%信頼区間:0.76〜1.02)であり、予防可能性を示したが、有意ではなかった(図14)。また、欧米諸国で行われた研究とわが国及び中国で行われた研究のあいだには摂取量に極めて大きなちがいがあるため、これらをひとつにまとめて評価することは困難であると考えられた。
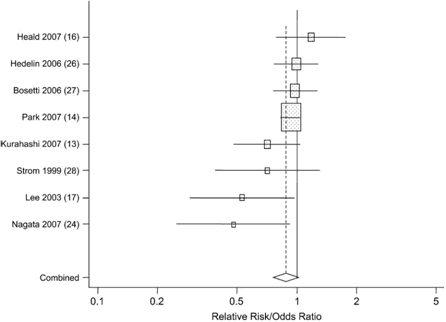
図14 イソフラボン摂取量と男性前立腺癌発症リスクとの関連を検討した8つの疫学研究(コホート研究、症例対照研究)のメタ・アナリシスの結果
数量的に統合された相対危険またはオッズは、0.76(95%信頼区間:0.76〜1.02)。
4.まとめ
イソフラボン摂取量のほとんどがダイズに由来するために、習慣的なイソフラボン摂取量の推定は、ダイズ製品のイソフラボン含有量に関する成分表とダイズ製品の習慣的摂取量を把握できるような食事調査法の存在によって可能となる。特に、前者、つまり、イソフラボン摂取量のほとんどがダイズ製品という比較的に少ない食品種に限られていることは、食品成分データベースの確立が比較的に容易なことを示している。そのため、食品中のイソフラボン含有量を決定し、イソフラボン摂取と健康との関連を検討するための基礎資料を作成しようという試みが他の機能性物質に先駆けて行われた。そのため、両者の関連に関する知見も、他の機能性物質よりも集積されている。
4)まとめ
以上、ポリフェノール類とイソフラボンについて、摂取量と生活習慣病リスクとの関連について、現在における研究成果を簡単にまとめた。ポリフェノール類はその種類が多く、種類別に検討すると、質的にも量的にも研究の集積も十分でなく、まだ一定の関連は得られていないようである。一方、イソフラボンはアジア人のようにイソフラボンを大量摂取している集団においては、その中でも摂取量が多い人たちで、女性乳癌や男性前立腺癌のリスクが少ない傾向が認められた。しかし、イソフラボンについてもまだ結論を下せるほどには十分な研究数は確保されておらず、結論は今後の研究成果を待たねばならない。
しかしながら、今回の検討でもっとも強調すべき点は、摂取量と生活習慣病リスクとの関連の有無ではないように思われる。むしろ、「これらを明らかにするためには、機能性データベースの存在が不可欠である」という事実のほうがはるかに重要であろう。つまり、「機能性物質の積極的な摂取が生活習慣病の予防につながるか否かを検討したうえで機能性データベースの一項目として含めるか否かを検討する」のではなく、「機能性物質の積極的な摂取が生活習慣病の予防につながるか否かという科学的な情報が必要であると判断する場合には、機能性データベースが存在していなければならない」ということである。
ポリフェノール類とイソフラボンを含む、いわゆる機能性物質の積極的な摂取が生活習慣病の予防につながるか否かは、疫学研究(栄養疫学研究)からはまだ結論を下すことはできないと思われる。そして、少なくとも、わが国においては、その一因は、機能性物質に関する機能性成分データベースの確立が他の先進諸国に比べて遅れていることにあると考えられる。
参考文献
1) 佐々木敏. 循環器疾患予防のための栄養素・非栄養素成分に関する疫学研究の最近の動向:系統的レビュー.日循予防誌 2003; 38: 105‐17.
2) 佐々木敏. ポリフェノールで生活習慣病は予防できるか?〜疫学研究からの知見〜 食生活 2008; 102: 26‐31.
3) Yan L,Spitznagel EL. Soy consumption and prostate cancer risk in men: a revisit of a meta‐analysis. Am J Clin Nutr 2009; 89: 1155‐63.
4) 荒井綜一 機能性食品の事典 荒井綜一、安部啓子、金沢和樹、吉川敏一、渡邊昌編集 朝倉書店 2007
5) 渡邊昌 栄養学原論 南光堂 2008
6) 厚生労働省ホームページ
http://www.mhlw.go.jp/topics/bukyoku/iyaku/syoku‐anzen/hokenkinou/hyouziseido‐3.html
7) 奥 恒行、中村禎子 特定保健用食品の許可内容と現状、ならびに制度の変遷 日本食物繊維学会誌 12:51‐58、2008
8) Sasaki S, Kobayashi M,Tsugane S. Development of substituted fatty acid food composition table for the use in nutritional epidemiologic studies for Japanese populations: its methodological backgrounds and the evaluation J Epidemiol 1999; 9: 190‐207.
9) Wakai K,Egami I, Kato K, et al. Dietary intake and sources of isoflavones among Japanese. Nutr Cancer 1999; 33: 139‐45.
10) Arai Y,Watanabe S,Kimira M,et al. Dietary intakes of flavonols flavones and isoflavones by Japanese women and the inverse correlation between quercetin intake and plasma LDL cholesterol concentration. J Nutr 2000; 130: 2243‐50.
11) Arts ICW, Hollman PCH. Polyphenols and disease risk in epidemiologic studies. Am J Clin Nutr 2005; 81(suppl): 317S‐25S.
12) Huxley RR, Neil HAW. The relation between dietary flavonol intake and coronary heart disease mortality: a meta‐analysis of prospective cohort studies. Eur J Clin Nutr 2003; 57: 904‐8.
13) Cui Y, Morgenstern H, Greenland S,et al. Dietary flavonoid intake and lung cancer‐‐a population‐based case‐control study. Cancer 2008; 112: 2241‐8.
14) Ovaskainen ML,Torronen R,Koponen JM,et al. Dietary intake and major food sources of polyphenols in Finnish adults. J Nutr 2008; 138: 562‐66.
15) Chun OK,Chung SJ,Song WO. Estimated dietary flavonoid intake and major food sources of U.S. adults. J Nutr 2007; 137: 1244‐52.
16) Johannot L,Somerset SM. Age‐related variations in flavonoid intake and sources in the Australian population. Public Health Nutr 2006; 9: 1045‐54.
17)Wu AH,Yu MC,Tseng CC,Pike MC. Epidemiology of soy exposures and breast cancer risk. Br J Nutr 2008; 98: 9‐14.
18) Horwitz,W: Protocol for the design,conduct and interpretation of method‐performance studies,Pure & Appl.Chem. ,67(2), 331‐343(1995).
19) AOACInt:Appendix D: Guidelines for collaborative study procedures to validate characteristics of a method of analysis. In Official methods of analysis of AOAC Int. 18th ed.Gaithersburg,MD,USA.(2005).
20) Horwitz, W. ,Kamps,L.R. and Boyer,K.W.:Quality Assurance in the Analysis of Foods for Trace Constituents,J.Assoc.Off.Anal.Chem. ,63(6), 1344‐1354(1980).
21) Thompson,M.: Recent trends in inter‐laboratory precision at ppb and sub‐ppb concentrations in relation to fitness for purpose criteria in proficiency testing, Analyst, 125, 385‐386(2000).
22) Thompson, M. ,Ellison, S.L.R. ,and Wood,R.: Harmonized guidelines for single‐laboratory validation of methods of analysis,Pure & Appl.Chem. ,74(5) ,835‐855(2002).
23) Horwitz,W: Protocol for the design,conduct and interpretation of method‐performance studies,Pure & Appl.Chem. ,67(2), 331‐343(1995).
24) AOACInt:Appendix D: Guidelines for collaborative study procedures to validate characteristics of a method of analysis. In Official methods of analysis of AOAC Int. 18th ed.Gaithersburg,MD,USA.(2005).
25) Horwitz, W. , Kamps,L.R. and Boyer, K.W.:Quality Assurance in the Analysis of Foods for Trace Constituents,J.Assoc.Off.Anal.Chem. , 63(6) ,1344‐1354(1980).
26) Thompson,M.: Recent trends in inter‐laboratory precision at ppb and sub‐ppb concentrations in relation to fitness for purpose criteria in proficiency testing, Analyst, 125, 385‐386(2000).
27) Thompson,M.,Ellison,S.L.R. ,and Wood,R.: Harmonized guidelines for single‐laboratory validation of methods of analysis, Pure & Appl.Chem. ,74(5) ,835‐855(2002).
28) 島村智子ら:日本食品科学工学会誌、54(11)、 482‐487(2007).
29) 渡辺純ら:内部資料
3.アンケート調査及び文献調査の結果
1)栄養士会へのアンケート調査結果
現在の日本食品標準成分表は一般基礎成分、ビタミン類、ミネラル類を中心に収載されているが、機能性成分についても収載の要望があるのか、アンケートを実施することにより調査した。アンケートは日本食品標準成分表を利用する機会の多い各都道府県の栄養士会に協力を要請した。実施したアンケートについて、様式‐1に示した。
アンケートの結果は、62〜71ページにまとめた。回答は25都府県からあり、有効回答数は184であった。
質問1より約6割の人が、日本食品標準成分表に機能性成分の収載を希望していることが判明した。希望する意見について、質問・問い合わせへの対応、情報提供、栄養指導、その他の各意見に分類した。
質問・問い合わせへの対応に関する意見ついては、実際に住民と接する機会が多い栄養士の方の回答が目立った。機能性成分がマスコミ等で紹介され、それを聞いた一般消費者が最寄りの栄養士へ尋ねていることがわかる。情報提供に関する意見及び栄養指導に関する意見と合わせて、機能性成分に関する情報が一方通行になっており、栄養士自身が自信を持って問い合わせに回答、情報提供、栄養指導が出来るよう、何らかの根拠のあるものを求めているものと推測される。その一つが日本食品標準成分表への収載かと思うが、一方で日本食品標準成分表への収載への反対意見もあった。機能性成分については適切なエビデンスが確立されていないものが多く、それらについて心配する意見があった。また、現状の日本食品標準成分表への肯定意見も多く、機能性成分が収載されることによって、日本食品標準成分表が使いづらくなることへの懸念もある。賛成側の意見の中でも別冊にすることへの要望があることから、機能性成分を収載する場合は別冊にすることも視野に入れる必要があると思われる。
いずれにしろ、国民はマスコミ等の影響を受け易い環境下にあるため、機能性成分については誤解を招かないように、正確なエビデンスのもとに収載する必要があると思われる。また、機能性成分の分析法については公定法が非常に少なく、現状では分析法によって異なる結果が得られることも想定される。したがって、正しいエビデンスと分析法が揃って、初めて収載が可能になるとも言える。
様式‐1
調査1.日本食品標準成分表へ機能性成分の含有量を収載することに関しての調査
お願い
日本食品標準成分表をより良い成分表にするための調査です。
日本食品標準成分表に機能性成分(栄養・嗜好面よりも、生体調節機能が期待される成分)の含有量を収載することに関して質問します。下記に回答くださいますようお願いいたします。なお、回答欄が不足する場合は、別紙に記載下さるか、この用紙のファイルをFDに入れましたので、記載欄を拡大し入力し印字くださっても結構です。お手数をおかけしますが、よろしくお願いいたします。
・・・・・・・・・・・・・・・・・・・回答用紙・・・・・・・・・・・・・・・
都道府県名:
協議会名:
回答者名(問い合わせ先):
回答年月日:2008年 月 日
質問1.
日本食品標準成分表に機能性成分(栄養・嗜好面よりも、生体調節機能が期待される成分)の含有量を収載することを希望するかどうか、またその理由を記載ください。
1.収載希望の有無について、該当するものに、○をつけてください。
希望する 希望しない
2.収載希望の有無を決めた理由を記載ください
理由:
質問2.質問1‐1.で「収載を希望する」と回答した方は次の質問にお答えください。
1. 具体的に収載を希望する物質名を挙げてください。(複数回答も可です。)
2. その成分が日本食品標準成分表に収載された場合、どのような利用方法が想定されますか。あるいは、現場ではどのような場面で利用すると思われますか。記載ください。
質問3. その他ご意見があればお書きください。
質問1.
日本食品標準成分表に機能性成分(栄養・嗜好面よりも、生体調節機能が期待される成分)の含有量を収載することを希望するかどうか、またその理由を記載ください。
<回答の内訳>
希望する 111人
希望しない 66人
記載なし 3人
判別不能 3人
どちらとも言えない 1人
希望する
得られた回答について以下に示す4種に区分した。各意見の末尾【 】内にに各栄養士会(学校健康教育栄養士協議会、行政栄養士協議会、研究教育栄養士協議会、集団健康管理栄養士協議会、地域活動栄養士協議会、病院栄養士協議会及び福祉栄養士協議会)の所属を記載した(アンケート用紙に記載の無かったものは、記載無し)。
1.質問・問い合わせへの対応に関する意見
2.情報提供に関する意見
3.栄養指導に関する意見
4.その他の意見
1.質問・問い合わせへの対応に関する意見
- 最近、機能性成分についての関心が高まり、食品の機能性成分の質問が以前より多くなっている。【地域活動】
- 機能性成分が記載されている食品が多く出回ってきたので、それについての質問が多くなることが予想され、日本食品標準成分表に記載があると参考になると思ったため。【行政】
- 住民から聞かれることがある。【行政】
- 大豆イソフラボンに関する問い合わせが多いため。【行政】
- 問い合わせがあった場合、対応できる。【行政】
- 住民から問い合わせがある。ただ、どの程度摂取したら良いかわからない中で、掲載すると、混乱が生じるおそれがある。【行政】
- ポリフェノールなど、住民から質問される場合があるので、具体的数値として把握できているといいと思う。【行政】
- 患者から、情報(機能)についてニーズが多い。【病院】
- 機能性成分に興味を示し問い合わせがあるため。【福祉】
- アレルギーについての問い合わせが多いため。【集団健康管理】
- 住民、食品業者等から問い合わせがあるため。【行政】
- 生体調整機能が期待されている成分について、聞かれることがあるので。【福祉】
- 患者様から尋ねられた時、すぐに答えられると良いと思う。また、マスコミで言われていることの確認などを専門職として理解していきたい。【病院】
- 機能性食品使用者の質問に対し、きちんとしたデータに基づいた回答ができる。【地域活動】
- 栄養指導の対象者に質問される事があるので。【集団健康管理】
- より良い給食の提供に役立つと考えるため。
- 栄養相談の際に必要だと思うので。
- サプリメントや健康食品を利用する人が増えており、その物質への質問が増えることも予想されるため、保健指導の際に分かると説明しやすいと思う。【行政】
- 栄養相談などで質問を受けることが多くなったため。【地域活動】
- 栄養相談の時に、質問を受けることがある。【地域活動】
- 患者から質問を受ける可能性があるから。
- 世の中全体の流れというかサプリメント類も沢山の物が出回っていて、じゃあ実際に普通に食べている物には、そういった物(機能性成分)は入っていないのか?という話になった時に、答えようが(調べようが)ないので。【福祉】
- 窓口相談の際、尋ねられるので。【行政】
- 相談の対象者に尋ねられることがあるため。
- トクホ等患者様からその成果や効能について聞かれるため、含有量が収載されていると調べられる。【病院】
- 栄養情報の氾濫で質問されることがあるため。【病院】
2.情報提供に関する意見
- 食品(商品)に、多種類の成分を含有している旨表示されるようになったため。【行政】
- 栄養機能食品や特定保健用食品764品目の保健機能食品も出回っており、日常食べることも多くなっていると思うので、機能性成分や特定の保健の用途食品の収載はあったほうが良い。【行政】
- 食品の機能性成分についての情報が宣伝や広告などにも多く表示されているが、正しい情報が少ない。【地域活動】
- 信頼できる情報提供の必要性がある。【地域活動】
- 病気の予防に効果が高いものなら、記載してもらいたいと思う。【行政】
- 現在、よく目にする、耳にする物質というか成分があればいいなと感じているからである。また情報があふれている中、信用のおける書物に記載することも必要だと思う。【学校健康教育】
- 今は食品中に含まれる機能性成分の研究が進み、様々な成分が判明し、その有効性が、一般の方々にも知られるようになってきた。日本食品標準成分表をより効果的に使用するため、機能性成分を収載した方が毎日の食事、健康づくりに役立つと考える。【学校健康教育】
- 機能性成分として、健康維持や病気予防に役立つ成分が食物中に存在することが近年明らかになってきたので、その含有量を収載した方が参考になる。【地域活動】
- われわれは、食品の成分含有量によりその食品の栄養価値をランク付けする傾向にある。しかし、季節、産地、調理法など、諸々の条件で含有量および吸収量が変化するゆえに、過信に注意し、大よその目安として使用することで良いのでは、と認識している。機能性成分は、その食品そのものが健康管理上、功を成す性質(成分)を持ち備えているものと思われる。食品の特性を知ると共に効率の良い使用により、成分量(紙面の上での含有量)にとらわれることなく、健康になるための食べ方よりも、食を楽しみながら食べることが肩の凝らない健康管理に繋がるように理解している私としては、自然体の食品、食材の性質、特質など、生産が複雑化されている現代こそ、食品の持つ特性を知り、役立てるべきと思っている。【地域活動】
- 現在含有量が不明であるため。【病院】
- 新しい情報を知る方法として、必要。【集団健康管理】
- メディアでの情報が氾濫しているため。【病院】
- 身体にとって有益だという説得力があると思われる。【福祉】
- がん、遺伝子、老化にかかわる栄養素の話題が多くなってきたため。【研究教育】
- 特定保健用食品が増えていて、国民の関心が高まっているので、収載を希望した。
- 食事提供の際、エンドユーザーへの情報提供に有効活用できる可能性があるから。【集団健康管理】
- 国民の健康に関する関心が非常に高まっているが、食品については科学的根拠のある情報を得ることが少ないので、日本食品標準成分表への収載を希望する。【病院】
- TVなどの情報の普及により、栄養相談の担当者から「?」と思うような質問が寄せられる。確かな情報根拠として日本食品標準成分表がそばにあるととても良いと思う。【福祉】
- 食品の三次機能が注目を浴び、多くの健康食品が流通している。機能性成分の収載も必要となってくるのではないか。ただし、「栄養成分」が基本であり、それに加えて一円にまとめるのは難しいのではないか。脂肪酸組成表やアミノ酸組成表のように別冊で良いので、機能性成分表を作れば良いと思う。【研究教育】
- 社会的な健康志向(一次予防や健康寿命の延伸、特定検診・保健指導など)により、機能性成分を含む食品が注目されている今、機能性成分を含有する食品やその含有量を知ること、機能性成分を含有しているという点から食品を選択できる能力を身につけることが必要だと考えるから。【研究教育】
- 機能性の効果が認められたものについては、周知されるのが良いと考えたから。【研究教育】
- サプリメントの普及の増加により成分の過剰や相乗効果などの確認のためにも。【研究教育】
- 話題に出たりするが、数値のことは知らないので。【学校健康教育】
- 日本食品標準成分表は専門職のみにあらず一般の方が利用するものである。よって、知りたい情報を掲載すると良いと考える。【集団健康管理】
- 機能性食品が当たり前のように出回っており、機能性成分が自分で簡単に算出できればメーカーの広告に惑わされることも減るだろうから。【行政】
- 機能性成分として、健康維持や病気予防に役立つ成分が食物中に存在することが近年明らかになってきたので、その含有量を収載した方が参考になる。【地域活動】
- 近年は生理活性成分について研究が進んでいるし、予防医学の観点からでも、食品から栄養素以外の生体調節機能成分は非常に有効と考える。また、種々のサプリメントや健康食品の是非を考えるためにも参考になると思う。【地域活動】
- アレルギーを抑制し免疫力をつける、体力回復、老化抑制など健康維持・健康増進を図るため、エビデンスのレベルデータの質・信頼度の高い総合的に評価されたものを知る。【地域活動】。
- ガン予防や老化防止などに機能性成分の働きが、近年よく言われている。どの食品にどの位含まれているかを知りたい。【病院】
- 機能性成分に関してはマスメディアの影響が大きく、特にテレビによる最新の情報が住民に届くとたちまちその成分を含む商品が品切れになるほど影響があり、過剰摂取などによる人体への悪影響など懸念するところである。そのような物質の含有量を住民から尋ねられることが多いので、公的な機関からの分析量が必要と感じる。【行政】
- 特定成分名が食品名と共に混同して取り沙汰され、偏った消費行動を誘発すること等があるが、機能性成分について科学的データに基づく客観的な解説をするためのデータは不十分だと思うので。【研究教育】
- 健康増進目的でサプリメントを飲用されている方が多いので、食品に含まれる機能性成分の表示も必要と思う。【病院】
- 機能性を謳った食品等多く市販されており、食事で摂るよりサプリメント等で補充されている人が多く見られるようになっている。また、疾病予防や病態改善のために使用されている方もいるので、記載されると良いと思う。【福祉】
- 機能性成分が日本食品標準成分表に記載してあれば、特定保健用食品なども関与している保健機能成分にどのようなものがあるかわかりやすい。【研究教育】
- 市場において食品の機能性を謳う商品が氾濫しているが、指標となる含有量が定まっていないのが現状であるため。【研究教育】
- 機能性成分についての情報は氾濫しており、正しい情報の必要性があるため。【病院】
- 栄養教育の場で食品摂取を考えてもらう場合の情報提供として有効。【研究教育】
- 栄養サポートを実施していく場合に必要となる。【研究教育】
- 正しい情報を提供する、確認することが出来るので。ただし、別冊にする等しないと利用が難しいかも。【病院】
- テレビやインターネットで様々な情報が簡単に入手出来たり、サプリメントの需要の高さから考えて、日本食品標準成分表で具体的に機能性成分が数値化してあると、とても分かりやすいと思う。
- 正しい知識の普及のため。【行政】
3.栄養指導に関する意見
- ダイエットや疾病予防のために効果があるとマスコミ等で盛んに宣伝され、こういった成分が強調された食品の消費も増えている。正しい知識を普及し、栄養指導時の食品選択に役立つと思われる。【行政】
- 数多くの健康食品が出回っており、指導上知っておく必要がある。【学校健康教育】
- 含有量を知ることにより、栄養指導または施設内の食事提供の目安となる。
- 成分が多い食品の紹介はあるが、実際はどの位の量が含まれているのかまでわかると、具体的に使用量の指導もできると思う。【行政】
- 市民からの問い合わせが多いため。栄養指導をする上で、必要と考えたため。【行政】
- 今後の生活習慣病などの栄養相談のために把握しておいた方が良い。
- 栄養表示の指導の参考になる。サプリメントなどで種々のファイトケミカルが出回っているため。【行政】
- 病院栄養士として、疾患の治癒に貢献できる。【病院】
- 近年の不安定な経済状況において、病院への通院をできるだけ避けるために、今後更に機能性食品の利用が拡大することが予想される。特定保健検診・指導においても多くの質問が寄せられることは必至である。商品が神格化せず、正しい利用方法を指導するためには、是非とも必要な情報だと考えられる。【学校健康教育】
- サプリメントへの過剰な依存ではなく、食事を基本とした健康管理の方法を探りたいから。【学校健康教育】
- 日常摂取している普通の食物の中にも、多様な機能性因子を含んでいる食品があり、こうした食品の機能性成分を収載すれば、病気の予防の手助けに栄養士として参考にできるため。【研究教育】
- 指導する上で役に立つ。【地域活動】
- 何でもサプリメントに頼る人が増えていると思う。食品から命をいただいて生きているという基本的な考えを大切にしてもらうためにも、機能性成分を載せることにより、指導面へ活かせるのでは?
- サプリメントへの過剰な依存ではなく、食事を基本とした健康管理の方法を探りたいから。【学校健康教育】
- 栄養表示の指導の参考になる。サプリメントなどで種々のファイトケミカルが出回っているため。【行政】
- 特定の疾患の治療や予防に利用または期待される成分があるため。【研究教育】
- サプリメント類ではなく、通常の食材を使った食生活の中で病気が予防できることが期待されるため。【行政】
- 食のバランス・体のバランス両方の指導に活用出来ると思う。【集団健康管理】
- 健康食品・サプリメントが市場に多く出回っているため、栄養士としては食品中の機能性成分の含有量を知っておく必要があると思うから。【福祉】
- 生活習慣病と食品の機能性、食品機能と抗ガン作用の見地から。【病院】
- 栄養指導においてサプリメントを採っている患者から食品での含有量を聞かれることがあるため。
- スポーツ栄養学などで活用できると考えられるため。【学校健康教育】
- 栄養指導時や食品の持つ身体への影響を研究するときに、データとして使用したい。【研究教育】
- 高齢社会となり、健康な人のさらなる健康を目指したアンチエイジングの考えを取り入れた栄養指導、栄養教育も重要となってきている。そこで、抗加齢と関連のある機能性成分の収載を希望する。【研究教育】
- アンチエイジングへの関心の高まり等から、栄養指導の際必要な情報である。【地域活動】
- ORACは米国農務省が2007年に277品目について発表。その数値も参考になるが、我国特有の食品についての情報も知りたい。【地域活動】
- 生体調節機能の期待を栄養指導に役立たせたい。【病院】
- マスコミ等で大きく取り上げられ、その是非等が栄養教育に必要である。【集団健康管理】
4.その他の意見
- 新素材が多く出回っているため。【地域活動】
- 最近、食事調査をする上で機能性食品を使っている人がとても多い。
- 専門家としてその食品に関する成分をより知ることができるため。【行政】
- 特定保健用食品を活用している方が多いため。【行政】
- 現状として利用している人があるので。【行政】
- 参考にさせていただきたい。【行政】
- 日本食品標準成分表が改定されるにつれてアミノ酸組成表、脂肪酸組成表と掲載されてきた。私は栄養士の職についてから短く、活用する場面は現時点ではあまりないが、機能性成分に関して記載があれば、活用の幅が広がると感じる。個人的にも関心がある。【行政】
- 最近の現状を考えると機能性食品を日常利用する機会が多くなっているため。【地域活動】
- 微量栄養素の欠乏・過剰摂取による身体に対する影響が大きい。【地域活動】
- 食事の聞き取りをすると「○○ダイエット」のような1つの食品を長期間食べ続ける例があり、その弊害を確認しやすくなることを期待して。【地域活動】
- サプリメントや栄養食品(特保含む)に対しても、広い知識を持つ事が必要と思うから。
- 栄養士だけでなく、一般の方にも生体調節機能を目にして欲しいから。【研究教育】
- どの程度の内容か、具体的に知っていないので想像する範囲(国民健康栄養調査の食品番号表に示されるような特別用途食品が一覧となるのかなとの想像)での回答となるが、データが多いと使い方が煩雑になるのではないかと。一般国民でも理解・利用できる内容・価格の資料であるものと、専門家が欲しい詳細なデータが入っている日本食品標準成分表とに分けられている方が良いと思う。【行政】
- 時代のニーズに対応するため。【病院】
- 近年、生活習慣病予防の有効性が認められてきたので。【行政】
- 生活習慣病予防の面から研究が進められているため、この先必要になりそうだから。【行政】
- 指標が欲しいので。【集団健康管理】
- 健康増進法26条、31条、32条の2を担当しているので、根拠となるデータが必要である。【行政】
- 現在、食品中の生体機能性成分の含量が、ビタミン以外のものは示されていない。【研究教育】
- 献立作成の手助けとなる。
- 栄養強化食品に含まれることが多いが、一般に食べる食材にどのくらい含まれているかわからないから。
- 薬との関係等。
- 調節機能が知りたいので希望する。
- 主に生体調節機能との関係文献が少ない。【研究教育】
- 色々な食品について知ることは良いことだと思う。ただし、誤って使用されたり認識されたりしないようにする必要はあると思う。【研究教育】
- すでに常用している方も多く、すでに日常的な食品として一般化している。【病院】
- 健康維持、増進、また病気予防に役立つ成分であるため必要だと思う。
- 特定保健食品等、科学的根拠の一つとして、成分表が利用できると考えられるため。【行政】
- 記載されている方が便利だから。【研究教育】
- 日本食品標準成分表1冊で話をすることも出来るかも。【病院】
- 生体調節機能は医療者側も患者側も興味深く実用性があると思うから。【病院】
- 含有量により、一般に報道されている評価が過大評価かどうか判断する指標になる。他の栄養素との関係は?【地域活動】
- 機能性成分については、食品別に詳細が掲載されている資料が少ないので、日本食品標準成分表に記載されていると都合が良いと思うため。【行政】
- 興味があるから。【学校健康教育】
希望しない
得られた回答について以下に示す4種に区分した。各意見の末尾【 】内にに各栄養士会(学校健康教育栄養士協議会、行政栄養士協議会、研究教育栄養士協議会、集団健康管理栄養士協議会、地域活動栄養士協議会、病院栄養士協議会及び福祉栄養士協議会)の所属を記載した(アンケート用紙に記載の無かったものは、記載無し)。
1.機能性成分のエビデンスなどに関する意見
2.使い勝手・利便性に関する意見
3.現状肯定の意見
4.その他の意見
1.機能性成分のエビデンスなどに関する意見
- 摂取の目安量等のエビデンスがないものについては、収載されても適切な活用ができない。摂取に関するエビデンスと含有量の収載をセットで進めてもらいため。【行政】
- 一般消費者を対象とした成分表で、上記成分が記載されるには、以下の十分な体制整備がまず必要かと思う。●食品業者への栄養成分表示対応。●機能性成分のエビデンス(というよりも、管理栄養士がそれを読み解く能力について資質向上が必要)。【行政】
- (食事摂取基準のような)機能性成分の有効な量や、上限値などが示されたものがなければ、収載された数値を活用することが出来ない。【行政】
- 食事摂取基準等(厚労省)で適正量が判断できない成分表示は記載されても、行政としては府民に対して指導支援が出来ない。マスコミ等で機能成分に取り上げられている成分は時間の経過とともに変化するので、記載に限りが無いように思う。【行政】
- 臨床データが乏しい。エビデンスが不明。【病院】
- 現場(病院など)においては、栄養指導などで食品選択の情報として役立つ場合もあるかもしれない。しかし、ヒトレベルではっきり生体を調節すると言えるなら収載しても良いと思うが、まだ動物実験レベルやヒトレベルでも多くの結果が出ていないのであれば、日本食品標準成分表への収載はしない方が良いと思う。【研究教育】
- 機能性成分を「何mg摂ったら○○に良い」「○○になる」というエビデンスが、まだ豊富ではないから。【研究教育】
- 信頼できる根拠となるデータがまだ不十分であると考えられるため。【研究教育】
- 生体調節機能成分は同じ成分であっても、機能発現の条件が様々であり、一様に含有量を掲載することは機能性に対する誤解を生みやすい危惧が考えられる。また、ポリフェノールのような、複数の化合物の混合物は、機能を有する物質と有しない物質の含有量で機能が異なるため、その物質の定義を明確にする必要があると考えられる。【研究教育】
2.使い勝手・利便性に関する意見
- 現在、日本食品標準成分表は主に献立作成のために使用しているので、生体調節機能が期待される成分まで記載されると、日本食品標準成分表のデータが膨大なものになり、使い勝手が悪くなりそうなため。また、生体調節機能を同時掲載されると、一般の人はこの方ばかりに興味や関心が向き、食品を組み合わせてバランス良い食生活を大切にするより、特定の食品を薬のように扱って「ばっかり食」の風潮をもたらす危険性が生じると危惧するので、生体調節機能が特に必要な場合に調べられるよう、出来れば生体調節機能が判明した食品だけを掲載した成分表の出版物があればと期待する。【研究教育】
- 成分数が増えても、十分使いこなせていないため。【福祉】
- いろいろ載りすぎて細かくなり、わかりにくくなる。使いにくくなってしまうのでは?【行政】
- 科学的根拠があっても、摂取の仕方によってはフードファディズムと同様なことが起こるのではないかと思う。また、摂取に関する注意等を掲載すると情報量が多くなり、かえって使いにくくなるように思う。【行政】
- 機能性成分を明らかにすること、表示することには賛成するが、日本食品標準成分表に収載することは他の従来の成分表示との整合性の点で希望しない。別に付随の形なら良い。【研究教育】
- 項目が増えて分かりにくくなるため。
- 日本食品標準成分表は栄養士だけが使っているわけではなく、一般の方も使っている。生体調節機能が期待される成分の含有量を示すより、従来どおりで行うことの方が万人に利用が可能である。別冊として機能成分の含有量を収載した成分表を出してもらえるのは、非常にありがたい。【研究教育】
- 機能性成分の収載に関しては、その機能や種類が多いため、日本食品標準成分表が複雑になる可能性があり、栄養成分の活用に不便をきたすことが予想される。【行政】
- 機能性成分を含有するものには、通常日常食として利用されないものも多いと考えられるため、現状の栄養指導には使用がしづらくなる。【行政】
- 効果が確認された機能性成分を含む食品は、特定保健用食品として認定される制度があり、これについては個別に栄養成分表示がなされており、これらのデータを収載したものがあれば、日本食品標準成分表への収載は不要である。作成するなら、機能性成分のみを収載した別冊とすることが良いと考えられる。【行政】
3.現状肯定の意見
- 現時点で日本食品標準成分表に不都合を感じていない。【行政】
- 今のところ、現在の収載成分で対応できるため。【行政】
- 特に必要性を感じない。【病院】
- 現在の収載で充分に活用できている。【集団健康管理】
- 行政では、生体調整機能成分について、現在必要性を感じていない。【行政】
- 必要無い。【福祉】
- 日常必要としない。【地域活動】
- 学校教育においては現在記載の成分で対応できている。【学校健康教育】
- 学校関係では、児童・生徒に対しては、基本のものがあれば良い。保護者に対しては、あればあるように使うかもしれないが、学校は基本を伝えていくところのため、あまり必要性は感じていない。【学校健康教育】
- 今まで通りでも十分使いやすいので、特に載せる必要はないかと思う。【研究教育】
- 学校給食では必要ないと考える。【学校健康教育】
- 必要と思わないから。【病院】
- 通常の食品成分は常用量で摂取されるという前提で、現在の日本食品標準成分表で対応できる。生体調節機能が通常の食品で期待されることが明確なら、必要になる。【研究教育】
- 日常業務で活用する機会が少ないと思われる。【集団健康管理】
- 現在でも、かなり充実していると思う。【学校健康教育】
- 特に利用方法がないため。【病院】
- 学校ではあまり必要を感じないから。【学校健康教育】
4.その他の意見
- 栄養計算をする中で、加工品など成分の測定が十分されていないものが多く栄養計算が十分ではない。市販品成分表やインターネットなどで調べるが更に成分が追加されても、測定されていないものが多ければ意味が薄れる。成分を増やすよりは、食品を増やしてはどうかと思うため。【福祉】
- 話題性もあるし住民のニーズもあると思われるが、機能性成分だけが強調された食品表示が進むことが危惧されるため(虚偽誇大表示関連)。【行政】
- 機能性成分を細かく記載しすぎると、一般の消費者はそればかり気にし過ぎてしまうと考えるため。【研究教育】
- 食事は一食分全体として栄養等を考えたいと思っている。1つの食品の成分にこだわるとバランスが崩れてしまいそう。【地域活動】
- 収載されていたら便利かもしれないが、書かれていることだけを信じて、それだけ食べれば良いと思う人もいるかもしれないから。【研究教育】
- 機能性成分ばかりに目がいき、その他の栄養素が摂れなくなるおそれがある。その物ばかりを摂取し、摂り過ぎや、本来摂るべき他の栄養素を摂らなくなるなど、バランスがくずれる恐れがある。【福祉】
- 同じ野菜でも旬の時とそうでない時がある(例:夏のきゅうり、トマトと冬のきゅうり、トマト)。同じ野菜でも無農薬のものと農薬が使用されているものがある。同じ野菜でも塩素入りの水道水で洗った場合と塩素が入っていない水で洗った場合の差があるので、機能性成分の含有量が統一出来ないと思うから。【集団健康管理】
- 生体調節機能が期待される成分の分量が明示されているのであれば問題ないが、今のところそこまで活用できるとは思わない。【集団健康管理】
- 収載例が無く、判断できかねるため。【行政】
- 具体的な収載例が無いため、判断出来かねる。【行政】
- 「日本食品標準成分表」に「〜が期待される成分」を収載することに違和感がある。専門職のみが利用するものではないので、正しい取り扱いが行われるか、疑問が多いと思う。【行政】。
- 食品の本来の目的は「食生活指針」にも示されている様に、一般の食材による健康と楽しみ・喜びをもたらしてくれる食事を作るために、生産・販売されるべきだと思う。確かに健康志向の現代社会であるが、機能性成分は病気予防、健康増進のイメージが強く、一般の食材にまで機能性成分を記載すると、食材が機能性食品化し、食材の偏り、食事のバランスの崩れをきたす心配があると思う。【地域活動】
- やたらと機能性成分を載せれば、健康食品が広く流通している背景もあり、薬効が期待できる等、一般の方へ無用な混乱や誤解を招く恐れがある。(表示する場合は、誤解を招かないような記載方法を考慮する必要がある。)【行政】
- 生体調節機能については他の本が出回っているため。栄養成分さえ分かれば、どのような機能があるか予測出来るため。【病院】
- 必要かと思うが、返答する能力が欠けており、うまく記入出来ない。【福祉】
- 広範囲にわたるので把握できないため。
- 近年、生体調節機能成分についての研究が多く、その成分を含んだ食品が注目されており、それらを利用する人も増えてきているが、期待される成分が多くの方々が利用する成分表に記載されるのはどうかと考える。一般の方が極端にその成分を期待し過ぎて摂り過ぎたりする問題が生じる可能性があるからである。【研究教育】
- 栄養はバランスが大事であって、機能性ばかりを重要視して偏った考えや乱用される可能性があるので、希望しない。【研究教育】
- すべての機能性成分の記載が難しいのであるならば、1つや2つを取り上げたところで、まるでその機能性成分の摂取を推奨しているかのような誤解を招きかねないので。【研究教育】
- 一般市民が特定の機能性成分の摂取を考えるなど、食品成分摂取への十分な理解がないまま利用されることが予想されるから。【研究教育】
- 栄養指導教育において質問が皆無ではないが、このたびは特に希望なし。
2) 分析項目選定のための消費者アンケート調査結果
分析項目選定のため、一般消費者にアンケートを実施した。実施したアンケートについて、様式‐2に示した。アンケートの集計結果は、75〜82ページにまとめた。有効回答数は138であった。
アンケートの結果を見ると、設問2.で機能性成分の意味について、男性では約25 %、女性では約49%しか知っている人がいなかった。アンケートの序文に説明はされているが、抽象的な表現だったためか、完全には理解されていないと思われる。また、設問3.1.では男性では約35%、女性では約53%の人が機能性成分に関心があると回答しており、設問2.と大差は無い。
機能性成分の定義を理解していない回答者は多かったが、具体的な成分名を挙げた設問3.2.ではコラーゲン、カテキン、ポリフェノールをはじめ多くの成分について回答者が知っていると答えた。これらの成分はマスコミ等でも紹介されており、回答者が耳にする機会も多いと推測される。一方でマスコミ等ではあまり紹介されないケルセチンやフェルラ酸などの成分は、当然のことだが知っている人は少なかった。成分の知名度は情報量に左右されており、各成分の持つ機能性までは考慮されているかどうかは不明である。
設問3.3.では、代表的な食品が万遍なく挙げられており、回答者もバランスよく食事を採ることが重要であることは十分認識しているものと思われる。このことは設問1.で多くの回答者が普段から食事のバランスに気を配っていることからも伺える。また、設問3.4.で食品中に機能性成分が含まれているかどうかを重視する回答者の割合は、機能性成分に関心がある回答者の割合と概ね一致していた。
設問3.5.で機能性成分についての意見を尋ねたが、まず機能性成分についての定義について知りたいという意見があった。回答者の中には機能性成分とミネラル・ビタミンなどの栄養素との違いがわかりづらかった人が多いと思われる。さらに機能性成分については、効果・効能、摂取の仕方、摂取量、エビデンス(科学的根拠)、副作用などの情報について、知りたいという意見もあった。様々な情報が氾濫する中で、消費者に機能性成分が定着するかどうかは、信頼できる情報の提供が鍵となってくるものと思われる。
様式‐2
アンケートのお願い
財)日本食品分析センター
近年、食品は生命の維持、体力を保持する等の栄養的要素の他に、生体の機能を調整する役割が求められていると言われています。このような関心を満たすために、「機能性成分」という言葉がうまれました。この「機能性成分」についてどう思われるか、アンケートにお答えください。
性別 1.男 2.女
年齢 1.20歳未満 2.20代 3.30代 4.40代 5.50代 6.60歳以上
設問1. あなたは、普段、食事のバランスに気を配っていますか?
1.気を配っている 2.多少気を配っている 3.あまり気にしていない 4.全く気にしない 5.どちらともいえない
6.その他( )
設問2. 機能性成分という言葉をご存知ですか?
1.知っている 2.知らない
設問3. 以下に該当するものに○印を記入してください。
1.機能性成分に関心がありますか?
1.関心がある 2.関心がない 3.どちらともいえない
2.以下の機能性成分のうち、知っている言葉はありますか? あれば、その番号に○をつけてください。(いくつでも)
1.カテキン 2.イソフラボン 3.ルチン 4.ケルセチン 5.クロロゲン酸 6.テオブロミン 7.フェルラ酸 8.γ‐アミノ酪酸(GABA) 9.アスタキサンチン 10.カロテン(ルテインなど) 11.ポリフェノール 12.アントシアニン 13.クルクミン 14.タンニン 15.カフェイン 16.大豆サポニン 17.人参サポニン 18.グルコサミン 19.セサミン 20.ドコサヘキサエン酸(DHA) 21.コエンザイムQ10(CQ10) 22.ヒアルロン酸 23.コラーゲン 24.フラボノイド 25.カルニチン 26.ゼアキサンチン
27.その他( )
3.体に良いと言われている食品として何が思い浮かびますか? あれば、2.にお書きください。(いくつでも)
1.特にない
2.
4.食品を購入する時、機能性成分が入っていることを選択の目安としますか?
1.目安とする 2.多少は気にする 3.ほとんどしない 4.全くしない
5.どちらともいえない 6.その他( )
5.「機能性成分」について、どのような情報が知りたいと思いますか? また、ご意見などがありましたらご自由にお書き下さい。
ご協力ありがとうございました。
アンケートの回答者(138人)
| 男性 | 女性 | |
|---|---|---|
| 20歳未満 | 2 | 5 |
| 20代 | 6 | 13 |
| 30代 | 13 | 12 |
| 40代 | 10 | 10 |
| 50代 | 11 | 28 |
| 60歳以上 | 13 | 15 |
| 合計 | 55 | 83 |
設問1. あなたは、普段、食事のバランスに気を配っていますか?
| 男性 | 女性 | 合計 | |
|---|---|---|---|
| 1.気を配っている | 17 | 41 | 58 |
| 2.多少気を配っている | 21 | 39 | 60 |
| 3.あまり気にしていない | 13 | 3 | 16 |
| 4.全く気にしない | 3 | 0 | 3 |
| 5.どちらともいえない | 1 | 0 | 1 |
設問2. 機能性成分という言葉をご存知ですか?
| 男性 | 女性 | 合計 | |
|---|---|---|---|
| 1.知っている | 14 | 41 | 55 |
| 2.知らない | 41 | 42 | 83 |
設問3.
1.機能性成分に関心がありますか。
| 男性 | 女性 | 合計 | |
|---|---|---|---|
| 1.関心がある | 23 | 44 | 67 |
| 2.関心がない | 11 | 4 | 15 |
| 3.どちらともいえない | 21 | 35 | 56 |
2.以下の機能性成分のうち、知っている言葉はありますか? あれば、その番号に○をつけてください。(いくつでも)
| 成分名 | 男性 | 女性 | 合計 |
|---|---|---|---|
| コラーゲン | 51 | 82 | 133 |
| カテキン | 51 | 80 | 131 |
| カフェイン | 52 | 78 | 130 |
| ポリフェノール | 50 | 79 | 129 |
| イソフラボン | 46 | 81 | 127 |
| ヒアルロン酸 | 40 | 77 | 117 |
| タンニン | 43 | 70 | 113 |
| コエンザイムQ10 | 40 | 71 | 111 |
| DHA(ドコサヘキサエン酸) | 41 | 66 | 107 |
| グルコサミン | 36 | 70 | 106 |
| セサミン | 32 | 68 | 100 |
| カロテン(ルテインなど) | 33 | 65 | 98 |
| フラボノイド | 35 | 60 | 95 |
| アントシアニン | 24 | 63 | 87 |
| ルチン | 26 | 56 | 82 |
| γ-アミノ酪酸(GABA) | 19 | 56 | 75 |
| 大豆サポニン | 18 | 47 | 65 |
| カルニチン | 11 | 34 | 45 |
| クルクミン | 14 | 30 | 44 |
| アスタキサンチン | 6 | 33 | 89 |
| 人参サポニン | 11 | 21 | 32 |
| クロロゲン酸 | 10 | 13 | 23 |
| テオブロミン | 4 | 15 | 19 |
| ケルセチン | 3 | 9 | 12 |
| フェルラ酸 | 1 | 5 | 6 |
| ゼアキサンチン | 0 | 2 | 2 |
3.体に良いと言われている食品として何が思い浮かびますか?
回答に挙げられた食品名については、日本食品標準成分表の食品群に区分し、カウントした。
| 食品群 | 具体的な食品名 | 回答者数 |
|---|---|---|
| 豆類 | 大豆、納豆、豆腐、豆乳、おから、きな粉など | 92 |
| 野菜類 | 人参、ほうれん草、ごぼう、トマト、にんにくなど | 70 |
| 乳類 | 牛乳、ヨーグルト、チーズなど | 42 |
| し好飲料類 | 緑茶、コーヒー、ココア、ワインなど | 38 |
| 種実類 | ゴマ | 35 |
| 魚介類 | さんま、いわし、さば、ふかひれなど | 33 |
| 藻類 | わかめ、ひじき、めかぶなど | 29 |
| 果実類 | りんご、バナナ、みかん、ブルーベリーなど | 28 |
| 穀類 | 玄米、雑穀、麦など | 20 |
| 調味料類 | 酢、黒酢など | 11 |
| きのこ類 | しいたけ、まいたけ、エリンギなど | 9 |
| 肉類 | 牛肉、豚肉、レバーなど | 7 |
| いも類 | じゃがいも、こんにゃく、ヤーコンなど | 6 |
| 貝類 | あさり、しじみ、牡蠣など | 5 |
| 卵類 | 卵 | 3 |
| 特になし | − | 19 |
上記以外に、はちみつ4人、ウコン4人、アロエ3人、梅干し3人、塩2人、油(オリーブ油、リノール酸油)2人、ハーブ1人 の回答があった。
4.食品を購入する時、機能性成分が入っていることを選択の目安としますか?
| 男性 | 女性 | 合計 | |
|---|---|---|---|
| 1.目安とする | 2 | 4 | 6 |
| 2.多少は気にする | 18 | 35 | 53 |
| 3.ほとんどしない | 19 | 23 | 42 |
| 4.全くしない | 11 | 9 | 20 |
| 5.どちらともいえない | 4 | 3 | 7 |
5.「機能性成分」について、どのような情報が知りたいと思いますか? また、ご意見などがありましたらご自由にお書き下さい。
◆機能性成分の定義に関する意見
- 機能性成分とは何か。【20代 女性】
- 機能性成分という言葉自体知らない。機能性成分の意味を知りたい。【40代 女性】
- 機能性成分の意味がわからない。【30代 男性】
- 定義が知りたい。どういう効果があるのか。【20代 男性】
- 機能性成分という言葉を始めて知ったので、どのような成分が身体によい働きをもたらすのか知りたい。食品を購入するときに表示されていたら、気にかけて見て、判断材料になると思う。【20代 女性】
- ビタミン類と機能性成分の違いは何か。【20歳未満 女性】
- イソフラボンとは一体何か?【30代 女性】
- 機能性成分という熟語を知らなかった。各成分の名称はTVのCMで知っているだけで、カフェイン以外の成分はその内容がわからない。【60歳以上 男性】
- 機能性成分自体知らなかったので、まずはその言葉の説明を知りたい。その次のステップとして、様々な情報を知りたいと思うと、現時点では考えている。【30代 男性】
◆機能性成分の仕組み・効果・効能に関する意見
- 害があるか。どの程度体にいいのか。【20歳未満 男性】
- どの成分が身体のどこに効くかというのを詳しく知りたい。【20歳未満 女性】
- 多くの成分の名前は良く聞くが、どういうものなのか、どういう効果をもたらすものなのか全然わからないので、そういった情報を知りたい。【20歳未満 女性】
- 具体的にどのような作用があるか(そのメカニズム)。【20代 女性】
- 期待できる効果。【20代 女性】
- 機能性成分がどのような食品に含まれているか。機能性成分が具体的にどのような影響(効果)を身体にもたらすのか。【20代 女性】
- 身体に吸収されるメカニズム。【30代 男性】
- 何に効果があり、どのように効くのか。【30代 男性】
- 何がどの機能をどのように調整するのか。【30代 男性】
- どのような効果があってどんな食品に多く含まれているのか。【30代 女性】
- どのように身体によいのか?【30代 女性】
- 機能性成分の効果。【40代 女性】
- 機能性成分の特徴。【40代 女性】
- 有効に作用するのかどうかという点。【40代 女性】
- 実際の効果との因果関係を示してほしい。【40代 女性】
- 具体的な役割。【50代 男性】
- どのような機能性成分がどのような機能維持に有効かについて知りたい。【50代 男性】
- 機能性成分は聞いたことがあっても、どのような機能とか、体にどのように良いかは、あまりわかっていない。【50代 女性】
- どの食品にどのような機能性成分が含まれ、それがどのように体に良いのか、という情報を知りたい。【50代 女性】
- 機能性成分のそれぞれが、どのような良い働きがあるのか、具体的かつわかりやすく知ることのできる情報がほしい。【50代 女性】
- 効能。名前だけは知っているが、それがどう体にいいのかは知らないので。【50代 女性】
- どのような成分が、どのような働きをするのか、知りたい。【50代 女性】
- 機能性成分の入っている食品が体にどのような影響を及ぼすのか。【60歳以上 男性】
- 機能性成分と効能の関連について。【60歳以上 男性】
- どのような効能があるのか。【60歳以上 女性】
- 成分別に、機能の役割。言葉は知っていても機能の意味がわからないので知りたい。【60歳以上 女性】
- 安全性(LD50)。【40代 男性】
- 体調管理に関する情報が知りたい。【50代 男性】
- 体内脂肪の減少・血糖値の低下。【50代 男性】
◆摂取量の目安、摂取の仕方・組み合わせなどに関する意見
- どの位の量をどの位の頻度で摂取することがよいのか。【20代 女性】
- 機能性成分が入っている食品をどの位の量食べると体に良いのか。【40代 女性】
- テレビなどでは、一つの成分について取り上げているものが多いが、毎日の食事全体でどの成分をどのくらいずつ摂取するのが良いのかがわかりづらいので、それぞれの良さを知った上で、どういうバランスで取り入れるのが一番良いのかを知りたい。【20代 女性】
- どの位食べたら良いと言われる効果が出るのか。例えば、トマトのリコペンが良いと言われても、何個位食べれば良いのかわかりづらい。【30代 女性】
- 何をどのくらい摂れば良いのかわからないので知りたい。【30代 女性】
- 一日に摂取したら良い適量を知りたい。【50代 女性】
- それぞれの機能性成分を含む食品を、どのくらいの分量食べたらどのくらい効能があるのか。【60歳以上 女性】
- 摂取量。取り合わせ方。【60歳以上 女性】
- 成分別に、年代により摂取量とか方法。【60歳以上 女性】
- どのように摂取したら効果的か。【20代 女性】
- 効率よく摂取するための調理法など。【30代 女性】
- 摂食の仕方(1.いつ?…朝食時・運動後・就寝前etc。2.効果的な摂り方は?…機能性成分の組み合わせ方で効果がアップする摂り方。3.摂取量…年代別・男女別に)。【40代 女性】
- 適量とその摂取の仕方(例えば一度に一日量取っても有効なのか、食事のタイミングで日に3回摂った方が良いのかなど)。【30代 男性】
- 相乗効果。【30代 女性】
- 組み合わせたら効果が上がる機能性成分があったら知りたい(相乗作用)。【50代 女性】
- 摂取の仕方(頻度など)、食べ合わせ(同時にとってはいけないものなど)。【40代 女性】
- 組み合わせてはいけない機能性成分があれば知りたい(相互作用)。【50代 女性】
- 機能性成分を阻害する食品を知りたい。【50代 女性】
- 機能性成分の吸収が良くなる食品の組み合わせ。望ましくない組み合わせ。【40代 男性】
- 効果的な組み合わせ例。あれば、同時に摂取すると効果が薄れてしまう組み合わせ例。【30代 男性】
◆過剰摂取に関する意見
- 摂り過ぎてはいけないものとそうでないものの区別(過剰症)。【40代 女性】
- 過剰摂取の注意点など予め知りたい。【50代 女性】
- サプリメントとして摂取しても良いか。摂り過ぎはかえって毒になるのではないか。【60歳以上 女性】
- 摂取し過ぎた場合の影響等。イソフラボンの時のように摂取過多による影響などもきちんと情報を公表していくことが必要だと思う。【20代 男性】
◆食品中の機能性成分に関する意見
- どのような食品に入っているのか。【20歳未満 男性】
- 機能性成分がどのような食品に多く含まれているかについて知りたい。【50代 男性】
- どんな食品に含まれているのか。【30代 女性】
- 機能性成分が含まれている食品。【40代 女性】
- 食品中の機能性成分の含有量。【20代 女性】
- 健康食品に含まれている量や純度、効果など。【30代 女性】
- 何から抽出しているのか。【30代 女性】
- 含有成分にばらつきがないかどうか。信頼性のある検査機関が検査しているのかどうか。【40代 女性】
◆機能性成分の情報開示に関する意見
- 商品のどこに表示されているか。【20代 女性】
- 効能をわかりやすく食品などに表示してあると、商品を手に取るきっかけになると思う。【20代 女性】
- 加工食品ではなく素材そのものの持つ機能性成分の量がわかる成分表のようなものがあると参考になる。また、一日の所要量がわかっている成分については、多く含まれる成分を挙げる、かつその食品をどれだけ摂取すればいいかも知りたい。また調理方法によってどれだけ損失するかもわかるとなお良い。取り合わせによる効果の違いもあるだろう。今後はますます自分で自分の健康を守る未病対策を各自で行う必要があると思う。病気と機能性成分の関係も明らかにされているので、国民の健康増進・維持の指標となるようなデータの公開をしてもらえると良いと思う。【30代 女性】
- 名前だけが(コマーシャル等で)ひとり歩きしているように思う。どういう食品にどういう成分が多く含まれているのか。どういう効果があるのか。摂取量等の情報が欲しい。【50代 女性】
- マスコミに食品に関するあらゆる情報があふれているが、賢い消費者になって毎日の食事に役立てたい。【50代 女性】
- 食品ごとの総量(又は単位量)等、一日の必要量の表示、摂り過ぎのデメリット等の一覧表があるか。【60歳以上 女性】
- 機能性成分にかかわる言葉は新聞やTVのコマーシャルで耳にするが、言葉自体はそれほど知られていないと思うので、宣伝の必要を感じている。また、これらの食品PRが多くあればと思っている。【60歳以上 男性】
- 各成分の機能を一般人が正しく知ることができる広報。【60歳以上 男性】
- どんな機能があって、どの程度の分量で、効果や機能が現れてくるのか、パッケージに明示されていると参考になると思う。【40代 男性】
- ネット上の正しい情報。【40代 男性】
- 科学的根拠に裏付けられた正しい情報をネット等で知りたい。【40代 男性】
- 何がどれだけ含まれているということが商品に書かれていると思うが、それをどれだけ摂ると効果があるのか、ということも知りたいと思う。【20代 男性】
◆バランスが取れた食事が基本であるという意見
- 毎日のご飯作りでは、機能性成分に重点はおかない。機能性成分というのは、”毎日続ける”イメージか。例えばサプリメント。我が家では毎日酢大豆を食べる。イソフラボンを聞く前からずっと食べ続けている。ビタミンB2。やはり栄養素で考えている。【30代 女性】
- 健康の基本はバランスの取れた食事と思っているので、機能性成分は利用していない。何か病気にでもなったら利用するかも…。でも薬の方が良い結果が得られるからやはり利用しないと思う。【50代 女性】
- 現代の一つの流行なのではと思っている。あまり気にせず、バランスの良い食事を取りたいと思う。そして毎日の食事をおいしく食べられるとよいと思う。【50代 女性】
- 毎日の食事をバランスの取れた食品・食材によって健康を維持することが大切だと考えている。【50代 女性】
- 減塩・酢摂取・水分(茶)を良くとる、また、万遍なく食品を摂るように心がけている。三食きちんととること。サプリメントに頼ることなく食品で摂るようにしたい。毎日少しずつでも運動を取り入れることは必要。季節のものをできるだけとること。【60歳以上 女性】
- 特に気にせず、好き嫌いなく万遍なく食べていれば良いと思っている。【60歳以上 女性】
- 三大栄養素、ビタミン、鉄分、カルシウム、塩分、カリウム等のみ考慮し、機能性成分のことは全く無視した生活をした場合、どんな問題が発生するか。【60歳以上 男性】
- 特になし。おいしければ良い。【60歳以上 男性】
- 機能性成分の情報によって食品を選んで食べ続ける自信がないので、機能性成分の情報を得たいと思わない。【60歳以上 男性】
- 特に現在まで意識することなく食事を摂取していて、それなりに健康であるので、わざわざそれらの成分を抽出してサプリメント化してまで摂取する必要があるのか疑問に感じる。【20代 男性】
◆その他の意見
- 本当に効能があるのか疑問。パッケージなどで効能を強調し過ぎている気がする。【30代 女性】
- 健康食品(錠剤)は体に効くのか。【60歳以上 女性】
- 機能性成分の色々の言葉が難しい。専門用語は良くわからない。【30代 女性】
- 商道徳を守り、販売すべき。【60歳以上 男性】
- サプリメント会社より来ているので特になし。サプリメントで飲んでいるので食品に入っているものを買おうとは思わない。【50代 女性】
3)データベースに関する文献
1.イソフラボン類
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| 北海道産大豆及び大豆加工食品中のイソフラボン含有量について 高橋哲夫、斉藤明子ほか 北海道衛生研究所 所報、 52、 29-36(2002) |
イソフラボン類は同種の食品であっても、生産地、製造方法、製造時期等によって含量が大きく変動することが知られている。 イソフラボン配糖体は食品の製造過程において、あるいは体内に摂取された後腸内細菌によって分解され一部がアグリコンに変化するため、イソフラボンを酸加水分解することによりアグリコンとして定量を行った。 調査試料は乾燥大豆、きな粉、豆腐、凍り豆腐、おから、油揚げ、がんもどき、納豆、味噌、醤油計43試料。 酸加水分解をすると、ゲニステイン、ビオカニンA以外は93%以上の回収が認められたが、ゲニステインは低く、74%であった。 |
(1)非加水分解試料 均一にした試料1.0gに内標(6-メトキシフラボン)を添加し、80%メタノール40mlを加え、超音波照射20分。室温で20時間放置後、抽出液に80%メタノールを加えて全量を50mlとし、遠心分離(3000r/min、10分)。上澄み5mlに水を加えて全量を45mlとし、その9mlをCHEM ELUTに負荷。20分放置後酢酸エチル100mlで溶出。溶出液を乾固後、メタノール2mlに溶解しHPLCで測定。 (2)加水分解試料(Frankeらの加水分解法) 均一にした試料1.0gに内標を添加し、濃塩酸7ml、0.06% BHT含有エタノール35mlを加え、超音波照射20分。3時間加熱還流して加水分解。放冷後水を加えて50mlとし、遠心分離(3000r/min、10分)。上澄み5mlに水を加え全量を45mlとし、その9mlをCHEM ELUTに負荷。以下非加水分解試料と同じ。 |
| Content and composition of isoflavonoids in mature or immature beans and bean sprouts consumed in Japan Nakamura Y., Kaihara A. et al. Journal of Health Science, 47(4), 394-406(2001) |
国内及び海外の34種類の生豆(大豆を含む)と、国内の未成熟の豆5種類、スプラウト5種類について、加水分解を行い、イソフラボン6種(ダイゼイン、グリシテイン、ゲニステイン、ホルモノネチン、ビオカニンA、クメステロール)を定量した。加水分解なしのデータも一部ある。 | 加水分解なし:粉末1g、粉砕済みの未成熟の豆2g、粉砕済みのスプラウト3gを各試験管にとり、80%メタノール50mlで30分間超音波抽出後、室温で24時間抽出。遠心分離(1000g、15分、5 ℃)後、メタノールで50mlに定容。 加水分解あり:上記同様にサンプリングし、10 M HCl 10mlと0.05% BHT含有エタノール40mlを加え、30分超音波抽出。沸騰水浴中で3時間加熱還流後、遠心分離(1000g、15分、5 ℃)。 |
| ダイズ種子中のイソフラボン含有率の品種・収穫年度による差異 山川武夫、仲野快恵ほか 日本土壌肥料学雑誌、 78(1)、 33-38(2007) |
ダイズにはかなりの品種があり、ほとんどの品種のイソフラボン含有率は分析されておらず、環境的要因についても詳しいことはわかっていない。本研究は広範囲のダイズ品種、すなわち早生ダイズから秋ダイズにかけて同じ圃場で栽培した種子を用い、その収穫年度と品種間での含有イソフラボンの種類と含有率の差を明らかにすることを目的としている。 | 凍結乾燥後粉砕した試料150 mgに70%エタノール0.75ml(枝豆ダイズには1.5ml)を加え、ボルテックスでかくはん後、振とう抽出(150rpm、25 ℃、2 h)。遠心分離(13000rpm、10分、4 ℃)後、上澄みをHPLCで分析。 |
| 国内産大豆のイソフラボン、チアミン、リボフラビンおよびトコフェロール含量の変動 西場洋一、須田郁夫ほか 日本食品科学工学会誌、 54(6)、 295-303(2007) |
国内における大豆の微量栄養・機能性成分の実態解明の一助とする目的で、北海道から九州までの国内各地域の大豆試験圃場から主要大豆品種を含む大豆品種を入手し、大豆に期待される微量成分の中からイソフラボン、チアミン、リボフラビン、トコフェロールを分析し、各成分の変動や、各栽培地において品種が与える影響等を調べた。 国内各地域産の大豆は20品種・31試料。 九州各地産の「フクユタカ」は11ヶ所11試料。 |
大豆約100gを粉砕。粉砕試料2gに70%エタノール25mlを加えて30分間振とう抽出後、遠心分離し抽出液を分取。残さに対し同様の抽出をさらに2回行い、抽出液を合わせて100mlに定容。フィルターろ過後HPLCで分析。 |
2.カテキン類
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| Catechin contents of foods commonly in the Netherlands. 1.Fruits, vegetables, staple foods, and processed foods Arts, I.C.W., Van de Putte, B. et al. J. Agric. Food Chem.,48,1746-1751(2000) |
C(カテキン)、EC(エピカテキン)、GC(ガロカテキン)、EGC(エピガロカテキン)、 ECg(エピカテキンガレート)、EGCg(エピガロカテキンガレート)について、24種類の果物、27種類の野菜・豆、何種類かの主食、加工品中の含量を調べた。検体は1997年から1998年に4回に分けて入手した。最低1 kg(0.5 kgのものもあり)、3ロット購入した。 りんごは7品種、ナシは4品種について測定。結果はC、ECの測定値のみ記載(EGCgは全てND、その他は時々含まれていた)。Cは野菜、主食品(米、マカロニ、小麦、パン)には含まれていなかった。 |
チョコレート以外の検体は液体窒素下で小さく切り、凍結乾燥後、-20 ℃にて保管。凍結乾燥品に含水メタノールを加えて1時間振とう抽出。チョコレートは凍結乾燥せずに還流抽出。アントシアニンを多く含む果物についてはそれらを前処理によって分離した。 測定はHPLC(UV-FL)。UV:270 nm、FL:Ex 280 nm、Em 310 nm。メタノール/リン酸緩衝液のグラジエントまたはアセトニトリル/リン酸緩衝液のグラジエント。 分析はN=2分析、添加回収試験はりんごで92〜105 %だった。分析時にコントロールを一緒に測定。 |
| オートクレーブ処理した茶葉および茶ドリンクのカテキン成分 黄素梅、井上和美ほか 日本食品化学学会誌、 11(2)、 99-102(2004) |
新鮮茶葉をオートクレーブ処理したもの、市販茶葉をオートクレーブで処理したもの、市販茶ドリンク(5種)についてHPLC分析を実施。 通常の茶葉にはEGCg、ECgが多いが、オートクレーブ処理するとGCg(ガロカテキンガレート)、Cg(カテキンガレート)が生成する。GCg、Cgのほうがコレステロール吸収抑制作用があると報告されているので、オートクレーブ処理した茶葉は新しい素材となりうる。市販ドリンクはGCg、Cgが製造の工程で生成されるため、オートクレーブをしても値は増えなかった。 |
測定波長:280 nm(カテキン8種測定) カラム:ODS-80TS 4.6×250 mm 移動相:TBA含有緩衝液とアセトニトリルのグラジエント |
| HPLCによる各種緑茶に含まれるカテキン類の分析 西条了康、武田善行 日本食品科学工学会誌、 46(3)、 138-147(1999) |
抹茶、高級煎茶、普通煎茶、番茶、ほうじ茶、中国緑茶、ベトナム緑茶、インド緑茶について測定した。 日本緑茶ではエピ体4種(EC、EGC、EGCg、ECg)が総カテキンのほとんどを占めた。 外国産緑茶には日本緑茶よりも総カテキン量が多く含まれており(特にEGCg)、少量だがEGCmetg(エピガロカテキンメトキシガレート)、ECmetg(エピカテキンメトキシガレート)、EGCgg(エピガロカテキンジガレート)、ECgg(エピカテキンジガレート)などが入っていた。EGCmetg、ECmetg、EGCgg、ECggはアッサム種、中国種の特有成分と推察された。 |
粉砕した茶葉をアセトンで抽出した後メタノールに溶解。さらに固相抽出後、HPLCで測定。 |
| 茶葉及び茶飲料中のカテキン類、メチルキサンチン類及びアスコルビン酸の分析 小林千種、中里光男ほか 東京都立衛生研究所研究年報、 49、 135-143(1998) |
平成8〜9年に市販されていた煎茶、玉露、抹茶等の緑茶25検体、ウーロン茶5検体、紅茶5検体、健康茶3検体、清涼飲料2検体、缶入り緑茶16検体についてカテキン8種、カフェイン、テオブロミン、テオフィリン、アスコルビン酸の含量を測定した。 総カテキンは煎茶、玉露、抹茶、ウーロン茶、紅茶の順に高含量だった。浸出液中では玉露が一番高かった。缶飲料は2S体の含有量が50 %以上だった。 |
50 %アセトニトリルで抽出後、Bond Elut C18で前処理。 HPLC測定条件:UV 275 nm、ECD。カラム:ODS-H80 4.6×250 mm。移動相:メタノール-リン酸緩衝液。(アスコルビン酸は別条件) 11種一斉分析が行えるようカラム前処理・HPLCカラムについて検討を行った。ウーロン茶、紅茶でCgに妨害があったので、ECD(電気化学検出器)で測定することにした。検量線範囲はUV:5〜100μg/ml、ECD:1〜20μg/ml。 |
| Polyphenolic compounds and antioxidant activity of new and old apple varieties Wojdylo, A., Oszmianski, J. and Laskowski, P. J. Agric. Food Chem., 56, 6520-6530(2008) |
2005年、2006年に集めた67種のりんごについてカテキン(C)、エピカテキン(EC)、プロシアニジン、ケルセチン配糖体等17項目について測定した。 C、ECは全てのりんごで検出された。Cの含量は0.001〜0.07 %、ECの含量は0.007〜0.3 %であった。全てのりんごでCよりECの方が含量が高かった。 |
LC-MSとHPLC(UV吸収があるものについて)で測定。 |
3.フェノール酸(クロロゲン酸、フェルラ酸)
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| Analysis of phenolic compounds by High-performance liquid chromatography and liquid chromatography/mass spectrometry in potato plant flowers, leaves, stems, and tubers and in home-processed potatoes Im, H. W., Suh, B. S. et al. J. Agric. Food Chem., 56, 3341-3349(2008) |
じゃがいものクロロゲン酸含量の調査。 クロロゲン酸は5-カフェオイルキナ酸(CQA)の他に3-CQA及び4-CQAを類縁体として測定。 じゃがいもの大きさによる含量の差は認められなかった。部位は、中心部よりも端の方が含量が高い傾向が認められた。 品種間による差は非常に大きく、クロロゲン酸では3〜637 mg/100g、類縁体では0.3〜90 mg/100gであった。いずれの場合も、含量はクロロゲン酸>類縁体であった。 |
サンプルは凍結乾燥し、80 %エタノールを加え80 ℃で10分間加熱。ホモジナイズ後、遠心分離してから上澄みを濃縮乾固。80 %エタノールに溶解し、HPLCにて測定。 HPLCカラムはInertsil-ODSを使用。移動相はアセトニトリルと0.5 %ギ酸のグラジエント。 クロロゲン酸類縁体については、5-CQAの検量線から各CQAの濃度を算出。 クロロゲン酸のLODは16.5 ng相当。 |
| Simultaneous determination of all polyphenols in vegetables, fluits, and teas Sakakibara H, Honda Y. et al. J. Agric. Food Chem., 51, 571-581(2003) |
野菜、果物、茶中のポリフェノールの定量分析。 クロロゲン酸の含量はキャベツ:11.1μmol/100g、白菜:13〜28 μmol/100g、レタス:3.0〜8.2μmol/100g、ごぼう根:38〜178μmol/100g、アスパラガス:9.7〜24 μmol/100g、トマト:17.9μmol/100g、なす:31〜62μmol/100g、コーヒー豆:698μmol/100g、ブルーベリー:273〜325μmol/100g、ビワ:250μmol/100gであった。 フェルラ酸の含量はごぼう根:38〜100μmol/100g、ミズナ:7.17〜9.42μmol/100g、セリ:38〜178μmol/100g、なす:38〜180μmol/100gであった。 |
粉砕後凍結乾燥したサンプル50 mgに内標準物質を添加し、0.5 %酢酸含有メタノール2 mlを加えて超音波照射1分+遠心分離(3000 r/min、10分)を4回実施。抽出液を遠心濃縮機で乾燥後、DMSO 0.5 mlに溶解してフィルターろ過。 HPLC条件:Capcel pak C18 UG120(250×4.6 mm、S-5、5 mm)、ガードカラム(10×4.0 mm)、カラム温度35 ℃。波長は200〜600 nm。50 mMリン酸ナトリウム(pH3.3)含有10 %メタノールと70 %メタノールのグラジエント分析。ポリフェノールのピークがアグリコン標準品の保持時間と一致しない試料については、加水分解したものについても測定し、クロマトグラムを比較した。 加水分解条件:粉末50 mg、0.5 mg/ml BHT含有62.5 %メタノール4 ml、2 N HCl 1 mlをゴム付き試験管にいれ、小さな穴を開けたゴム栓を締める。90 ℃で2時間加熱し、酢酸エチル10 mlに分配。酢酸エチル層をN2ガスで乾固後、DMSO 0.5 mlに溶解してフィルターろ過。 |
| Quantitative determination of hydroxycinnamic acids in wheat, rice, rye, and barley straws, maize stems, oil palm frond fiber, and fast-growing poplar wood Sun, R. C., Sun, X. F. et al. J. Agric. Food Chem., 49, 5122-5129(2001) |
小麦、米、ライ麦、トウモロコシ、ヤシの葉油、早生パルプ木中のヒドロキシけい皮酸の定量分析。 エステル結合を切るためのアルカリ加水分解の温度を18、25、30 ℃で行ったところ、30 ℃が良好。 エステル、エーテル結合のヒドロキシけい皮酸を総ヒドロキシけい皮酸として測定した。測定物質はシナピン酸、p-ヒドロキシ安息香酸、p-ヒドロキシベンズアルデヒド、バニリン酸、シリンガ酸、バニリン、シリンガデヒド、アセトバニリン、p-クマル酸、フェルラ酸。シナピン酸はNDの検体もあったが他は全て検出した。全体的に小麦、トウモロコシが含量が高かった。 |
トルエン及びエタノールの混液で抽出後、アルカリ加水分解。さらに95 %エタノールで抽出し、クロロホルムに分配した後、メタノールに再溶解してHPLC測定。 カラム:Hichrom H5 ODS。測定波長:320 nm。 移動相は水、メタノール、酢酸のグラジエント。 |
| High-performance liquid chromatography determination of phenolic constituents in 17 varieties of cowpeas Cai, R., Hettiarachchy, N.S. et al. J. Agric. Food Chem. 51, 1623-1627(2003) |
ササゲ豆17品種中におけるフェノール類の含量測定。加水分解前後で比較した。 測定物質はプロトカテキュ酸、p-ヒドロキシ安息香酸、カフェイン酸、p-クマル酸、フェルラ酸、2.4-ジメトキシ安息香酸、ケイ皮酸。 17品種のうちLouisiana Purplehullが最も高含量だった。 また、加水分解により含量が最も増えたのはプロトカテキュ酸で30倍程度、フェルラ酸は2倍程度だった。 |
メタノールで還流抽出後、HPLC測定。一部の抽出液についてアルカリ加水分解し、pH調整後、HPLC測定。 カラム:TSK-gel ODS。波長:254、238 nm。 移動相はTFA、アセトニトリル、メタノールのグラジエント。 |
4.フラボノイド(フラボノール類、フラボン類、フラバノン類)
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| ピーマンを主とした市販野菜類のフラボノイド含有量における季節変動 井奥加奈、高田陽子ほか 日本食品科学工学会誌、 52(4)、190-195(2005) |
市販野菜のフラボノイド含有量について、季節間の変動を調査した。ピーマンについては年間を通じてケルセチン、ルテオリンの含量を測定。青梗菜、小松菜、ケール、ほうれん草、青じそについては6月と1月の差を調査した。 ピーマンのケルセチン含有量は1〜6月が7〜12月に比べて低く、また10〜12月は産地間による差も認められた。ルテオリンは年間を通してケルセチンよりも含有量が高く、傾向はルテオリンと同じ。 ケールは含有量が多く、ケルセチン19.7 mg/100g、ケンフェロール31.7 mg/100gであった。 |
加水分解を行い、アグリコンとして測定。 分析法:凍結乾燥した試料を1 g採取し、70 %エタノール100 mlで24時間、30 ℃、暗所で抽出。抽出後、濃縮した溶液に2 mol/L塩酸を加え、60分間沸騰水浴中で加水分解。Sep-pak ODS-Lightで精製し、HPLC測定。(HPLC条件は既報通り) |
| 世界のソバにおけるルチン含量の品種間差 氏原暉男、北林広巳、南峰夫 New Food Industry、 39(5)、 63-68(1997) |
普通ソバ27品種とダッタンソバ16品種のルチン含量を調査した。 | HPLCで測定。 |
| Simultaneous determination of all polyphenols in vegetables, fluits, and teas Sakakibara H., Honda Y. et al. J. Agric. Food Chem., 51, 571-581(2003) |
野菜、果物、茶中のポリフェノールの定量分析。 野菜ではタマネギ実にケルセチン配糖体:92〜178μmol/100g、ケルセチン:1.2〜1.9 μmol/100g、セロリ葉にアピゲニン配糖体:18〜51 μmol/100g、アピゲニン:5.3〜16μmol/100g、パセリにアピゲニン配糖体:235〜873μmol/100g、アピゲニン:8.6〜331μmol/100g、白菜にケンフェロール配糖体:54〜115 μmol/100g、セリにケルセチン配糖体:16〜108μmol/100g、イソラムネチン:65〜129μmol/100g、アスパラガスにケルセチン配糖体:7.7〜95μmol/100g、ネギにケンフェロール配糖体:79.1〜95.4μmol/100gが含まれていた。 果物ではオレンジにヘスペリジン:148 μmol/100g、ナリンゲニン配糖体:167 μmol/100g、りんごにケルセチン配糖体:8.0〜13μmol/100g、グレープフルーツにナリンゲニン配糖体:152〜438 μmol/100g、ナリンゲニン:4.6〜27μmol/100gが含まれていた。 |
粉砕後凍結乾燥したサンプル50 mgに内標準物質を添加し、0.5 %酢酸含有メタノール2 mlを加えて超音波照射1分+遠心分離(3000 r/min、10分)を4回実施。抽出液を遠心濃縮機で乾燥後、DMSO 0.5 mlに溶解してフィルターろ過。 μHPLC条件:Capcel pak C18 UG120(250×4.6 mm、S-5、5 mm)、ガードカラム(10×4.0 mm)、カラム温度35 ℃。波長は200〜600 nm。50 mMリン酸ナトリウム(pH3.3)含有10 %メタノールと70 %メタノールのグラジエント分析。ポリフェノールのピークがアグリコン標準品の保持時間と一致しない試料については、加水分解したものについても測定し、クロマトグラムを比較した。 加水分解:粉末50 mg、0.5 mg/ml BHT含有62.5 %メタノール4 ml、2 N HCl 1 mlをゴム付き試験管にいれ、小さな穴を開けたゴム栓を締める。90 ℃で2時間加熱し、酢酸エチル10 mlに分配。酢酸エチル層をN2ガスで乾固後、DMSO 0.5 mlに溶解してフィルターろ過。 |
| Flavonoid composition of fruit tissues of Citrus species Nogata Y., Sakamoto K. et al. Biosci. Biotech. Biochem., 70(1), 178-192(2006) |
カンキツ果実に含まれる主要な機能性成分である17種類のフラボノイド類について、カンキツ果実45種のアルベド、フラベト、じょうのう膜及び果肉における組成・含量を調査した。 | フラベド、アルベド及びじょうのう膜は凍結乾燥後粉砕。試料100 mgにメタノール-DMSO (1:1)5 mlを加え、室温で12時間抽出。遠心分離(3000×G、10分)後、上澄みを分取。残さにはさらにメタノール-DMSO(1:1)1 mlを加え2回以上抽出。抽出液を合わせ、蒸留水で10倍に希釈し、 Sep-Pack C18(0.36 g、メタノール5 ml、10 %メタノール10 mlでコンディショニング)に通液。10 %メタノールで洗浄後、メタノール-DMSO(1:1)で溶出。溶出液を5 mlに定容し、フィルターろ過。 果肉はミキサーでホモジナイズ後遠心分離(15000×G、20分)し、上澄み3 mlを上記方法で精製。 |
5.カロテノイド
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| USDA-NCC Carotenoid Database for U.S.Foods 1998 Holden, J.M et al |
約300種の食品について、α-カロテン、β-カロテン、β-クリプトキサンチン、ルテイン+ゼアキサンチン含量及び約80種の食品のリコペン含量を調査。 | |
| 日本で一般的に消費される野菜中カロテノイド量の定量 Aizawa, K; Inakuma, T. Food Sci. Technol. Res., 13(3), 247-252(2007) |
70種の野菜のカロテノイド量を逆相HPLCで定量した。α-カロテンは55種で、β-カロテンは全種で、リコペンはトマト4種と金時にんじんで、カプサンチンは2種のアマトウガラシで、ルテインは68種で、ゼアキサンチンは30種で、β-クリプトキサンチンは12種で検出された。葉野菜には高含量のβ-カロテンとルテインが含まれていた。それに対して果物では様々なカロテノイドが見られた。 | 3 %ピロガロールを加えてホモジナイズ。AOACの試料分析法抽出に準じる。試料5 gにヘキサン・アセトン・エタノール・トルエン(10:7:6:7)を10 ml加え、乳鉢で磨砕。抽出液の色がなくなるまで2-3回繰り返す。エタノールで100 ml定容。10 ml分取し、ピロガロール0.2 g、60 %KOH-メタノール1 ml、KOH 0.5 gを加え、40 ℃30分けん化。ヘキサン・酢酸エチル(9:1)で数回抽出。溶媒留去。HAET・エタノール(4:6)10 mlに溶解。HPLCはYMC C30 Carotenoidカラム、460 nm、移動相A:メタノール・MTBE・水(83:15:2)0.05 %トリエチルアミンと0.1 %BHTを含む、移動相B: (8:90:2)でグラジエント。 |
| 果物、野菜中のカロテノイド含量とそのデータの評価 Mangles, A.R., Holden, J.M, J. Am. Diet. Assoc., 93, 284-296(1993) |
果物、野菜(計120)中のα-カロテン、β-カロテン、ルテイン(+ゼアキサンチン)、リコペン、β-クリプトキサンチンの含量を文献調査によりまとめた。1971〜1991に発表された180以上の文献を調査し、クロマトグラフ法によるものだけを採用した。含量は平均値、最大最小値を記載し、またそのデータの信頼性評価も示した。それぞれの品名につき、採用したデータの数及び信頼できる参考文献の数も記載した。 | 掲載なし |
| 日本の生及び加工果物中のカロテノイド含量 Yano, M., Kato, M. Food Sci. Technol. Res., 11, 13-18(2005) |
生の果物75種及び加工果物15種について10種のカロテノイド(フィトエン、ζ-カロテン、リコペン、α-カロテン、ルテイン、β-カロテン、β-クリプトキサンチン、ゼアキサンチン、all-trans-ビオラキサンチン、9-cis-ビオラキサンチン)をHPLC法で測定した。 | 10 %炭酸Mg含有40 %メタノールを加えホモジナイズ。カロテノイド色素を、0.1 % 2、6-ジ-tert-ブチル4-メチルフェノール含有アセトン・メタノール(7:3)で抽出。飽和NaCl溶液を加え、ジエチルエーテルに転溶。20 %KOH-メタノールを加え、窒素置換して室温で一夜けん化。飽和NaCl溶液を加え、ジエチルエーテルに転溶。脱水、濃縮してメチル-tert-ブチルエーテル・メタノール(1:1)に溶解。回収率89.8〜105.5 %。YMC Carotenoid S-5 、250×φ4.6 mm、DAD、3液のグラジエント溶出。 |
| オランダにおける牛乳及び乳製品中のレチノール、カロテノイドの特徴(差異) Paul J.M.Hulshof, J. Food Composition and Analysis, 19, 67-75(2006) |
牛乳及び乳製品中のレチノール及びカロテノイド(ルテイン、ゼアキサンチン、β-クリプトキサンチン、α-カロテン、β-カロテン)の含量を測定した。 | 液体試料:試料1 mlに25 %アンモニア溶液0.25 ml及びエタノール1 ml加える。0.0025 %BHT含有ジエチルエーテル、石油エーテル各2 mlを加えて振とうし、脂溶性成分を抽出する。2回繰り返す。溶媒を揮散させ、0.2 %ピロガロール含有KOHエタノール1.5 ml加え、窒素置換し、暗所で3時間振とうする。終了後ヘキサン3 mlで2回抽出する。溶媒揮散後、メタノール・THF(3:1)0.25 mlに溶解し、HPLCに注入する。 チーズの場合:1 gに0.01 %BHT含有THF 30 mlを加えミキサーでかくはんし、ろ過する。残さの色がなくなるまで繰り返す。抽出液を濃縮し50mlとする。この2 mlを分取し、溶媒留去したのち、けん化を行う。 Vydac 218TP53(C18)、 250×3.2 mm、グラジエント溶出、メタノール・水・THF・トリエチルアミン(87.9:10:2:0.1)、メタノール・THF・トリエチルアミン(92.4:7.5:0.1)の2液。450 nm。 |
| オーストリアにおけるカロテノイドデータベースの開発 M. Murkovic, K. Gams, J. Food Composition and Analysis, 13, 435-440(2000) |
カロテノイドデータベースを創設した。頑健な試験法及びサンプリングに焦点を当てた。試験法はヨーロッパのEC MATプロジェクトで確立されたものを用いた。試料は気候の異なる3ヶ所から採取した。(対象はルテイン、ゼアキサンチン、β-クリプトキサンチン、リコペン、α-カロテン、β-カロテン) | 試料10 gに1 g炭酸Mg加え中和。THF:MEOH(1:1) 50 mlと内標(β-アポ-8'-カロテナール)を加えホモジナイズ抽出。ろ過、残さからさらに2回抽出。石油エーテル50 ml、10 %NaCl 50 ml加え振とう。計3回石油エーテルで抽出。濃縮。移動相に溶解。Vydac、 201TP54カラム。250×4.6 mm。0.1 %BHT含有アセトニトリル・メタノール・ジクロロメタン(76:20:4.5)。450 nm。 |
| スペインにおける生及び調理した野菜のカロテノイド構成 Fernando Granado, Begona Olmedilla, J. Agric. Food Chem., 40, 2135-2140(1992) |
スペインでよく使われる18種類の野菜について、生及び調理後のルテイン、ゼアキサンチン、リコペン、β-クリプトキサンチン、α-カロテン、β-カロテン、γ-カロテン含量を調べた。 |
6.γ‐アミノ酪酸
| タイトル、著者名、出典 | 概要 | 分析法 |
|---|---|---|
| 野菜によるγ-アミノ酪酸の蓄積 大野一仁、松長崇、 佐野和男 愛媛県工業系試験研究機関研究報告、 45、 20-34(2007) |
野菜中のGABA含量を測定するために温州ミカンで用いた「嫌気処理をせず低温化で処理する」方法を野菜に応用し、GABA生成能の高い野菜のスクリーニング、GABAの最適な生成条件、GABA生成酵素の特性を検討した。 | 前処理:73 %エタノールで抽出、乾固後クエン酸緩衝液で定容 測定:アミノ酸自動分析計(日立L-8500) |
| 市販大豆もやしの生育過程におけるγ-アミノ酪酸および遊離アミノ酸組成の変動 水野時子、山田幸二 日本食生活学会誌、 17(4)、 329-335(2007) |
大豆もやし生育過程における呈味成分や機能性成分としてのγ-アミノ酪酸及び遊離アミノ酸組成、併せて一般成分、脂質中の脂肪酸組成の変動を検討した。 | 前処理:1 %ピクリン酸溶液で抽出、乾固後クエン酸緩衝液で定容 測定:アミノ酸自動分析計(日立L-8500) |
| カンキツ果汁中のγ-アミノ酪酸とその富化 大野一仁、首藤喬一、 門家重治 果汁協会報、 582、 6-19(2007) |
各種果実17種のγ-アミノ酪酸を定量したところ、ウンシュウミカンが最高で、カンキツ果実に比較的多く含まれていた。 | 前処理:73 %エタノールで抽出、乾固後クエン酸緩衝液で定容 測定:アミノ酸自動分析計(日立L-8500) |
| 秋田酒こまちと蕎麦におけるγ-アミノ酪酸の分布 秋田県総合食品研究所報告、 7、 47-48(2005) |
酒造米「秋田酒こまち」の玄米とソバにおけるγ-アミノ酪酸含量分布を調べた。 | 前処理:0.1 N塩酸で抽出後ろ過 測定:アミノ酸自動分析計(日本電子JLC-500V) |
| 発芽玄米と籾発芽玄米のγ-アミノ酪酸及び遊離アミノ酸含量 大久保範、大能俊久、 森勝美 日本食品科学工学会誌、 50(7)、 316-318(2003) |
玄米、発芽玄米及び籾発芽玄米の遊離アミノ酸含量とγ-アミノ酪酸含量には正の相関(r=0.928)が認められた。 | 前処理:0.1 N塩酸で抽出後ろ過 測定:アミノ酸自動分析計(日本電子JLC-500V) |
| 嫌気-好気交互処理による茶葉のγ-アミノ酪酸の増加 沢井祐典、吉冨均、 山口優一、深山大介 日本食品科学工学会誌、 46(7)、 462-466(1999) |
茶葉において嫌気処理と好気を組み合わせることにより、GABA含量をより高めるための検討を行った。 | |
| エダマメ中のγ-アミノ酪酸含量の差異 阿部利徳、竹屋佳奈子、 日本食品科学工学会誌、 52(11)、 545-549(2005) |
エダマメ子実中のGABA含量の品種間差異、開花受精後のGABA含量の消長およびGABAを合成する酵素遺伝子、GADの発現の経時的変化等を調べ、エダマメ子実中のGABAについて明らかにした。 | 前処理:75 %エタノールで抽出、上清を減圧乾固。0.1 %TFA-アセトニトリル(1:1)に溶解してSEP-PAK C18で精製。50 mmolリン酸緩衝液(pH6.5):アセトニトリル(95:5)に溶解。 測定:HPLC |
| ジャガイモ及びその加工食品のγ-アミノ酪酸含量 中村和哉、奈良一寛、野口智紀ほか 日本食品科学工学会誌、 53(9)、 514-517(2006) |
前処理:75 %エタノールで抽出後ろ過。 測定:OPAで誘導体化後、HPLC カラム:ZORBAX Eclipse-AAA 移動相:40 mM NaH2PO4、ACN/MeOH/水(45:45:10)のグラジエント |
|
| Influence of processing on the generation of γ-aminobutyric acid in green coffee beans Gerhard Bytof, Sven-Erik Knopp, Peter Schieberle Eur. Food Res. Technol., 220, 245-250(2005) |
4 %スルホサリチル酸溶液で抽出後、遠心ろ過 測定:OPAで誘導体化後、HPLC(ODSカラム)、蛍光(ex.334 nm、em.425 nm) またはアミノ酸自動分析計を用いたニンヒドリン法 |
|
| Enzymatic polishing of rice - A new processing technology Mithu Das, Suneel Gupta, Vishal Kapoor, Rintu Banerjee Food Science and Technology, 41, 2079-2084(2008) |
HPTLC(詳細不明) | |
| Determination of Amines and Amino Acid in Wine PEKKA LEHTONEN Am.J.Enol.Vitic., 47(2), 127-133(1996) |
95 %エタノールで抽出、遠心後濃縮しカラム精製(Dowex 50W-X8)。 測定:アミノ酸自動分析計 |
|
| γ-Aminobutyric Acid Content of Selected Uncooked Foods Suk-Heung Oh, Yeon-Jong Moon, Chan-Ho Oh Nutraceuticals & Food, 8, 75-78(2003) |
メタノール:クロロホルム:水(12:5:3)を加えてかくはん。上清を除き水とクロロホルムを加えてかくはんし、上清を合わせ再度遠心後、上清を凍結乾燥し水に再度溶解。 測定:AQCで反応後HPLC(詳細不明) |
|
| Comparative Studies on Major Nutritional Components of Rice with a Giant Embryo and A Normal Embryo Linlin Zhang, Peisong Hu, Shaoqing Tang, Haijun Zhao, Dianxing Wu Journal of Food Biochemistry, 29, 653-661(2005) |
5 %トリクロロ酢酸で抽出後、遠心ろ過。pH2.2に調整後、クエン酸緩衝液で希釈 測定:HPLC(詳細不明) |
4)分析法に関する文献
1.イソフラボン類
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| Determination of total soy isoflavonea in dietary supplements, supplement ingredients, and soy foods by high-performance liquid chromatography with ultraviolet detection: collaborative study Collison, M. W. Journal of AOAC International, 91(3), 489-500(2008) |
HPLC-UVを用いた健康食品、健康食品素材及び大豆製品中の総イソフラボン量の測定。(室間コラボレーション) 6カ国の13機関でコラボを実施した。Repeatability(同一試験室間)及びRepuroducibility(異なる試験室間)の相対標準偏差はそれぞれ、400 mg/gを超えるサンプルでは1.07と2.29、0.87 mg/gのサンプルでは3.31と9.36であった。 HORRAT値は0.8 mg/gを含む全検体で1.00〜1.62に収まった(AOACのガイドラインでは0.5〜2.00が許容要囲)。 |
検体秤量後、内部標準物質(アピゲニン)を添加し、アセトニトリル-水-DMSO(58.5:39.0:2.5)を加えて1時間かくはん抽出。 カラムはODS系(250×3.0 mm、5 mm)などを使用。測定波長260 nm。カラム温度40 ℃。 移動相は40 %アセトニトリルとアセトニトリルのグラジエント。 計算方法は以下の2通り。 1.総イソフラボン量:12種のイソフラボン量を算出し、その合計量を求める。すなわち、アセチル化及びマロニル化配糖体は、対応する配糖体から分子量換算し求める。 2.アグリコン当量:配糖体をアグリコンに分子量換算し、その合計量を求める。 |
| Polyphenolic content in different plant parts of soy cultivars grown under natural conditions Romani, A., Vignolini, P. et al. J. Agric. Food Chem., 51, 5301-5306(2003) |
大豆の各部位におけるポリフェノール含量の調査。 イソフラボンは根に多いが、種類によっては葉や茎にも含まれる。 ケルセチン類縁体、ケンフェロール類縁体は葉に多く、根には含まれない。 また、豆の濃度については3品種での比較がされている。 |
遊離型を測定しているが、イソフラボンは3種のアグリコンとして測定(加水分解はしておらず、あくまで計算上のこと)。クメステロール類縁体もクメステロールとして測定。ケンフェロール類縁体及びケルセチン類縁体は、それぞれKaempferol 3-O-glucoside及びルチンとして測定。いずれも分子量換算で補正している。 70 %エタノール(pH2)で抽出し、HPLCで測定。ODS系カラムを使用。 |
| 大豆イソフラボンを含む特定保健用食品等の取扱いに関する指針について 平成18年食安発第0823001号 別紙「食品中の大豆イソフラボンアグリコン(アグリコン当量)の試験方法」 |
12種のイソフラボン標準品を用いてアグリコン、配糖体、アセチル体およびマロニル体の溶出位置を決定する。定量標準品はダイジン、ゲニスチン、グリシチン。 なお、醗酵食品に含有されているスクシニル体もイソフラボンに含めるため、通知法に添付されているクロマトグラム例から溶出位置を推定。 |
エタノール及び水の混液で抽出し、HPLCで測定。 カラム例:YMC-Pack ODS-AM AM12S05-2546WT、 4.6×250 mm 水-アセトニトリル-酢酸のグラジエント。 測定波長:254 nm、カラム温度:35 ℃、流速:1.0 ml/min。 |
2.カテキン類
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| 食品総合研究所 食品機能部 健全性評価研究室. "緑茶カテキン類のHPLCによる簡易・迅速分析". 独立行政法人 農業・食品産業技術総合研究機構 (オンライン)、 入手先 <http://www.nfri.affrc.go.jp/research/seika/seikah7/nfri95006.html>、 (参照2008-10-12) |
緑茶中に多く含まれるEGCgを中心に関連のカテキン類のHPLCによる分析法を開発した。 | 50 %アセトニトリルで抽出。 カラム:Develosil HG 4.6×150 mm 水-アセトニトリル-リン酸の混液とアセトニトリルのグラジエント(分析時間20分)。 測定項目:EC、EGC、ECg、EGCg、C、GC、Cg 、GCg、カフェイン 定量限界:2 ng、保持時間のCV:0.5 %以下、定量値CV:2.5 %以下、検量線範囲:2 ng〜2μg。(注入量不明、測定値等データ無し) |
| Simultaneous determination of catechins, caffeine and gallic acids in green, Oolong, black and pu-erh teas using HPLC with a photodiode array detector Zuo, Y., Chen, H. and Deng, Y. Talanta, 57, 307-316(2002) |
緑茶、ウーロン茶、紅茶、プーアール茶について、カテキン類、カフェイン、没食子酸の同時分析を行った。 | 試料1.9〜3.8 g採取後、80 %メタノールを20 ml加え3時間抽出。これを3回繰り返す。さらに0.15 %塩酸含有80 %メタノールを20 ml加え3時間抽出。これを2回繰り返す。全抽出液をろ過し、0.45μmフィルターを通した後、HPLCで測定。 カラム:Altech adsorbosil C18 水-酢酸(97:3)とメタノールのグラジエント 測定波長:280 nm |
| High-sensitive determination of catechins by high-performance liquid chromatography with electrochemical detection Miyashita N., Kotani A. and Kusu F. Analytical Sciences, 17, Supplement, a145-a148(2001) |
電気化学検出器を用いて、緑茶とウーロン茶についてカテキン類の分析を行った。 再現性や添加回収率は、良好であった。 |
液体試料と移動相を等量混合したものを1分間超音波照射し、フィルターろ過後HPLCで測定。 カラム:CAPCELL PAK C18 UG120 移動相は水-メタノール-リン酸(81:19:0.5)のアイソクラティック。 測定電位:600 mV |
| UV吸収スペクトルを用いた緑茶飲料中のガレート型カテキンの簡易定量 奥村寿子、一谷正己ほか 日本食品化学学会誌、 14(3)、 128-133(2007) |
緑茶に含まれる茶カテキンのうち、ガレート型は遊離型よりも優れた生理活性を有することが知られている。 水溶液のpHを中性から塩基性に変化させるとガレート型カテキンでUV吸収極大がシフトしたが、遊離型は変化しなかった。このスペクトルの変化を利用してガレート型カテキンの定量法を開発した。 |
<HPLC測定> カラム:Capcellpak 4.6×100 mm メタノール-0.5 %リン酸水溶液(18:82) 測定波長:280 nm <UVスペクトル測定> アルギニン水溶液を加え、322 nmにおける吸光度で検量線作成。 HPLC法とUVスペクトル法で、測定結果は良い一致を示した。 |
| セミミクロ高速液体クロマトグラフィーによる食品中のカテキン類及びメチルキサンチン類の定量 寺田久屋、鈴木晃世ほか 食品衛生誌、 33(4)、 347-354(1992) |
茶カテキンであるEGC、EGCg、ECg、C、ECとメチルキサンチン類のカフェイン、テオブロミン、テオフィリンを短時間に同時分析できる方法を検討した。 アイスクリーム、煎餅、ゼリー、飴など加工品でも回収率良好だった。 |
茶葉は40 %エタノールで超音波抽出。前処理にSep-pak C18を使用し、HPLCで測定。 カラム:Inertsil ODS-2 2.1×250 mm メタノール-水-0.2 Mリン酸水溶液(pH3.0)(12:33:5) 測定波長:207 nm 標準溶液:0.01 mg/ml |
3.フェノール酸(クロロゲン酸、フェルラ酸)
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| Analysis of phenmolic compounds in white rice, brown rice, and germinated brown rice Tian, S., Nakamura K. and Kayahara H. J. Agric. Food Chem., 52, 4808-4813(2004) |
白米、玄米、発芽玄米中におけるフェノール酸(フェルラ酸、p-クマル酸、クロロゲン酸、カフェイン酸など)を分析。遊離型及び総量について測定。 含量は、発芽玄米>玄米>白米 の順。 一例として、発芽玄米中のフェルラ酸量は、遊離型が0.28 mg/100g、総量が16.39 mg/100g。 |
遊離型は70 %エタノールで抽出後、HPLCで測定。 総量は1 mol/LのNaOHaqで加水分解後、HPLCで測定。 HPLCはODS系カラムを使用、測定波長は325 nm。 |
| Phenolic acids in berries, fruits, and beverages Mattila, P., Hellstrom, J. and Torronen R. J. Agric. Food Chem. 54, 7193-7199(2006) |
ベリー類、果物及び飲料中におけるフェノール酸(p-クマル酸、p-ヒドロキシ安息香酸、桂皮酸、没食子酸、フェルラ酸、カフェイン酸など)を分析。可溶性フェノール酸及び総フェノール酸について測定。 総量分析においては、カフェイン酸、フェルラ酸、p-クマル酸が多くのサンプルで検出された。 LODは可溶性フェノール酸が0.1 mg/100g、総フェノール酸が0.5 mg/100g。 |
試料秤量後、ブチル化ヒドロキシシラノール及び酢酸含有メタノールで抽出し、HPLCで測定(可溶性フェノール酸)。 残りの抽出液をアルカリ加水分解(NaOH溶液、20 ℃、16時間かくはん)した後、HClを加え酸性条件下で有機溶媒に転溶。HPLCで測定(総フェノール酸)。 カラム:Inertsil ODS-3、 150×4.0 mm、3μm 測定波長:329 nm(フェルラ酸、カフェイン酸、クロロゲン酸など)、280 nm(クマル酸)。 カラム温度:35 ℃。 50 mmol/Lリン酸緩衝液(pH2.5)とアセトニトリルのグラジエント。 流速:0.7 ml/min。 |
| Reversed-phase high-performance liquid chromatography determination of selected phenolic acids in propolis concentrates in terms of standarudization for drug manufacturing purposes Krzek, J., Kaleta, J. et al. Journal of AOAC International, 89(2), 352-358(2006) |
プロポリス中のフェノール酸のHPLC分析。 フェノール酸はカフェイン酸、p-クマル酸、フェルラ酸を測定。各々のLODはそれぞれ0.315、0.325、0.695 mg/mLであった。回収率はそれぞれ98.14、101.05、99.42 %、直線性の範囲はそれぞれ1.31〜99.18、1.52〜119.16、2.42〜184.14μg/mLであった。 Repeatability(同一試験室内)の相対標準偏差はそれぞれ2.27 %、1.69 %、1.54 %であった。 |
試料秤量後、メタノールで25 mLに定容。定容液を1 mL分取し、固相抽出カラム(LiChrolut RP18)で精製しHPLCで測定。 カラム:ODS系カラム(LiChrospere 100 RP18e、 250×4.0 mm、5 mm) 測定波長:320 nm、カラム温度:25 ℃ 0.03 mmol/Lリン酸二水素Na溶液(pH3.0)とアセトニトリルのグラジエント |
| Determination of phenolic acids in fruit juices by isocratic column liquid chromatography Amakura Y., Okada M. et al. Journal of Chromatography A, 891, 183-188(2000) |
ジュースのフェノール酸含量の調査。 ジュースはリンゴ、グレープ、ザクロ、プルーンの4種。クロロゲン酸、フェルラ酸、カフェイン酸などを定量。 クロロゲン酸はプルーンジュースで190 μg/g、リンゴジュースで16.6 μg/g。フェルラ酸はいずれも検出せず。カフェイン酸はグレープジュースで9.5 mg/g。 |
ジュースは弱酸性にした後、Sep-pak tC18及びBond Elut PSAに通して精製。HPLCにて測定。 カラムはL-column ODSを使用。 |
4.フラボノイド(フラボノール類、フラボン類、フラバノン類)
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| Spectorophotometric and coulometric detection in the high-performance liquid chromatography of flavonoids and optimization of sample treatment for the determination of quercetin in orange juice Careri, M., Elviri, L. et al. Journal of Chromatography A, 881, 449-460(2000) |
オレンジジュース中のフラボノイド配糖体の測定とフラボノイドアグリコンの測定。 フラボノイド配糖体:ケルセチン、アピゲニン、ケンフェロール、クリシン、ガランギン アグリコン(加水分解):エリオシトリン、ナリルチン、ナリンジン、ヘスペリジン、ネオヘスペリジン |
加水分解法:ジュース3.5 gにメタノール4 ml、12 mol/L HCl 1 ml、BHT 12 mgを加え(メタノール:水=1:1、BHT濃度が1500 mg/Lになるようにする)、加水分解(90 ℃、1時間還流)。冷却後メタノールを加えて10 mlとし5分間超音波抽出後、フィルターろ過しHPLCで測定。 配糖体の分析:ジュース1 gにメタノール3 mlと内標準物質を加え、30秒間かくはん後55 ℃で15分間加温。遠心分離(3150 G、15分)後、上澄み液分取。残留物をメタノール3 mlで再抽出。抽出液を合わせて水で10 mlに定容し、フィルターろ過後HPLCで測定。 カラム:C18カラム(Luna 150×2.0 mm、3 mm) pH2.4のギ酸水溶液とアセトニトリルのグラジエント 測定波長: 280 nm(フラバノン)、265nm(フラボン、フラボノール)、370nm(ケルセチン) |
| Simultaneous determination of all polyphenols in vegetables, fluits, and teas Sakakibara H, Honda Y. et al. J. Agric. Food Chem., 51, 571-581(2003) |
野菜、果物、茶中のポリフェノールの定量分析。 ほとんどのフラボノイド゙は配糖体と存在しているが、最も含量の多いアグリコンはケルセチンとケンフェロールであった。 にんじん、大根、ごぼう、ジャガイモの根菜類はポリフェノールの含有がわずかで、キャベツ、チャイブ(ネギ科)、レタス、ホウレン草などの葉野菜は配糖体としてフラボンとフラボノールを含有していた。葉野菜の中でも、セロリとパセリはペパーミント、セイジ、オレガノ、タイムなどのハーブ野菜に分類され、相対的に高いレベルで、アグリコン型でフラボンとフラボノールを含有していた。 |
粉砕後凍結乾燥したサンプル50 mgに内標準物質を添加し、0.5 %酢酸含有メタノール2 mlを加えて超音波照射1分+遠心分離(3000 r/min、10分)を4回実施。抽出液を遠心濃縮機で乾燥後、DMSO 0.5 mlに溶解してフィルターろ過。 HPLC条件:Capcel pak C18 UG120(250×4.6 mm、S-5、5 mm)、ガードカラム(10×4.0 mm)、カラム温度35 ℃。波長は200〜600 nm。50 mMリン酸ナトリウム(pH3.3)含有10 %メタノールと70 %メタノールのグラジエント分析。ポリフェノールのピークがアグリコン標準品の保持時間と一致しない試料については、加水分解したものについても測定し、クロマトグラムを比較した。 加水分解条件:粉末50 mg、0.5 mg/ml BHT含有62.5 %メタノール4 ml、2 N HCl 1 mlをゴム付き試験管にいれ、小さな穴を開けたゴム栓を締める。90 ℃で2時間加熱し、酢酸エチル10 mlに分配。酢酸エチル層をN2ガスで乾固後、DMSO 0.5 mlに溶解してフィルターろ過。 |
| Determination of flavonoids in plant material by HPLC with diode-array and electro-array detections Mattila, P., Astola, J. and Kumpulainen J. J. Agric. Food Chem., 48, 5834-5841(2000) |
リンゴンベリー、クランベリー、赤玉ねぎ、黄玉ねぎ、ブロッコリー、緑茶、紅茶、赤ワイン、リンゴ、レモン、オレンジ、パセリ中のフラボノイドの分析。 | お茶は浸出液、赤ワインはそのもの、その他は凍結乾燥物について分析。 凍結乾燥物は、試料0.5 gに2 g/Lの2、(3)- tert-butyl-4-hydroxyanisole(BHA)含有62.5 %メタノール40 mlを加えて分散させ超音波で5分間抽出。6 mol/L HCl 10 mlを加え約40〜60秒N2ガスを充填して密閉。90 ℃で2時間かくはんして加水分解後、冷却。ろ過後、メタノールで100 mlに定容し、5分間超音波照射。メンブランフィルター(0.2 mm)ろ過後HPLCで測定。 お茶の浸出液及び赤ワインは、試料15 mlに2 g/LのBHA含有62.5 %メタノール25 mlを加えて加水分解(4時間)。酢酸エチル分配後、測定。 |
| Simultaneous analysis of adrenergic amines and flavonoids in Citrus peel jams and fruit juices by liquid chromatography: part 2 Avula B., Upparapalli, S. K. and Khan, I. A. Journal of AOAC International, 90(3), 633-640(2007) |
柑橘系のジャム及びジュース中に含まれるアドレナリン作用のあるアミン類、フラボノイドのHPLC分析。 柑橘系果物から作られたジャム、ジュースに含まれるフラボノイド20種及びアドレナリン作用のあるアミン類6種の同時分析法を開発した。 調査の結果、フラボノイド及びアミン類の濃度範囲は広く、多くは果物種に依存していた。 また、この分析法は多くのサンプルの連続分析にも適用可能であった。 分析項目例(フラボノイド):ルチン、ナリルチン、ナリンジン、ヘスペリジン、ネオヘスペリジン、ナリンゲニン、ヘスペレチン |
ジャムは秤量後、メタノール-DMSO(1:1)を加え20分間超音波照射(2回繰り返す)後、上澄みを回収。さらに水で3回抽出し先液と合わせ試料溶液とする。 ジュースは10分間超音波照射し、遠心分離後の上澄みを試料溶液とする。 HPLC測定条件 カラム:ODS系カラム(Synergi Hydro-RP 80A、250×4.6 mm、4 mm) 測定波長:280 nm、カラム温度:30 ℃。 0.1 mol/L酢酸Na溶液(pH5.5)とアセトニトリルのグラジエント。 |
| 茶のフラボノールアグリコンおよびC-グルコシルフラボンの検索と定量 津志田藤二郎、松浦俊明ほか 茶業技術研究、 69、45-50(1986) |
茶についてフラボノール配糖体を全て加水分解しアグリコンとした後、定量。茶芽の採取時期による含量の差や品種間差異などを比較。 分析項目:ミリセチン、ケルセチン、ケンフェロール 内部標準物質:モリン ミリセチンとケルセチンは茶芽の生育に伴い増加したが、ケンフェロールは5月7日の採取以降減少した。 ほとんどの品種でケルセチンが最も多く、次いでケンフェロール、ミリセチンの順であった。 |
粉末500 mgをとり、25 %エタノール溶液約80 mlを加え、沸騰浴中に5分間入れた後、室温下で時々かくはんしながら約2時間抽出して100 mlに定容。遠心分離(2500 r/min、5分)して得た上澄み液10 mlを栓付き試験管に分取し、メルカプトエタノール0.2 ml、内部標準のモリン溶液(69.7 mg/100ml)0.2 ml、及び塩酸1 mlを加え加水分解。この液を酢酸エチル10 mlと振とうし、酢酸エチル層に転溶(3回繰り返す)。酢酸エチル抽出液を減圧濃縮乾固後メタノール5 mlに溶解し、HPLCで測定。 カラム:C18カラム(4.6×250 mm) 10 %アセトニトリル含有5 mMりん酸2水素Na(pH2.3)及び35 %アセトニトリル含有5 mMりん酸2水素Na(pH2.3)のグラジエント 流速:1.5 ml/min、測定波長:325 nm |
5.カロテノイド
| タイトル、著者名、出典 | 概要 | 分析条件等 |
|---|---|---|
| 食品中カロテノイド系色素の分析法開発と市販食品実態調査 林 智子ほか(愛知県食品衛生検査所) 食品衛生研究、 58(3) 55-60(2008) |
食品中のカロテノイド色素をケン化後の主生成物(オレンジ色素:β-クリプトキサンチン、トウガラシ色素:カプサンチン、マリーゴールド色素:ルテイン、トマト色素:リコペン)を指標物質として定量。 | 試料からカロテノイド色素をエーテルで抽出後、ケン化、C18固相抽出カートリッジで精製し、逆相HPLCで定量。 カラム:TOSOH TSKgel ODS-80Ts 5 μm(4.6×150 mm)及びMightysil RP-18GP 5μm(4.6×150 mm) 移動相:アセトニトリル-アセトン-ヘキサン(11:7:2)など5種類 検出波長:460 nm 市販食品を用いた添加回収試験(n=5)の結果は回収率73.9 %以上、変動係数10.7 %以下であった。 |
| 高速液体クロマトグフィーによる野菜のカロテノイドおよびクロロフィルの同時分析 満田幸恵ほか 日本食品科学工学会誌、 49(7)、 500-506(2002) |
野菜中のカロテノイド及びクロロフィルをアセトンで抽出し、ODSカラムを用い、グラジエント溶出法で定量した。 | カラム:ODS-80TS(4.6×250mm) 移動相:A アセトニトリル水(9:1)、B 酢酸エチル 0-20分 A 100 %-B 50 % 20-30分 B 50 % 従来の転溶操作を行う方法よりばらつきが少ない。 |
| Ultrasound-assisted methodを用いた卵黄からのルテイン改良抽出法 Yue, X., Xu, Z. J. Food Sci., 71(4),239-241 (2006) |
卵黄からのルテインの抽出について、けん化後ヘキサンを加えてVortexで抽出する方法(SOL)とヘキサンを加えて10分間超音波抽出法(UA-SOL)を比較し、後者がルテインを分解することなく高い値が得られることを示した。けん化時間も変化させて比較した。脂質やたんぱく質の多いサンプルに対してはUA-SOLが抽出力に優れていることを示した。(けん化で化学的にマトリクスを壊すより物理的に壊す方がルテインが安定である)(卵中のルテインは遊離体であるから) | 卵黄0.001 gを25 ml遠心管に取り、0.1 g/mlアスコルビン酸1 ml、10 %NaOH溶液を0〜0.6 mlまで変化させ、それに対応して0.6〜0 mlの水を加え60 ℃30分けん化。ヘキサン3 ml加えてVortex、遠心分離、分取を2回繰り返し、溶媒揮散させてMeOH1 mlに溶解。(SOL) ヘキサン3 ml加えた後超音波プローブを差込み10分間処理したのち遠心分離、分取、ヘキサン3 ml加え、超音波なしで1回抽出。溶媒揮散させてMeOH1 mlに溶解。(UA-SOL) HPLC条件;5C18、Discovery、4.6×250 mm、メタノール・アセトン(9:1)、0.8 ml/分、450 nm。 |
| 食品中のカロテノイドHPLC分析法の改良と評価及び英国における一般的野菜・果物中のカロテノイド含量 Hart, D. J., Scott, K. J. Food Chemistry, 54(1), 101-111(1995) |
果物・野菜中のカロテノイド含量測定法と英国における一般的野菜・果物中のカロテノイド含量を測定し示した。測定法では、移動相に加えるトリエチルアミンについて検討し、分析法のバリデーションデータを示した。 カロテノイド含量では、調理による変化を調べたが、ほとんどロスがなかった。 |
試料10 gに1 g炭酸Mg加え中和。THF:MEOH(1:1) 50 mlと内標(β-アポ-8'-カロテナール又はエキネノン)を加え1分間ホモジナイズ抽出。ろ過、抽出液で残さを洗い、分液漏斗に集めた。0.1 %BHT含有石油エーテル50 ml、10 %NaCl 50 ml加え振とう。計3回石油エーテルで抽出。35 ℃で濃縮、最終的にDCMで定容。必要ならばけん化操作を行う(コショウと果物のみ)。4 mlのDCM溶液に10 %KOH-MeOHを等量加え窒素下暗所室温で1時間けん化。0.1 %BHT含有石油エーテル20 ml、10 %NaCl 20 ml加え振とう。計3回石油エーテルで抽出。全有機溶媒層をpH が中性になるまで水洗。濃縮、DCM定容。 |
| DAD、APCI-MS付HPLC及びNMRによる加熱野菜中のルテイン、ゼアキサンチン立体異性体分析 Aman, R., Biehl, J. Food Chemistry, 92, 753-763(2005) |
HPLC-DADによりルテイン、ゼアキサンチンの立体異性体の同時分析条件を開発した。これにより、加熱工程での分解や異性化について評価した。 | |
| オリーブ油中のクロロフィル及びカロテノイドHPLC定量のための迅速定量抽出法 Mateos, R., Garcia-Mesa, J. A. Anal. Bioanal. Chem., 385, 1247-1254(2006) |
オリーブ油の色を左右する色素クロロフィルとカロテノイドの簡便な定量法を開発した。 | ジオールSPEカートリッジカラム(Supelco)をメタノール6 ml、ヘキサン6 mlでコンディショニングする。オリーブ油1 gを4 mlのヘキサンに溶解し、カラムに負荷。さらにヘキサン5 mlを流す。ヘキサンではカロテンが溶出する。次にアセトン3 mlで溶出。溶媒を揮散させて、再度アセトン0.3 ml定容。HPLC:Inertsil ODS 2、4.6×250 mm、A:メタノール・水(8:2) 0.025 %酢酸アンモニウム、0.05 %トリエチルアミン含有、B:メタノール・アセトン(1:1) グラジエント。446 nm。 |
| ルテイン:果実及び野菜中の有用な成分 MALTA MARIA CALVO Critical Reviews in Food Science and Nutrition, 45, 671-696(2005) |
ルテインの総説。分析法について多数の文献から集めたものをまとめている。HPLC条件が表にまとまっている。野菜、果実中の含量についても文献から抜粋して表になっている。その他、存在形態、生体に対する働きなど。 | |
| HPLC、UV-Vis、MSを組み合わせた天然カロテノイドのオンライン分析 眞岡孝至、秋元直茂、橋本圭二 Foods Food Ingredients J. Jpn., 208(8),623-630 (2003) |
LC/APCI-MS、LC/ESI-MS、LC/FAB-MS/MS、LC/UV-Vis、フォトダイオードアレー検出器とLC/APCI-MSの組み合わせの5種類の手法によりカロテノイドの分析を実施した。(カロテン、リコペン、ルテイン、ゼアキサンチン、カプサンチンなど) | パプリカに含まれるカロテノイドについてLC/FAB-MS/MSで検討した。また、フォトダイオードアレー検出器とLC/APCI-MSの組み合わせでトマトのカロテノイドの分析を実施、パプリカについて順相HPLC条件にてLC/APCI-MSの組み合わせで実施した。 |
| LC-ESI-MSによる魚卵中のカロテノイド及びall-trans-レチノールの測定 Hongxia Li, Selene T. Tyndale Journal of Chromatography B, 816, 49-56(2005) |
魚卵中のカロテノイド及びall-trans-レチノールをLC-ESI-MSにより測定。(β-カロテン、ルテイン、ゼアキサンチン、β-クリプトキサンチン、カンタキサンチン、アスタキサンチン) | Chinook salmon egg と鶏卵黄について実施。(抽出溶媒は氷冷)試料3-4 gにアセトン10 ml加え乳鉢で磨砕、vortex、これをさらに2回繰り返す。全アセトン抽出液にMtBEを等量及び水5 mlを加えて2層に分離。水層からさらに3回MtBEで抽出。溶媒留去し、MtBEに溶解して保管。 Finesse Genesis C18 column(150×2.1 mm)、メタノール・MtBE・水の割合を変化させたグラジエント溶出。 |
| 野菜加工品中のカロテノイド及びクロロフィルのクロマトグラフ分析 F. De Sio, L. Servillo Acta Alimentaria, 30(4), 395-405(2001) |
野菜及び野菜加工品中のカロテノイド(ルテイン、ゼアキサンチン、β-クリプトキサンチン、α-カロテン、β-カロテン、リコペン)及びクロロフィルをHPLCで分析した。C30カラムを用い、メタノール、水、ジクロロメタンのグラジエント溶出を採用した。この移動相は分離、分析時間の面で他の報告よりも優れていた。 | 試料(オレンジジュース、トマトピューレ、トマトペースト)からジクロロメタン・メタノール(2:1)で抽出、カロテノイドエステルでけん化が必要であれば10 %KOHメタノールを加え室温暗所で20時間けん化。10 %NaCl及びジエチルエーテルを加え転溶。水洗。溶媒留去。クロロホルムに溶解。YMC-Pack C30、250×4.6 mm、0.1 %BHT及び0.05 %TEA含有メタノール・水(95:5)、0.1 %BHT及び0.05 %TEA含有ジクロロメタンの2液でグラジエント。30 ℃、450 nm。 けん化、未けん化を比較したところ、トマトピューレ、トマトペーストでは同一であった。オレンジジュースやオレンジジュースベースの飲料ではルテインは100 %、ゼアキサンチンとβ-クリプトキサンチンは50 %増加した。 |
| C30カラムを用いたHPLC分析での植物カロテノイド分離に対する移動相組成の効果 Lei Li, Jian Qin Chromatographia, 65, 91-94(2007) |
植物中のルテイン、ゼアキサンチンのHPLCでの分離について、移動相組成を変化させて検討。 | Bischoff C30 カラム(3.0μm、3×150 mm)を用い、移動相A:メタノール・MtBE・水・酢酸アンモニウム(60:33:7:1.5)、B:(8:90:2:1)のグラジエントが最適であった。 |
| Determination of astaxanthin stereoisomers and colour attributes in flesh rainbow trout(Oncorhynchus mykiss) as a tool to distinguish the dietary pigmentation source V.M. Moretti Food Additives and Contaminants, 23(11), 1056-1063(2006) |
troutの履歴を知るために各部位の含量、立体構造との関連性を調べ、ツールとした。飼料の一つヘマトコッカス中の含量を測定するためにコレステロールエステラーゼによる分解を行った。 |
6.γ-アミノ酪酸
| タイトル、著者名、出典 | 概要 | 分析法 |
|---|---|---|
| 蛍光検出高速液体クロマトグラフィーによる搗精度の異なる米および飯中のγ-アミノ酪酸の分析 岩城啓子、松村羊子、 北田善三 日本調理科学会誌、 38(3)、 231-235(2005) | GABAの簡易な分析法として、フルオレスカミンにて蛍光誘導体化しHPLCで分析する方法を検討した。 | カラム:Cosmosil 5C18-MS�U 4.6×250 移動相:アセトニトリル-0.01 M酢酸緩衝液(pH6.6 30:70)に5 mM臭化テトラ-n-ブチルアンモニウムを含む。 GABA試料溶液(100μg/ml)100μlに対して0.2 Mホウ酸塩緩衝液(pH9.0)500 μlフルオレスカミン-アセトン溶液(3 mg/ml)200 μlのときに反応物が最も高率で生成した。 |
| イオンクロマトグラフィーによるギャバロン茶のγ-アミノ酪酸の定量法 山田嘉隆、沢井祐典 日本食品科学工学会誌、 49(3)、 188-194(2002) |
茶業界において着味茶、発色茶の鑑別のため使用されているIC法を利用してギャバロン茶のγ-アミノ酪酸を簡便に測定できる方法を開発した。 | 測定:イオンクロマトグラフ法 検量線の相関係数:0.999 7回繰り返し精度:CV 1.9 % 回収率:82-104 % |
| 市販大豆もやしの生育過程におけるγ-アミノ酪酸および遊離アミノ酸組成の変動 水野時子、山田幸二 日本食生活学会誌、 17(4)、 329-335(2007) |
大豆もやし生育過程における呈味成分や機能性成分としてのγ-アミノ酪酸及び遊離アミノ酸組成、併せて一般成分、脂質中の脂肪酸組成の変動を検討した。 | 前処理:1 %ピクリン酸溶液で抽出、乾固後クエン酸緩衝液で定容 測定:アミノ酸自動分析計(日立L-8500) |
| カンキツ果汁中のγ-アミノ酪酸とその富化 大野一仁、首藤喬一、 門家重治 果汁協会報、 582、 6-19(2007) |
各種果実17種のγ-アミノ酪酸を定量したところ、ウンシュウミカンが最高で、カンキツ果実に比較的多く含まれていた。 | 前処理:73 %エタノールで抽出、乾固後クエン酸緩衝液で定容 測定:アミノ酸自動分析計(日立L-8500) |
| Influence of processing on the generation of γ-aminobutyric acid in green coffee beans Gerhard Bytof, Sven-Erik Knopp, Peter Schieberle Eur. Food Res. Technol., 220, 245-250(2005) |
4 %スルホサリチル酸溶液で抽出後、遠心ろ過 測定:OPAで誘導体化後、HPLC(ODSカラム)、蛍光(ex.334 nm、em.425 nm) またはアミノ酸自動分析計を用いたニンヒドリン法 | |
| Determination of Amines and Amino Acid in Wine PEKKA LEHTONEN Am.J.Enol.Vitic., 47(2), 127-133(1996) |
95 %エタノールで抽出、遠心後濃縮しカラム精製(Dowex 50W-X8)。 測定:アミノ酸自動分析計 |
4.代表的な機能性成分の分析結果
1)機能性成分及び食品の選定
分析を行う機能性成分の選定は、栄養士会及び消費者へのアンケ‐ト結果、文献の調査結果、更に専門家の意見を参考とし、以下に示す10成分を選定した。
1.イソフラボン類
アグリコン総量及び個別12種のイソフラボン
2.カテキン類
(+)‐カテキン、エピカテキン、エピガロカテキンガレート、エピガロカテキン、エピカテキンガレート
3.フェルラ酸
フェルラ酸(加水分解処理)
4.クロロゲン酸
5‐カフェオイルキナ酸(5‐CQA)ならびに3‐CQA、4‐CQA及び5‐CQAの総量
5.フラボノ‐ル類
ケルセチン、ケンフェロール及びイソラムネチン(いずれも加水分解処理)、一部の食品につきルチン
6.フラボン類
アピゲニン及びルテオリン(いずれも加水分解処理)
7.フラバノン類
ヘスペレチン及びナリンゲニン(いずれも加水分解処理)、一部の食品につきヘスペリジン及びナリンジン
8.クルクミン
9.カロテノイド類
ルテイン、ゼアキサンチン、アスタキサンチン及びリコペン
10.γ‐アミノ酪酸
分析を行う食品の選定は、上記に加え五訂日本食品標準成分表(以下、五訂成分表と略す)の18分類のうち、選定した機能性成分が含まれる可能性が高いと推定された7分類(穀類、いも類、豆類、野菜類、魚介類、果実類及びし好飲料類)を中心に選定した。各分類の中で最低1品目は産地別または品種別の測定を行うため、3または5サンプルの分析を行った。
野菜については食品数が多いため、過去の国内生産量上位2食品については無条件で分析対象とした(ただし、明らかに含まれないと思われる成分は除外した)。
選定した食品及び分析項目は、表1‐15〜表1‐27に示した。また、試験部位は五訂成分表に合わせた。
試験にあたっては、以下に示す分析法の妥当性評価試験を行い、各評価基準を満たさなかったものは分析対象から除外した。
1.真度
検体に含まれる目的成分の2倍量を添加し、差し引き回収率を求めた。試験を行う主だった検体種ごとに行い、試行5回とした。その平均回収率(基準:70〜120%)で評価した。
2.併行精度
1.真度で得られた結果をもとに、相対標準偏差(基準:5%以内、ただし、加水分解操作を伴う試験法は10%以内)で評価した。
3.特異性
異なる分析条件で測定し、得られた結果の2条件の比(基準:±10%以内)で評価した。
4.検出限界及び定量限界の算出
検出限界は検出限界相当付近の標準溶液のS/N比が3をクリア、定量限界は定量限界相当付近の標準溶液のS/N比が10をクリアすることを評価基準とした。
表1‐15 穀類の品目及び分析項目
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | フェルラ酸 | フラボノ−ル | γ−アミノ酪酸 |
|---|---|---|---|---|---|---|---|
| CE−1 | こめ 白米 | 秋田県 | あきたこまち | 東京都 多摩市 | ● | − | − |
| CE−2 | こめ 白米 | 新潟県 | コシヒカリ | 東京都 多摩市 | ● | − | − |
| CE−3 | こめ 白米 | 山形県 | ササニシキ | 東京都 多摩市 | ● | − | − |
| CE−4 | こめ 白米 | 福島県 | ミルキ−クイ−ン | 東京都 多摩市 | ● | − | − |
| CE−5 | こめ 白米 | 宮城県 | ひとめぼれ | 東京都 多摩市 | ● | − | − |
| CE−6 | こめ 玄米 | 秋田県 | あきたこまち | 東京都 多摩市 | ● | − | ● |
| CE−7 | こめ 玄米 | 新潟県 | コシヒカリ | 東京都 多摩市 | ● | − | ● |
| CE−8 | こめ 玄米 | 山形県 | ササニシキ | 東京都 多摩市 | ● | − | ● |
| CE−9 | こめ 玄米 | 福島県 | ミルキ−クイ−ン | 東京都 多摩市 | ● | − | ● |
| CE−10 | こめ 玄米 | 宮城県 | ひとめぼれ | 東京都 多摩市 | ● | − | ● |
| CE−11 | こめ 発芽玄米 | 福岡県 | ヒノヒカリ | 東京都 多摩市 | ○ | − | ● |
| CE−12 | こめ 発芽玄米 | 茨城県 | ミルキ−クイ−ン | 東京都 多摩市 | − | − | ● |
| CE−13 | こめ 発芽玄米 | 秋田県 | あきたこまち | 東京都 東大和市 | − | − | ● |
| CE−14 | こむぎ 全粒粉 | 日本 | 不明 | 東京都 多摩市 | ○ | − | − |
| CE−15 | おおむぎ 押麦 | 日本 | 不明 | 東京都 多摩市 | ○ | − | − |
| CE−16 | そば そば粉 | 福井県 | 不明 | 東京都 豊島区 | ○ | ● | − |
| CE−17 | そば そば粉 | 北海道 | 不明 | 東京都 豊島区 | − | ● | − |
| CE−18 | そば そば粉 | 茨城県 | 不明 | 東京都 豊島区 | − | ● | − |
| CE−19 | そば 乾麺 | 日本 | 不明 | 神奈川県 相模原市 | ○ | ○ | − |
| CE−20 | あわ 精白粒 | 岩手県 | イ−ハト−ブ | 東京都 武蔵村山市 | ○ | − | − |
●:品種別の試験を実施
○:通常の試験を実施
−:分析対象外
表1‐16 いも類の品目及び分析項目
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | フェルラ酸 | クロロゲン酸 | γ−アミノ酪酸 |
|---|---|---|---|---|---|---|---|
| PO−1 | さつまいも 生 | 千葉県 | べにあずま | 東京都 町田市 | ○ | ○ | − |
| PO−2 | さといも 生 | 大分県 | 土垂れ | 東京都 町田市 | − | ○ | − |
| PO−3 | やまのいも 生 | 北海道 | ながいも | 東京都 町田市 | ○ | ○ | − |
| PO−4 | じゃがいも 生 | 北海道 | 男爵 | 東京都 町田市 | − | ○ | ● |
| PO−5 | じゃがいも 生 | 北海道 | メ−クイン | 東京都 町田市 | − | − | ● |
| PO−6 | じゃがいも 生 | 北海道 | メ−クイン | 東京都 町田市 | − | − | ● |
●:産地別の試験を実施
○:通常の試験を実施
−:分析対象外
表1‐17 豆類の品目及び分析項目
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | イソフラボン | カテキン | フラボノ−ル | γ−アミノ酪酸 |
|---|---|---|---|---|---|---|---|---|
| PU−1 | あずき 全粒、乾 | 茨城県 | 大納言 | 東京都 多摩市 | − | ○ | ○ | − |
| PU−2 | えんどう 全粒、乾 | 北海道 | 不明 | 神奈川県 横浜市 | − | ○ | ○ | − |
| PU−3 | ささげ 全粒、乾 | 茨城県 | 金時ささげ | 東京都 多摩市 | − | ○ | ○ | − |
| PU−4 | 豆腐 木綿 | 不明 | 不明 | 東京都 調布市 | ○ | − | − | − |
| PU−5 | 納豆 糸引き | 不明 | 丸大豆 | 東京都 調布市 | ○ | − | − | − |
| PU−6 | きな粉 | 北海道 | 不明 | 東京都 調布市 | ○ | − | − | − |
| PU−7 | 豆乳 | 不明 | 不明 | 東京都 調布市 | ○ | − | − | − |
| PU−8 | おから 全粒、乾 | 不明 | 不明 | 東京都 調布市 | ○ | − | − | − |
| PU−9 | だいず 全粒、乾 | 新潟県 | エンレイ大粒2等 | 東京都 中央区 | ● | − | − | ○ |
| PU−10 | だいず 全粒、乾 | 富山県 | エンレイ大粒3等 | 東京都 中央区 | ● | − | − | − |
| PU−11 | だいず 全粒、乾 | 石川県 | エンレイ大粒3等 | 東京都 中央区 | ● | − | − | − |
●:産地別の試験を実施
○:通常の試験を実施
−:分析対象外
表1‐18 野菜類の品目及び分析項目(1)
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | イソフラボン | カテキン | フェルラ酸 | クロロゲン酸 | フラボノール |
|---|---|---|---|---|---|---|---|---|---|
| VG−1 | キャベツ 生 | 愛知県 | 不明 | 東京都 多摩市 | − | ○ | ○ | ○ | ○ |
| VG−2 | たまねぎ 生 | 北海道 | 不明 | 東京都 多摩市 | − | ○ | ○ | ○ | ● |
| VG−3 | たまねぎ 生 | 静岡県 | 不明 | 東京都 町田市 | − | − | − | − | ● |
| VG−4 | たまねぎ 生 | 宮崎県 | 不明 | 神奈川県 横浜市 | − | − | − | − | ● |
| VG−5 | トマト 生 | 愛知県 | 不明 | 東京都 町田市 | − | ○ | ○ | ○ | ○ |
| VG−6 | トマト 生 | 福岡県 | 不明 | 東京都 町田市 | − | − | − | − | − |
| VG−7 | トマト 生 | 栃木県 | 不明 | 東京都 多摩市 | − | − | − | − | − |
| VG−8 | にんじん 根、生 | 千葉県 | 不明 | 東京都 多摩市 | − | ○ | ○ | ○ | ○ |
| VG−9 | なす 生 | 岡山県 | 不明 | 東京都 多摩市 | − | ○ | ○ | ● | ○ |
| VG−10 | なす 生 | 高知県 | 不明 | 東京都 町田市 | − | − | − | ● | − |
| VG−11 | なす 生 | 千葉県 | 不明 | 埼玉県 所沢市 | − | − | − | ● | − |
| VG−12 | ピーマン 青、生 | 高知県 | 不明 | 東京都 多摩市 | − | − | − | − | ○ |
| VG−13 | ほうれんそう 生 | 群馬県 | 不明 | 東京都 町田市 | − | − | ○ | − | ○ |
| VG−14 | ほうれんそう 生 | 岩手県 | 不明 | 東京都 町田市 | − | − | − | − | − |
| VG−15 | ほうれんそう 生 | 埼玉県 | 不明 | 東京都 町田市 | − | − | − | − | − |
| VG−16 | レタス 生 | 茨城県 | 不明 | 東京都 町田市 | − | − | − | − | ○ |
| VG−17 | ごぼう 根、生 | 青森県 | 不明 | 東京都 多摩市 | − | − | − | ● | − |
| VG−18 | ごぼう 根、生 | 鹿児島 | 不明 | 東京都 町田市 | − | − | − | ● | − |
| VG−19 | ごぼう 根、生 | 茨城県 | 不明 | 東京都 町田市 | − | − | − | ● | − |
| VG−20 | ケール 生 | 不明 | マイケール | インターネット | − | − | − | − | ○ |
●:産地別の試験を実施
○:通常の試験を実施
−:分析対象外
表1‐19 野菜類の品目及び分析項目(2)
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | イソフラボン | カテキン | フェルラ酸 | クロロゲン酸 | フラボノール |
|---|---|---|---|---|---|---|---|---|---|
| VG−21 | モロヘイヤ 生 | 沖縄県 | 不明 | 東京都 町田市 | − | − | − | ○ | ○ |
| VG−22 | パセリ 生 | 茨城県 | 不明 | 東京都 多摩市 | − | − | − | − | − |
| VG−23 | しそ 生 | 茨城県 | 不明 | 東京都 町田市 | − | − | − | − | ○ |
| VG−24 | セロリー 生 | 福岡県 | 不明 | 東京都 多摩市 | − | − | − | − | − |
| VG−25 | アスパラガス 生 | 佐賀県 | 不明 | 東京都 多摩市 | − | − | − | − | ○ |
| VG−26 | アスパラガス 生 | 長崎県 | 不明 | 東京都 東大和市 | − | − | − | − | − |
| VG−27 | アスパラガス 生 | 愛媛県 | ウェルカム | 東京都 多摩市 | − | − | − | − | − |
| VG−28 | きゅうり 生 | 栃木県 | ブルーム | 東京都 多摩市 | − | − | − | − | − |
| VG−29 | えだまめ 冷凍 | 台湾 | 不明 | 東京都 多摩市 | ○ | − | − | − | − |
| VG−30 | かぼちゃ 生 | 沖縄県 | えびす | 東京都 多摩市 | − | − | − | − | − |
| VG−31 | 金時人参 根、生 | 不明 | 不明 | インターネット | − | − | − | − | − |
●:産地別の試験を実施
○:通常の試験を実施
−:分析対象外
表1‐20 野菜類の品目及び分析項目(3)
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | フラボン | フラバノン | ルテイン/ゼアキサンチン | リコペン | γ−アミノ酪酸 |
|---|---|---|---|---|---|---|---|---|---|
| VG−1 | キャベツ 生 | 愛知県 | 不明 | 東京都 多摩市 | ○ | ○ | ○ | − | ○ |
| VG−2 | たまねぎ 生 | 北海道 | 不明 | 東京都 多摩市 | ○ | ○ | − | − | − |
| VG−3 | たまねぎ 生 | 静岡県 | 不明 | 東京都 町田市 | − | − | − | − | − |
| VG−4 | たまねぎ 生 | 宮崎県 | 不明 | 神奈川県 横浜市 | − | − | − | − | − |
| VG−5 | トマト 生 | 愛知県 | 不明 | 東京都 町田市 | ○ | ○ | ○ | ● | ● |
| VG−6 | トマト 生 | 福岡県 | 不明 | 東京都 町田市 | − | − | − | ● | ● |
| VG−7 | トマト 生 | 栃木県 | 不明 | 東京都 多摩市 | − | − | − | ● | ● |
| VG−8 | にんじん 根、生 | 千葉県 | 不明 | 東京都 多摩市 | ○ | ○ | ○ | − | ○ |
| VG−9 | なす 生 | 岡山県 | 不明 | 東京都 多摩市 | ○ | ○ | − | − | − |
| VG−10 | なす 生 | 高知県 | 不明 | 東京都 町田市 | − | − | − | − | − |
| VG−11 | なす 生 | 千葉県 | 不明 | 埼玉県 所沢市 | − | − | − | − | − |
| VG−12 | ピーマン 青、生 | 高知県 | 不明 | 東京都 多摩市 | ○ | ○ | ○ | − | − |
| VG−13 | ほうれんそう 生 | 群馬県 | 不明 | 東京都 町田市 | ○ | ○ | ● | − | − |
| VG−14 | ほうれんそう 生 | 岩手県 | 不明 | 東京都 町田市 | − | − | ● | − | − |
| VG−15 | ほうれんそう 生 | 埼玉県 | 不明 | 東京都 町田市 | − | − | ● | − | − |
| VG−16 | レタス 生 | 茨城県 | 不明 | 東京都 町田市 | ○ | − | ○ | − | ○ |
| VG−17 | ごぼう 根、生 | 青森県 | 不明 | 東京都 多摩市 | − | − | − | − | − |
| VG−18 | ごぼう 根、生 | 鹿児島 | 不明 | 東京都 町田市 | − | − | − | − | − |
| VG−19 | ごぼう 根、生 | 茨城県 | 不明 | 東京都 町田市 | − | − | − | − | − |
| VG−20 | ケール 生 | 不明 | マイケール | インターネット | − | − | − | − | − |
●:産地別の試験を実施
○:通常の試験を実施
−:分析対象外
表1‐21 野菜類の品目及び分析項目(4)
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | フラボン | フラバノン | ルテイン/ゼアキサンチン | リコペン | γ−アミノ酪酸 |
|---|---|---|---|---|---|---|---|---|---|
| VG−21 | モロヘイヤ 生 | 沖縄県 | 不明 | 東京都 町田市 | − | − | − | − | − |
| VG−22 | パセリ 生 | 茨城県 | 不明 | 東京都 多摩市 | ○ | − | − | − | − |
| VG−23 | しそ 生 | 茨城県 | 不明 | 東京都 町田市 | ○ | − | − | − | − |
| VG−24 | セロリー 生 | 福岡県 | 不明 | 東京都 多摩市 | ○ | − | − | − | − |
| VG−25 | アスパラガス 生 | 佐賀県 | 不明 | 東京都 多摩市 | ○ | − | − | − | ● |
| VG−26 | アスパラガス 生 | 長崎県 | 不明 | 東京都 東大和市 | − | − | − | − | ● |
| VG−27 | アスパラガス 生 | 愛媛県 | ウェルカム | 東京都 多摩市 | − | − | − | − | ● |
| VG−28 | きゅうり 生 | 栃木県 | ブルーム | 東京都 多摩市 | ○ | − | − | − | − |
| VG−29 | えだまめ 冷凍 | 台湾 | 不明 | 東京都 多摩市 | − | − | ○ | − | − |
| VG−30 | かぼちゃ 生 | 沖縄県 | えびす | 東京都 多摩市 | − | − | ○ | − | ○ |
| VG−31 | 金時人参 根、生 | 不明 | 不明 | インターネット | − | − | ○ | ○ | − |
●:産地別の試験を実施
○:通常の試験を実施
−:分析対象外
注:フラバノン類のヘスペレチン及びナリンゲニンは、妥当性評価試験において回収率が基準を下回ったため、測定対象外とした。
表1‐22 魚介類の品目及び分析項目
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | アスタキサンチン |
|---|---|---|---|---|---|
| FS−1 | えび 生、殻つき | 静岡県 | 桜海老、釜揚げ | 東京都 多摩市 | ○ |
| FS−2 | しろさけ イクラ | 北海道 | 不明 | 東京都 八王子市 | ○ |
| FS−3 | ぎんざけ | チリ | 不明 | 東京都 多摩市 | ● |
| FS−4 | べにざけ | アメリカ | 不明 | 東京都 多摩市 | ● |
| FS−5 | しろさけ | ロシア | 不明 | 東京都 多摩市 | ● |
●:産地別の試験を実施
○:通常の試験を実施
表1‐23 果実類の品目及び分析項目(1)
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | カテキン | フェルラ酸 | クロロゲン酸 | フラボノール | フラボン |
|---|---|---|---|---|---|---|---|---|---|
| FR−1 | うんしゅうみかん 生 | 静岡県 | 青島 | 東京都 多摩市 | − | ○ | ○ | ○ | ○ |
| FR−2 | うんしゅうみかん 生 | 福岡県 | 不明 | 東京都 多摩市 | − | − | − | − | − |
| FR−3 | うんしゅうみかん 生 | 徳島県 | 十万みかん | 東京都 町田市 | − | − | − | − | − |
| FR−4 | りんご 生 | 青森県 | ふじ | 東京都 多摩市 | ○ | ○ | ○ | ○ | ○ |
| FR−5 | いちご 生 | 栃木県 | とちおとめ | 東京都 多摩市 | ○ | − | − | − | − |
| FR−6 | いよかん 生 | 愛媛県 | 宮内いよかん | 東京都 多摩市 | − | − | − | − | − |
| FR−7 | バレンシアオレンジ 生 | オーストラリア | バレンシア | 東京都 多摩市 | − | − | − | − | − |
| FR−8 | グレープフルーツ ルビー 生 |
アメリカ | ルビー | 東京都 多摩市 | − | − | − | − | − |
| FR−9 | レモン 生 | 愛媛県 | メイヤー | 東京都 多摩市 | − | − | − | − | − |
| FR−10 | ゆず 生、皮 | 高知県 | 不明 | 東京都八王子市 | − | − | − | − | − |
| FR−11 | ゆず 生、果汁 | FR-10と同じ | FR-10と同じ | FR-10と同じ | − | − | − | − | − |
| FR−12 | かき 熟、生 | 福岡県 | 富有 | 東京都 多摩市 | − | − | − | − | − |
| FR−13 | プルーン 乾 | アメリカ | 不明 | 東京都 多摩市 | ○ | − | ○ | − | − |
| FR−14 | ブルーベリー 生 | チリ | ブギータ | 東京都 多摩市 | ○ | − | ○ | ○ | − |
| FR−15 | すいか 生 | 群馬県 | ひとりじめ | 東京都 多摩市 | − | − | − | − | − |
| FR−16 | バナナ 生 | フィリピン | キャベンディッシュ | 東京都 多摩市 | − | − | − | − | − |
| FR−17 | メロン 生 | 静岡県 | アールスフェボリット | 東京都 多摩市 | − | − | − | − | − |
| FR−18 | パパイヤ 生 | 宮崎県 | サンライズ・ ソロ | 東京都 立川市 | − | − | − | − | − |
○:通常の試験を実施
−:分析対象外
表1‐24 果実類の品目及び分析項目(2)
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | フラバノン | ルテイン/ゼアキサンチン | リコペン | γ−アミノ酪酸 |
|---|---|---|---|---|---|---|---|---|
| FR−1 | うんしゅうみかん 生 | 静岡県 | 青島 | 東京都 多摩市 | ● | − | − | ○ |
| FR−2 | うんしゅうみかん 生 | 福岡県 | 不明 | 東京都 多摩市 | ● | − | − | − |
| FR−3 | うんしゅうみかん 生 | 徳島県 | 十万みかん | 東京都 町田市 | ● | − | − | − |
| FR−4 | りんご 生 | 青森県 | ふじ | 東京都 多摩市 | ○ | − | − | − |
| FR−5 | いちご 生 | 栃木県 | とちおとめ | 東京都 多摩市 | − | − | − | ○ |
| FR−6 | いよかん 生 | 愛媛県 | 宮内いよかん | 東京都 多摩市 | ○ | − | − | − |
| FR−7 | バレンシアオレンジ 生 | オーストラリア | バレンシア | 東京都 多摩市 | ○ | − | − | − |
| FR−8 | グレープフルーツ ルビー 生 |
アメリカ | ルビー | 東京都 多摩市 | ○ | − | ○ | − |
| FR−9 | レモン 生 | 愛媛県 | メイヤー | 東京都 多摩市 | ○ | − | − | − |
| FR−10 | ゆず 生、皮 | 高知県 | 不明 | 東京都 八王子市 | ○ | − | − | − |
| FR−11 | ゆず 生、果汁 | FR-10と同じ | FR-10と同じ | FR-10と同じ | ○ | − | − | − |
| FR−12 | かき 熟、生 | 福岡県 | 富有 | 東京都 多摩市 | − | ○ | ○ | − |
| FR−13 | プルーン 乾 | アメリカ | 不明 | 東京都 多摩市 | − | − | − | − |
| FR−14 | ブルーベリー 生 | チリ | ブギータ | 東京都 多摩市 | − | − | − | − |
| FR−15 | すいか 生 | 群馬県 | ひとりじめ | 東京都 多摩市 | − | − | ○ | − |
| FR−16 | バナナ 生 | フィリピン | キャベンディッシュ | 東京都 多摩市 | − | − | − | ○ |
| FR−17 | メロン 生 | 静岡県 | アールスフェボリット | 東京都 多摩市 | − | − | − | ○ |
| FR−18 | パパイヤ 生 | 宮崎県 | サンライズ・ソロ | 東京都 立川市 | − | ○ | ○ | ○ |
○:通常の試験を実施
−:分析対象外
注:フラバノン類のヘスペレチン及びナリンゲニンは、妥当性評価試験において回収率が基準を下回ったため、測定対象外とした。
表1‐25 し好飲料類の品目及び分析項目(1)
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | カテキン | フェルラ酸 | クロロゲン酸 | フラボノール |
|---|---|---|---|---|---|---|---|---|
| BV−1 | せん茶 茶 | 静岡県 | やぶきた | 東京都 多摩市 | ● | ○ | ○ | ○ |
| BV−2 | せん茶 茶 | 京都府 | やぶきた | 東京都 多摩市 | ● | − | − | − |
| BV−3 | せん茶 茶 | 福岡県 | やぶきた | 東京都 多摩市 | ● | − | − | − |
| BV−4 | せん茶 浸出液 | BV-1と同じ | BV-1と同じ | BV-1と同じ | ● | ○ | ○ | ○ |
| BV−5 | せん茶 浸出液 | BV-2と同じ | BV-2と同じ | BV-2と同じ | ● | − | − | − |
| BV−6 | せん茶 浸出液 | BV-3と同じ | BV-3と同じ | BV-3と同じ | ● | − | − | − |
| BV−7 | ウーロン茶 茶 | 中国 | 不明 | 東京都 多摩市 | ○ | − | − | − |
| BV−8 | ウーロン茶 浸出液 | BV-7と同じ | BV-7と同じ | BV-7と同じ | ○ | ○ | ○ | ○ |
| BV−9 | 紅茶 茶 | スリランカ | セイロン | 東京都 多摩市 | ○ | − | − | − |
| BV−10 | 紅茶 浸出液 | BV-9と同じ | BV-9と同じ | BV-9と同じ | ○ | ○ | ○ | ○ |
| BV−11 | コーヒー 豆 | ブラジル、メキシコ、コロンビア | 不明 | 東京都 多摩市 | − | ○ | ○ | − |
| BV−12 | コーヒー 浸出液 | BV-11と同じ | BV-11と同じ | BV-11と同じ | − | ○ | ○ | − |
| BV−13 | コーヒー インスタント | エチオピア、コロンビア他 | モカ | 東京都 多摩市 | − | ○ | ○ | − |
| BV−14 | ココア ピュアココア | オランダ | 不明 | 東京都 多摩市 | ○ | − | − | − |
●:産地別の試験を実施
○:通常の試験を実施
−:分析対象外
表1‐26 し好飲料類の品目及び分析項目(2)
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | フラボン | フラバノン | ルテイン/ゼアキサンチン |
|---|---|---|---|---|---|---|---|
| BV−1 | せん茶 茶 | 静岡県 | やぶきた | 東京都 多摩市 | ○ | ○ | ○ |
| BV−2 | せん茶 茶 | 京都府 | やぶきた | 東京都 多摩市 | − | − | − |
| BV−3 | せん茶 茶 | 福岡県 | やぶきた | 東京都 多摩市 | − | − | − |
| BV−4 | せん茶 浸出液 | BV-1と同じ | BV-1と同じ | BV-1と同じ | ○ | ○ | − |
| BV−5 | せん茶 浸出液 | BV-2と同じ | BV-2と同じ | BV-2と同じ | − | − | − |
| BV−6 | せん茶 浸出液 | BV-3と同じ | BV-3と同じ | BV-3と同じ | − | − | − |
| BV−7 | ウーロン茶 茶 | 中国 | 不明 | 東京都 多摩市 | − | − | − |
| BV−8 | ウーロン茶 浸出液 | BV-7と同じ | BV-7と同じ | BV-7と同じ | ○ | ○ | − |
| BV−9 | 紅茶 茶 | スリランカ | セイロン | 東京都 多摩市 | − | − | − |
| BV−10 | 紅茶 浸出液 | BV-9と同じ | BV-9と同じ | BV-9と同じ | ○ | ○ | − |
| BV−11 | コーヒー 豆 | ブラジル、メキシコ、コロンビア | 不明 | 東京都 多摩市 | − | − | − |
| BV−12 | コーヒー 浸出液 | BV-11と同じ | BV-11と同じ | BV-11と同じ | − | − | − |
| BV−13 | コーヒー インスタント | エチオピア、コロンビア他 | モカ | 東京都 多摩市 | − | − | − |
| BV−14 | ココア ピュアココア | オランダ | 不明 | 東京都 多摩市 | − | − | − |
○:通常の試験を実施
−:分析対象外
表1‐27 その他の品目及び分析項目
| 識別 番号 |
食品名 | 産地 | 品種 | 購入地域 | イソフラボン | クルクミン |
|---|---|---|---|---|---|---|
| OT−1 | くず粉 乾、粉末 | 不明 | 不明 | 東京都 調布 | ○ | − |
| OT−2 | カレー カレー粉 | 不明 | 不明 | 東京都 多摩市 | − | ○ |
| OT−3 | カレー カレールー | 不明 | 不明 | 東京都 多摩市 | − | ○ |
| OT−4 | 秋うこん 乾、粉末 | インド | 秋ウコン | 神奈川県 横浜市 | − | ● |
| OT−5 | 春うこん 乾、粉末 | 鹿児島 | 春ウコン | インターネット | − | ● |
| OT−6 | 黒うこん 乾、粉末 | 鹿児島 | ガジュツ | インターネット | − | ● |
●:産地別の試験を実施
○:通常の試験を実施
−:分析対象外
2)分析結果
1.分析方法
a)イソフラボン類
試験は「大豆イソフラボンを含む特定保健用食品等の取り扱いに関する指針について(平成17年食安発第0823001号)別紙〔試験法〕」によって行った。すなわち、固体およびペースト状の試料の場合は、均一に粉砕もしくは混合した後、0.5〜5 g採取し、70%エタノール25 mlを加え5分間超音波処理した後、30分間かくはんした。次に遠心分離(2500 r/min、5分間)を行い、上澄み液を回収した。残さには70%エタノール25 mlを加え、30分間かくはんし遠心分離(2500 r/min、5分間)後上澄み液を回収し、先の抽出液と合わせた。再度、同様の操作を行い、3回分の抽出液を合わせた後、70%エタノールで100 mlに定容し、メンブランフィルター(マイレクスLH 親水性PTFE[日本ミリポア株式会社])に通したものを試料溶液とした。
液状検体の場合は、10〜30 gを分取後、70%エタノールで100 mlに定容し、メンブランフィルター(マイレクスLH 親水性PTFE[日本ミリポア株式会社])に通したものを試料溶液とした。
別にダイジン、グリシチン及びゲニスチン標準品を精密にはかり、70%エタノール溶液を用いて20μg/mlとなるように調製し、これを定量用標準溶液とした。別途、その他の9種のイソフラボン類(ダイゼイン、グリシテイン、ゲニステイン、アセチルダイジン、アセチルグリシチン、アセチルゲニスチン、マロニルダイジン、マロニルグリシリン及びマロニルゲニスチン)の定性用標準溶液を調製した。
試料溶液及び標準溶液10μlをHPLCに注入し、イソフラボンアグリコン量及び各イソフラボン量を求めた。納豆については、サクシニル体のイソフラボン類3種(サクシニルダイジン、サクシニルグリシチン及びサクシニルゲニスチン)が存在するため、これら3種のイソフラボン類についても結果に考慮した。
<高速液体クロマトグラフ操作条件>
条件1.(定量用)
機 種:LC‐20AD [株式会社 島津製作所]
検 出 器:紫外可視分光光度計 SPD‐20A [株式会社 島津製作所]
カ ラ ム:YMC‐Pack ODS‐AM AM12S05‐2546WT、φ4.6 mm×25 cm [株式会社 ワイエムシィ]
移 動 相:A液及びB液のリニアグラジエント
| A液 | B液 | |
|---|---|---|
| 0分 | 100% | 0% |
| 50分 | 0% | 100% |
| 50.1分 | 100% | 0% |
A液;水、アセトニトリル及び酢酸の混液(85:15:0.1)
B液;水、アセトニトリル及び酢酸の混液(65:35:0.1)
カラム温度:35 ℃
測定波長:254 nm
流 量:1.0 ml/min
注 入 量:10 μl
条件2.(特異性確認用)
機 種:LC‐20AD [株式会社 島津製作所]
検 出 器:紫外可視分光光度計 SPD‐20A [株式会社 島津製作所]
カ ラ ム:Unison UK‐C18、φ4.6 mm×25 cm [インタクト株式会社]
移 動 相:A液及びB液のリニアグラジエント
| A液 | B液 | |
|---|---|---|
| 0分 | 88% | 12% |
| 13分 | 77% | 23% |
| 30分 | 53% | 47% |
| 30.1分 | 88% | 12% |
A液;2.5%酢酸
B液;アセトニトリル
カラム温度:50 ℃
測定波長:254 nm
流 量:1.0 ml/min
注 入 量:10 μl
b)カテキン類
粉末試料においては試料を0.1〜4 g採取し、メタノール及びシュウ酸水溶液の混液(8:2)30 mlを加え10分間振とう抽出した。次に遠心分離を行い、上澄みを回収した。残さにはメタノール及びシュウ酸水溶液の混液(8:2)30 mlを加え、同様の操作を行った。再度、残さにメタノール及びシュウ酸水溶液の混液(8:2)20 mlを加え同様の操作を行い、3回分の抽出液を合わせた後、メタノール及びシュウ酸水溶液の混液(8:2)で100 mlに定容した。必要に応じ適宜希釈した後、メンブランフィルター(マイショリディスクW‐25‐5[東ソー株式会社])を通したものを試料溶液とした。
液体試料においては試料を1.0〜2 g採取し、1 mg/mlシュウ酸水溶液2 ml、水1〜2 ml及びメタノールを適量加え超音波照射を5分間行い、メタノールで20 mlに定容した。必要に応じ適宜希釈した後、メンブランフィルター(マイショリディスクW‐25‐5[東ソー株式会社])を通したものを試料溶液とした。
別に(+)‐カテキン、エピカテキン、エピガロカテキンガレート、エピガロカテキン及びエピカテキンガレート標準品を精密にはかりとってメタノールに溶解し、メタノール及びシュウ酸水溶液の混液(8:2)を用いて適宜希釈し、標準溶液を調製した。
試料溶液及び標準溶液をHPLCに注入し、各カテキン類の含量を求めた。せん茶、ウーロン茶及び紅茶については、5種類のカテキン類を測定した。茶以外の食品については、(+)‐カテキン及びエピカテキンを測定した。
<高速液体クロマトグラフ操作条件>
(+)‐カテキン及びエピカテキン
条件1.(定量用)
機 種:LC‐20AD [株式会社 島津製作所]
検 出 器:蛍光分光光度計 RF‐10AXL [株式会社 島津製作所]
カ ラ ム:YMC‐Pack ODS‐A AA12S05‐1506WT、φ6.0 mm×15 cm [株式会社 ワイエムシィ]
移 動 相:水、メタノール及び酢酸の混液(85:15:1)
カラム温度:40 ℃
蛍光励起波長:280 nm
蛍光測定波長:310 nm
流 量:1.0 ml/min
注 入 量:10 μl
条件2.(特異性確認用)
機 種:LC‐20AD [株式会社 島津製作所]
検 出 器:蛍光分光光度計 RF‐10AXL [株式会社 島津製作所]
カ ラ ム:YMC‐Pack ODS‐A AA12S05‐1506WT、φ6.0 mm×15 cm [株式会社 ワイエムシィ]
移 動 相:水、アセトニトリル及び2‐プロパノールの混液(200:25:2)
ただし0.4%クエン酸含有
カラム温度:25 ℃
蛍光励起波長:280 nm
蛍光測定波長:310 nm
流 量:1.0 ml/min
注 入 量:10 μl
エピガロカテキンガレート(定量用、条件1.)、エピガロカテキン及びエピカテキンガレート
機 種:LC‐10ADvp [株式会社 島津製作所]
検 出 器:紫外可視吸光光度計 SPD‐10AVvp [株式会社 島津製作所]
カ ラ ム:YMC‐Pack ODS‐A AA12S05‐1506WT、φ6.0 mm×15 cm [株式会社 ワイエムシィ]
移 動 相:水、メタノール及び0.02 mol/lリン酸緩衝液(pH3.0)の混液(33:12:5)
カラム温度:40 ℃
測定波長:270 nm
流 量:1.0 ml/min
注 入 量:5 μl
<液体クロマトグラフ‐タンデム型質量分析計操作条件>
エピガロカテキンガレート(特異性確認用、条件2.)及びエピガロカテキン
機 種:LC部;Alliance 2695 [Waters Corporation]
検 出 器:MS部;Quattro micro [Waters Corporation]
カ ラ ム:Atlantis T3、φ2.1 mm×15 cm [Waters Corporation]
移 動 相:水、アセトニトリル及び5%酢酸溶液のリニアグラジエント
| A液 | B液 | C液 | |
|---|---|---|---|
| 0分 | 55% | 5% | 40% |
| 10分 | 48% | 12% | 40% |
| 20分 | 0% | 60% | 40% |
| 23分 | 55% | 5% | 40% |
A液;水
B液;アセトニトリル
C液;5%酢酸
カラム温度:40 ℃
流 量:0.3 ml/min
カラム温度:40 ℃
イオン化法:エレクトロスプレー(正イオン検出モード)
設定イオン数:m/z 459.1→139.0(エピガロカテキンガレート)
m/z 306.9→138.9(エピガロカテキン)
c)フェルラ酸
試料を0.5〜2 g採取し、水を少量加えてなじませた後、1 mol/l水酸化ナトリウム溶液を50 ml加え、穏やかに振とうしながら40 ℃で3時間、加水分解を行った。2 mol/l塩酸溶液を約28 ml加え、pH試験紙で酸性であることを確認した。約5分間水冷した後、酢酸エチル50 mlを加え5分間振とう抽出を行った。遠心分離を行い、上層(酢酸エチル層)をナス型フラスコに分取し、下層(水層)に、再度酢酸エチル50 mlを加え同様の操作を2回行った。3回分の上層を集め、無水硫酸ナトリウムを用いて脱水ろ過し、エバポレーターを用いて減圧乾固した。メタノール及び水の混液(1:1)で溶解した後、メンブランフィルター(マイショリディスクW‐25‐5[東ソー株式会社])を通したものを試料溶液とした。
別にフェルラ酸標準品を精密にはかり、メタノール及び水の混液(1:1)を用いて溶解後、適宜希釈し、標準溶液を調製した。
試料溶液及び標準溶液をHPLCに注入し、フェルラ酸の含量を求めた。
<高速液体クロマトグラフ操作条件>
条件1.(定量用)
機 種:LC‐10AD [株式会社 島津製作所]
検 出 器:紫外可視吸光光度計 SPD‐10AV [株式会社 島津製作所]
カ ラ ム:YMC‐Pack ODS‐A AA12S05‐1506WT、φ6.0 mm×15 cm [株式会社 ワイエムシィ]
移 動 相:2.5%酢酸及びアセトニトリルの混液(88:12)
カラム温度:40 ℃
測定波長:320 nm
流 量:1.0 ml/min
注 入 量:10 μl
条件2.(特異性確認用)
機 種:LC‐10AD [株式会社 島津製作所]
検 出 器:紫外可視吸光光度計 SPD‐10AV[株式会社 島津製作所]
カ ラ ム:COSMOSIL 3C18‐AR‐Ⅱ、φ4.6 mm×10 cm [株式会社 ワイエムシィ]
移 動 相:2.5%酢酸、2‐プロパノール、アセトニトリル及びメタノールの混液(90:5:3:1)
カラム温度:40 ℃
測定波長:320 nm
流 量:1.0 ml/min
注 入 量:10 μl
d)クロロゲン酸
固体試料の場合は均一に粉砕もしくは混合した後、2.5〜8 g採取し、0.02 mol/l過塩素酸及びメタノールの混液(9:1)60 mlを加え10分間振とう抽出した。次に遠心分離を行い、上澄みを回収した。残さに0.02 mol/l過塩素酸及びメタノールの混液(9:1)60 mlを加え同様の操作を行った。再度、残さに0.02 mol/l過塩素酸及びメタノールの混液(9:1)50 mlを加え同様の操作を行い、3回分の抽出液を合わせた後、0.02 mol/l過塩素酸及びメタノールの混液(9:1)で250 mlに定容した。必要に応じて適宜希釈した後、メンブランフィルター(マイショリディスクW‐25‐5[東ソー株式会社])を通したものを試料溶液とした。
液状試料の場合は、1〜2 gを分取後、0.02 mol/l過塩素酸及びメタノール(9:1)で20 mlに定容した。必要に応じて適宜希釈した後、 メンブランフィルター(マイショリディスクW‐25‐5[東ソー株式会社])を通したものを試料溶液とした。
別に5‐カフェオイルキナ酸標準品を精密にはかり、0.02 mol/l過塩素酸及びメタノールを用いて適宜希釈し、標準溶液を調製した。
試料溶液及び標準溶液をHPLCに注入し、5‐カフェオイルキナ酸の含量及び総クロロゲン酸量(3‐カフェオイルキナ酸、4‐カフェオイルキナ酸及び5‐カフェオイルキナ酸を5‐カフェオイルキナ酸換算し合計したもの)を求めた。
<高速液体クロマトグラフ操作条件>
条件1.(定量用)
機 種:LC‐2010CHT [株式会社 島津製作所]
カ ラ ム:Cadenza CD‐C18、φ4.6 mm×15 cm [インタクト株式会社]
移 動 相:A液及びB液のリニアグラジエント
| A液 | B液 | |
|---|---|---|
| 0分 | 95% | 5% |
| 18分 | 89% | 11% |
| 20分 | 40% | 60% |
| 25分 | 40% | 60% |
| 26分 | 95% | 5% |
A液;0.3%酢酸
B液;アセトニトリル
カラム温度:35 ℃
測定波長:325 nm
流 量:1.0 ml/min
注 入 量:10 μl
条件2.(特異性確認用)
機 種:LC‐10AD [株式会社 島津製作所]
カ ラ ム:CAPCELLPAK C18 ACR、φ4.6 mm×15 cm [インタクト株式会社]
移 動 相: 水、アセトニトリル及びリン酸の混液(920:80:2)
カラム温度:40 ℃
測定波長:325 nm
流 量:1.0 ml/min
注 入 量:10 μl
e)フラボノール類
e)‐1 ルチン
試料を均一に粉砕もしくは混合した後、0.5〜2 g採取し、メタノール及び2.5%酢酸の混液(8:2)30 mlを加え10分間振とう抽出した。次に遠心分離を行い、上澄みを回収した。残さにメタノール及び2.5%酢酸の混液(8:2)30 mlを加え同様の操作を行った。再度、残さにメタノール及び2.5%酢酸の混液(8:2)20 mlを加え同様の操作を行い、3回分の抽出液を合わせた後、メタノール及び2.5%酢酸の混液(8:2)で100 mlに定容した。必要に応じ適宜希釈した後、メンブランフィルター(マイショリディスクW‐25‐5[東ソー株式会社])を通したものを試料溶液とした。
別にルチン標準品を精密にはかり、メタノール及び2.5%酢酸の混液(8:2)を用いて適宜希釈し、標準溶液を調製した。
試料溶液及び標準溶液をHPLCに注入し、ルチンの含量を求めた。
<高速液体クロマトグラフ操作条件>
条件1.(定量用)
機種:LC‐10ADvp [株式会社 島津製作所]
検出器:紫外可視分光光度計 SPD‐10AVvp [株式会社 島津製作所]
カラム:Unison UK‐C18、φ4.6 mm×15 cm [インタクト株式会社]
移動相:A液及びB液のリニアグラジエント
| A液 | B液 | |
|---|---|---|
| 0分 | 90% | 10% |
| 10分 | 85% | 15% |
| 20分 | 70% | 30% |
| 25分 | 65% | 35% |
| 30分 | 50% | 50% |
| 30.01分 | 10% | 90% |
| 35分 | 10% | 90% |
| 35.01分 | 90% | 10% |
A液;水及びリン酸の混液(1000:4)
B液;アセトニトリル
カラム温度:40 ℃
測定波長:360 nm
流量:1.0 ml/min
注入量:10 μl
条件2.(特異性確認用)
機種:LC‐10ATvp [株式会社 島津製作所]
検出器:紫外可視分光光度計 SPD‐10AV [株式会社 島津製作所]
カラム:Unison UK‐C18、φ4.6 mm×15 cm [インタクト株式会社]
移動相:A液、B液及びC液のリニアグラジエント
| A 液 | B 液 | C 液 | |
|---|---|---|---|
| 0 分 | 95 % | 5 % | 0 % |
| 20 分 | 55 % | 5 % | 40 % |
| 30 分 | 45 % | 5 % | 50 % |
| 35 分 | 45 % | 5 % | 50 % |
| 35.01 分 | 95 % | 5 % | 0 % |
A液;水及びリン酸の混液(1000:4)
B液;アセトニトリル
C液;メタノール
カラム温度:50 ℃
測定波長:360 nm
流 量:1.0 ml/min
注 入 量:10 μl
e)‐2 ケルセチン、ケンフェロール及びイソラムネチン
固体の試料の場合は、均一に粉砕もしくは混合した後、0.5〜8 g採取し、メタノール100 mlを加え1時間80 ℃の水浴で加熱還流抽出した。次に遠心分離を行い、上澄みを回収した。残さにメタノール100 mlを加え同様の操作を行い、上澄みを先の抽出液と合わせ、メタノールで250 mlに定容し試験溶液とした。
液状試料の場合は、2〜4 gを分取後、メタノールで50 mlに定容し試料溶液とした。
試料溶液を適宜分取し濃縮乾固後、メタノール4 mlに溶解した。さらに水3 ml、濃塩酸1 ml及びブチルヒドロキシトルエン12 mgを加え、1時間90 ℃の水浴で加熱還流抽出した。冷却後、20 mlに水で定容した。メタノール5 ml及び水10 mlでコンディショニングしたSep‐Pak Plus tC18に適宜負荷し、水30 mlで洗浄後、メタノール及び2.5%酢酸の混液(8:2)で溶出し10 mlに定容したものを加水分解溶液とした。
別にケルセチン、ケンフェロール及びイソラムネチン標準品を精密にはかり、メタノール及び2.5%酢酸の混液(8:2)を用いて適宜希釈し、標準溶液を調製した。
加水分解溶液及び標準溶液をHPLCに注入し、ケルセチン、ケンフェロール及びイソラムネチンの含量を求めた。
<高速液体クロマトグラフ操作条件>
条件1.(定量用)
機種:LC‐10ATvp [株式会社 島津製作所]
検出器:紫外可視分光光度計 SPD‐10AV [株式会社 島津製作所]
カラム:Unison UK‐C18、φ4.6 mm×15 cm [インタクト株式会社]
移動相:A液、B液及びC液のリニアグラジエント
| A 液 | B 液 | C 液 | |
|---|---|---|---|
| 0 分 | 95 % | 5 % | 0 % |
| 20 分 | 55 % | 5 % | 40 % |
| 30 分 | 45 % | 5 % | 50 % |
| 35 分 | 45 % | 5 % | 50 % |
| 35.01 分 | 95 % | 5 % | 0 % |
A液;水及びリン酸の混液(1000:4)
B液;アセトニトリル
C液;メタノール
カラム温度:50 ℃
測定波長:360 nm
流量:1.0 ml/min
注入量:20 μl
条件2.(特異性確認用)
機種:LC‐10ADvp [株式会社 島津製作所]
検出器:紫外可視分光光度計 SPD‐10AVvp [株式会社 島津製作所]
カラム:Unison UK‐C18、φ4.6 mm×15 cm [インタクト株式会社]
移動相:A液及びB液のリニアグラジエント
| A液 | B液 | |
|---|---|---|
| 0分 | 90% | 10% |
| 10分 | 85% | 15% |
| 20分 | 70% | 30% |
| 25分 | 65% | 35% |
| 30分 | 50% | 50% |
| 30.01分 | 10% | 90% |
| 35分 | 10% | 90% |
| 35.01分 | 90% | 10% |
A液;水及びリン酸の混液(1000:4)
B液;アセトニトリル
カラム温度:40 ℃
測定波長:360 nm
流 量:1.0 ml/min
注 入 量:10 μl
f)フラボン類
固体の試料の場合は、均一に粉砕もしくは混合した後、1〜8 g採取し、メタノール100 mlを加え1時間80 ℃の水浴で加熱還流抽出した。次に遠心分離を行い、上澄みを回収した。残さにメタノール100 mlを加え同様の操作を行い、上澄みを先の抽出液と合わせ、メタノールで250 mlに定容し試験溶液とした。
液状試料の場合は、2〜4 gを分取後、メタノールで50 mlに定容し試料溶液とした。
試料溶液を適宜分取し濃縮乾固後、メタノール4 mlに溶解した。さらに水3 ml、濃塩酸1 ml及びブチルヒドロキシトルエン12 mgを加え、3時間90 ℃の水浴で加熱還流抽出した。冷却後、20 mlに水で定容した。メタノール5 ml及び水10 mlでコンディショニングしたSep‐Pak Plus tC18に適宜負荷し、水30 mlで洗浄後、メタノール及び2.5%酢酸の混液(8:2)で溶出し10 mlに定容したものを加水分解溶液とした。
別にルテオリン及びアピゲニン標準品を精密にはかり、メタノール及び2.5%酢酸(8:2)を用いて適宜希釈し、標準溶液を調製した。
加水分解溶液及び標準溶液をHPLCに注入し、ルテオリン及びアピゲニンの含量を求めた。
<高速液体クロマトグラフ操作条件>
条件1.(ルテオリンの定量用及びアピゲニンの特異性確認用)
機 種:LC‐10ADvp [株式会社 島津製作所]
検 出 器:紫外可視分光光度計 SPD‐10AVvp [株式会社 島津製作所]
カ ラ ム:Unison UK‐C18、φ4.6 mm×15 cm [インタクト株式会社]
移 動 相:A液、B液及びC液のリニアグラジエント
| A液 | B液 | C液 | |
|---|---|---|---|
| 0分 | 95% | 5% | 0% |
| 20分 | 55% | 5% | 40% |
| 30分 | 45% | 5% | 50% |
| 35分 | 45% | 5% | 50% |
| 35.01分 | 95% | 5% | 0% |
A液;水及びリン酸の混液(1000:4)
B液;アセトニトリル
C液;メタノール
カラム温度:50 ℃
測定波長:360 nm
流 量:1.0 ml/min
注 入 量:10 μl
条件2.(ルテオリンの特異性確認用及びアピゲニンの定量用)
機 種:LC‐10ATvp [株式会社 島津製作所]
検 出 器:紫外可視分光光度計 SPD‐10AVvp [株式会社 島津製作所]
カ ラ ム:Unison UK‐C18、φ4.6 mm×15 cm [インタクト株式会社]
移 動 相:A液及びB液のリニアグラジエント
| A 液 | B 液 | |
|---|---|---|
| 0 分 | 90 % | 10 % |
| 10 分 | 85 % | 15 % |
| 20 分 | 70 % | 30 % |
| 25 分 | 65 % | 35 % |
| 30 分 | 50 % | 50 % |
| 30.01 分 | 10 % | 90 % |
| 35 分 | 10 % | 90 % |
| 35.01 分 | 90 % | 10 % |
A液;水及びリン酸の混液(1000:4)
B液;アセトニトリル
カラム温度:40 ℃
測定波長:360 nm
流 量:1.0 ml/min
注 入 量:10 μl
g)フラバノン類
g)‐1 ヘスペリジン及びナリンジン
試料を均一に粉砕もしくは混合した後、2〜6 g採取し、メタノール100 mlを加え1時間80 ℃の水浴で加熱還流抽出した。次に遠心分離を行い、上澄みを回収した。残さにメタノール100 mlを加え同様の操作を行い、上澄みを先の抽出液に合わせ、メタノールで250 mlに定容し試験溶液とした。
別にヘスペリジン及びナリンジン標準品を精密にはかり、メタノールを用いて適宜希釈し、標準溶液を調製した。
試験溶液及び標準溶液をHPLCに注入し、ヘスペリジン及びナリンジンの含量を求めた。
<高速液体クロマトグラフ操作条件>
条件1.(定量用)
機 種:LC‐10ATvp [株式会社 島津製作所]
検 出 器:紫外可視分光光度計 SPD‐10AVvp [株式会社 島津製作所]
カ ラ ム:Mightysil RP‐18 GP、φ4.6 mm×25 cm [関東化学株式会社]
移 動 相:水、アセトニトリル及び2‐プロパノールの混液(150:36:4)
ただし、0.4%クエン酸含有
カラム温度:30 ℃
測定波長:280 nm
流 量:1.0 ml/min
注 入 量:10 μl
条件2.(特異性確認用)
機 種:LC‐20AD [株式会社 島津製作所]
検 出 器:紫外可視分光光度計 SPD‐20A [株式会社 島津製作所]
カ ラ ム:XBridge C18、φ4.6 mm×15 cm [Waters Corporation]
移 動 相:水、アセトニトリル及びリン酸の混液(850:150:1)
カラム温度:40 ℃
測定波長:280 nm
流 量:1.0 ml/min
注 入 量:7 μl
g)‐2 ヘスペレチン(及びナリンゲニン)
試料(FR‐1)を均一に粉砕した後、5 g採取し、メタノール100 mlを加え1時間80 ℃の水浴で加熱還流抽出した。次に遠心分離を行い、上澄みを回収した。残さにメタノール100 mlを加え同様の操作を行い、上澄みを先の抽出液に合わせ、メタノールで250 mlに定容し試験溶液とした。
試料溶液を適宜分取し濃縮乾固後、メタノール4 mlに溶解した。さらに水3 ml、濃塩酸1 ml及びブチルヒドロキシトルエン12 mgを加え、2時間90 ℃の水浴で加熱還流抽出した。冷却後、20 mlに水で定容した。メタノール5 ml及び水10 mlでコンディショニングしたSep‐Pak Plus tC18に適宜負荷し、水30 mlで洗浄後、メタノール及び2.5%酢酸の混液(8:2)で溶出し10 mlに定容したものを加水分解溶液とした。
別にヘスペレチン標準品を精密にはかり、メタノール及び2.5%酢酸(8:2)を用いて適宜希釈し、標準溶液を調製した。
加水分解溶液及び標準溶液をHPLCに注入し、ヘスペレチンの含量を求めたが、妥当性確認試験の真度の結果が基準を満たさなかったため、ヘスペレチン及びナリンゲニンの分析は行わなかった。
<高速液体クロマトグラフ操作条件>
条件1.(定量用)
機 種:LC‐10ADvp [株式会社 島津製作所]
検 出 器:紫外可視分光光度計 SPD‐10AVvp [株式会社 島津製作所]
カ ラ ム:Unison UK‐C18、φ4.6 mm×15 cm [インタクト株式会社]
移 動 相:A液及びB液のリニアグラジエント
| A液 | B液 | |
|---|---|---|
| 0分 | 90% | 10% |
| 10分 | 85% | 15% |
| 20分 | 70% | 30% |
| 25分 | 65% | 35% |
| 30分 | 50% | 50% |
| 30.01分 | 10% | 90% |
| 35分 | 10% | 90% |
| 35.01分 | 90% | 10% |
A液;水及びリン酸の混液(1000:4)
B液;アセトニトリル
カラム温度:40 ℃
測定波長:280 nm
流 量:1.0 ml/min
注 入 量:10 μl
条件2.(特異性確認用)
機 種:LC‐10ATvp [株式会社 島津製作所]
検 出 器:紫外可視分光光度計 SPD‐10AV [株式会社 島津製作所]
カ ラ ム:Unison UK‐C18、φ4.6 mm×15 cm [インタクト株式会社]
移 動 相:A液、B液及びC液のリニアグラジエント
| A 液 | B 液 | C 液 | |
|---|---|---|---|
| 0 分 | 95 % | 5 % | 0 % |
| 20 分 | 55 % | 5 % | 40 % |
| 30 分 | 45 % | 5 % | 50 % |
| 35 分 | 45 % | 5 % | 50 % |
| 35.01 分 | 95 % | 5 % | 0 % |
A液;水及びリン酸の混液(1000:4)
B液;アセトニトリル
C液;メタノール
カラム温度:50 ℃
測定波長:280 nm
流 量:1.0 ml/min
注 入 量:10 μl
h)クルクミン
試料を0.1〜4 g採取し、水3〜15 mlになじませた後メタノール30 mlを加え5分間超音波抽出した。次に遠心分離を行い、上澄みを回収した。残さにメタノール60 mlを加え、15分間超音波照射し、遠心分離後上澄みを回収した。再度残さにメタノール60 mlまたは30 mlを加え同様の操作を上澄み液が無色となるまで繰り返し行った。上澄み液を合わせ、抽出回数によって250 mlまたは500 mlに定容した。必要に応じ適宜希釈した後、メンブランフィルター(マイショリディスクW‐25‐5[東ソー株式会社])を通したものを試料溶液とした。
別にクルクミン標準品を精密にはかり、メタノールを用いて溶解後、適宜希釈し、標準溶液を調製した。
試料溶液及び標準溶液をHPLCに注入し、クルクミンの含量を求めた。
<高速液体クロマトグラフ操作条件>
条件1.(定量用)
機 種:LC‐10AD [株式会社 島津製作所]
検 出 器:紫外可視吸光光度計 SPD‐10AV [株式会社 島津製作所]
カ ラ ム:Mightysil RP‐18 GP、φ4.6 mm×15 cm [関東化学株式会社]
移 動 相:水、アセトニトリル及びトリフルオロ酢酸の混液(550:450:1)
カラム温度:40 ℃
測定波長:420 nm
流 量:1.0 ml/min
注 入 量:10 μl
条件2.(特異性確認用)
機 種:LC‐10AD [株式会社 島津製作所]
検 出 器:紫外可視吸光光度計 SPD‐10AV [株式会社 島津製作所]
カ ラ ム:L‐column ODS、φ4.6 mm×15 cm [財団法人 化学物質評価研究機構]
移 動 相:0.1%リン酸、アセトニトリル及びメタノールの混液(500:400:100)
カラム温度:40 ℃
測定波長:420 nm
流 量:1.0 ml/min
注 入 量:10 μl
i) カロテノイド類
i)‐1 リコペン
試料2〜6 gを採取し、ヘキサン、アセトン、エタノール及びトルエンの混液(10:7:6:7)40 mlをかくはんしながら加えた。続いてエタノールをかくはんしながら加え100 mlに定容し、超音波照射を10分間行い抽出した。アセトンで適宜希釈した後、メンブランフィルター(シリンジフィルター 13GDX、0.45 μm、PTFE[ワットマンジャパン株式会社])を通したものを試料溶液とした。
別にリコペン標準品をベンゼンに溶解し、アセトンを用いて適宜希釈し、標準溶液を調製した。標準溶液濃度はリコペンの吸光係数E1%1cm=3446(474 nm アセトン)を用いて算出した。
試料溶液及び標準溶液をHPLCに注入し、リコペンの含量を求めた。
<高速液体クロマトグラフ操作条件>
機 種:LC‐10AS[株式会社 島津製作所]
検 出 器:紫外可視吸光光度計 SPD‐10AV[株式会社 島津製作所]
カラム:条件1. Mightysil RP‐18 GP、φ4.6 mm×25 cm[関東化学株式会社]
条件2. SunFire C18、φ4.6 mm×15 cm [Waters Corporation]
移 動 相:アセトニトリル、メタノール及びテトラヒドロフランの混液(55:40:5)
(0.1%酢酸及びα‐トコフェロール 50 ppm 含有)
カラム温度:40 ℃
測定波長:270 nm
流 量:1.5 ml/min
注 入 量:20 μl
i)‐2 ルテイン、ゼアキサンチン
試料をせん茶は0.5〜1 g、野菜類は2〜6 gを採取し、ヘキサン、アセトン、エタノール及びトルエンの混液(10:7:6:7)40 mlをかくはんしながら加えた。続いてエタノールをかくはんしながら加え100 mlに定容し、超音波照射を10分間行い抽出した。
定容液から10〜20 mlナスフラスコに分取し、ヘキサン、アセトン、エタノール及びトルエンの混液を加えて30 mlとし、40%KOH‐メタノールによりけん化抽出を行った。ヘキサン、アセトン、エタノール及びトルエンの混液と水の液液分配により溶媒層を回収し、溶媒を留去後、ヘキサン及びアセトンの混液(81:19)に溶解した。メンブランフィルター(シリンジフィルター 13 mm、0.45μm、PTFE[日本ミリポア株式会社])を通したものを試料溶液とした。
別にルテイン標準品をアセトンに溶解し、ヘキサン及びアセトンの混液(81:19)へ置換、適宜希釈して標準溶液を調製した。標準溶液濃度はルテインの吸光係数E1%1cm=2550(445 nm エタノール)を用いて算出した。
ゼアキサンチンについても同様に、アセトン溶解、ヘキサン及びアセトンの混液(81:19)へ置換、適宜希釈したものを標準溶液とした。標準溶液濃度はゼアキサンチンの吸光係数E1%1cm=2540(450 nm エタノール)を用いて算出した。
試料溶液及び標準溶液をHPLCに注入し、ルテイン、ゼアキサンチンの含量を求めた。
<高速液体クロマトグラフ操作条件>
条件1.(定量用)
機 種:LC‐10ATvp[株式会社 島津製作所]
検 出 器:紫外可視吸光光度計 SPD‐10AVvp[株式会社 島津製作所]
カラム:Luna 3μ Silica 、φ4.6 mm×15 cm[phenomenex]
移 動 相:ヘキサン及びアセトンの混液(82:18)(dl‐α‐トコフェロール 50 ppm 含有)
カラム温度:30 ℃
測定波長:450 nm
流 量:1.2 ml/min
注 入 量:30 μl
条件2.(特異性確認用)
機 種:LC‐10AS[株式会社 島津製作所]
検 出 器:紫外可視吸光光度計 SPD‐10AV[株式会社 島津製作所]
カラム:Shim‐pack CLC‐SIL(M) 、φ4.6 mm×15 cm[株式会社 島津製作所]
移 動 相:ヘキサン及びアセトンの混液(81:19)(dl‐α‐トコフェロール 50 ppm 含有)
カラム温度:30 ℃
測定波長:450 nm
流 量:1.1 ml/min
注 入 量:30 μl
i)‐3 アスタキサンチン
試料を5〜10 g 乳鉢に採取し、クロロホルム及びメタノールの混液(2:1)を加えながら磨砕抽出し、色が無くなるまで繰り返した。抽出液を300 ml分液ロートへ移し、クロロホルム及びメタノールの混液(2:1)及び水を加えて液液分配を行い、溶媒層を回収して溶媒留去後、アセトンに溶解した。
アセトン液の一部をコレステロールエステラーゼにより酵素分解を行った。石油エーテルによる液液分配後、溶媒層を回収して留去し、ヘキサン及びアセトンの混液(82:18 V/V)に溶解し、メンブランフィルター(シリンジフィルター 13 mm×0.45μm PTFE[日本ミリポア株式会社])を通したものを試料溶液とした。
別にアスタキサンチン標準品を精密にはかりクロロホルムに溶解し、ヘキサン及びアセトンの混液(82:18)へ置換、適宜希釈して標準溶液を調製した。
試料溶液及び標準溶液をHPLCに注入し、アスタキサンチンの含量を求めた。
<高速液体クロマトグラフ操作条件>
アスタキサンチン
機 種:LC‐20AT[株式会社 島津製作所]
検 出 器:紫外可視吸光光度計 SPD‐20A[株式会社 島津製作所]
カラム:Luna 3μg Silica 、φ4.6 mm×15 cm[phenomenex]
移 動 相:
条件1.(定量用);
ヘキサン及びアセトンの混液(82:18) ただし、dl‐α‐トコフェロール 50 ppm含有
条件2.(特異性確認用);
ヘキサン及び酢酸エチルの混液(7:3) ただし、dl‐α‐トコフェロール 50 ppm 含有
カラム温度:30 ℃
測定波長:470 nm
流 量:1.2 ml/min
注 入 量:40μl
j)γ‐アミノ酪酸
試料約1〜5 gを精密に量りとリ、10%(W/V)スルホサリチル酸溶液25 mlを加えて振とう後、3 mol/l水酸化ナトリウム溶液でpH2.2になるように調整し、クエン酸ナトリウム緩衝液(pH2.2)で50 mlに定容した。必要に応じクエン酸ナトリウム緩衝液(pH2.2)で希釈した後、メンブランフィルター(クロマトディスク13A 0.45μm[ジーエルサイエンス株式会社])でろ過したものを試験溶液とした。
試験溶液及び標準溶液100 ?lを以下のアミノ酸自動分析計に注入し、得られたピーク高さからγ‐アミノ酪酸含量を測定した。なお特異性確認のための測定は、o‐フタルアルデヒドで誘導体化後、高速液体クロマトグラフ法によった。
条件1.(定量用)
<アミノ酸自動分析計操作条件>
機 種:JLC‐500/V [日本電子株式会社]
カラム:LCR‐6、φ4 mm×12 cm[日本電子株式会社]
移 動 相:クエン酸リチウム緩衝液[日本電子株式会社]
反 応 液:ニンヒドリン試液[和光純薬工業株式会社]
条件2.(特異性確認用)
<高速液体クロマトグラフ操作条件>
機 種:LC‐20AD [株式会社 島津製作所]
検 出 器:蛍光分光光度計 RF‐10AXL [株式会社 島津製作所]
カラム:TSKgel ODS‐80Ts、φ4.6 mm×15 cm [東ソー株式会社]
移 動 相:10 mmol/lりん酸緩衝液(pH6.9)及びアセトニトリルの混液(8:2)
カラム温度:40 ℃
蛍光励起波長:340 nm
蛍光測定波長:450 nm
流 量:1.0 ml/min
注 入 量:10 μl
2.分析結果
a) イソフラボン類
測定結果を表1‐28に示した。PU‐5(納豆)についてはサクシニル体の含量も求めた。
表1‐28 イソフラボン類の測定結果
単位:mg/100g
| 識別番号 | 食品名 | アグリコン当量 | ダイジン | ゲニスチン | グリシチン | ダイゼイン | ゲニステイン | グリシテイン | アセチルダイジン | マロニルダイジン | アセチルゲニスチン | マロニルゲニスチン | アセチルグリシチン | マロニルグリシチン |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| PU-4 | 豆腐 木綿 | 24 | 6.9 | 9.5 | 0.95 | 0.25 | 0.27 | 0.025 | 1.4 | 8.3 | 0.46 | 12 | 0.86 | 0.92 |
| PU-5 | 納豆 糸引き | 49 | 18 | 40 | 1.6 | 0.57 | 2.1 | ※※ | 0.96 | 0.64 | 3.9 | 1.3 | ※ | ※※ |
| PU-6 | きな粉 | 270 | 91 | 120 | 6.6 | 7.3 | 9.9 | 1.9 | 79 | ※ | 110 | ※ | 6.3 | ※ |
| PU-7 | 豆乳 | 26 | 6.6 | 7 | 0.83 | 0.087 | 0.082 | 0.0085 | 0.31 | 14 | 0.40 | 17 | ※ | 1.1 |
| PU-8 | おから 全粒、乾 | 39 | 13 | 16 | 1.6 | 1.1 | 1.2 | 0.050 | ※※ | 13 | 0.43 | 19 | ※※ | 1.2 |
| PU-9 | だいず 全粒、乾 | 130 | 15 | 18 | 4.8 | 1.2 | 1.2 | 0.14 | ※※ | 74 | 0.17 | 110 | ※※ | 12 |
| PU-10 | だいず 全粒、乾 | 94 | 15 | 19 | 7.0 | 0.99 | 0.93 | 0.13 | ※※ | 45 | 0.43 | 69 | ※※ | 14 |
| PU-11 | だいず 全粒、乾 | 150 | 25 | 28 | 8.9 | 1.5 | 1.2 | 0.15 | ※※ | 76 | 0.68 | 110 | ※※ | 17 |
| VG-29 | えだまめ 冷凍 | 48 | 3.9 | 6.2 | 1.3 | 0.0061 | 0.012 | ※ | ※※ | 31 | 0.060 | 44 | ※※ | 4.0 |
| OT-1 | くず粉 乾、粉末 | 5.0 | ※ | ※ | ※ | 4.4 | 0.63 | ※ | ※ | ※ | ※ | ※ | ※ | ※ |
※:ピーク認めず ※※:夾雑成分の影響のため、算出不能。
個別値についてはアグリコン換算なし。PU‐5(納豆)はサクシニルダイジンが3.3 mg/100g、サクシニルゲニスチンが7.0 mg/100g、認められた。
b)カテキン類
測定結果を表1‐29及び表1‐30に示した。
表1‐29 カテキン類の測定結果(1)
単位:mg/100g
| 識別番号 | 食品名 | (+)-カテキン | エピカテキン | エピガロ カテキン ガレート |
エピガロ カテキン |
エピカテキンガレート |
|---|---|---|---|---|---|---|
| PU-1 | あずき 全粒、乾 |
14 | <0.5 | − | − | − |
| PU-2 | えんどう 全粒、乾 | <0.5 | <0.5 | − | − | − |
| PU-3 | ささげ 全粒、乾 |
33 | 1 | − | − | − |
| VG-1 | キャベツ 生 | <0.5 | <0.5 | − | − | − |
| VG-2 | たまねぎ 生 | <0.5 | <0.5 | − | − | − |
| VG-5 | トマト 生 | <0.5 | <0.5 | − | − | − |
| VG-8 | にんじん 根、生 | <0.5 | <0.5 | − | − | − |
| VG-9 | なす 生 | <0.5 | <0.5 | − | − | − |
| FR-4 | りんご 生 | 0.6 | 4.2 | − | − | − |
| FR-5 | いちご 生 | 2.8 | <0.5 | − | − | − |
| FR-13 | プルーン 乾 | <0.5 | <0.5 | − | − | − |
| FR-14 | ブルーベリー 生 | 1 | <0.5 | − | − | − |
‐:測定対象外
定量限界:0.5 mg/100g
表1‐30 カテキン類の測定結果(2)
単位:mg/100g
| 識別番号 | 食品名 | (+)-カテキン | エピカテキン | エピガロ カテキン ガレート |
エピガロ カテキン |
エピカテキンガレート |
|---|---|---|---|---|---|---|
| BV-1 | せん茶 茶 | 110 | 990 | 6500 | 4000 | 1200 |
| BV-2 | せん茶 茶 | 160 | 1000 | 5400 | 3000 | 1000 |
| BV-3 | せん茶 茶 | 120 | 880 | 6300 | 3200 | 1100 |
| BV-4 | せん茶 浸出液 |
1.2 | 11 | 41 | 43 | 6.9 |
| BV-5 | せん茶 浸出液 |
1.2 | 8.4 | 30 | 27 | 5.3 |
| BV-6 | せん茶 浸出液 |
1.3 | 9.5 | 42 | 34 | 7.2 |
| BV-7 | ウーロン茶 茶 | 66 | 580 | 4600 | 2100 | 1100 |
| BV-8 | ウーロン茶 浸出液 | <0.5 | 3.3 | 14 | 8.6 | 4.0 |
| BV-9 | 紅茶 茶 | 93 | 320 | 1300 | 190 | 1100 |
| BV-10 | 紅茶 浸出液 |
0.7 | 2.4 | 6.2 | 1.5 | 5.4 |
| BV-14 | ココア ピュアココア |
100 | 87 | − | − | − |
‐:測定対象外
定量限界:0.5 mg/100g
c)フェルラ酸
測定結果を表1‐31に示した。
表1‐31 フェルラ酸の測定結果
単位:mg/100g
| 識別番号 | 食品名 | 測定結果 | 識別番号 | 食品名 | 測定結果 |
|---|---|---|---|---|---|
| CE-1 | こめ 白米 | 7.2 | PO-3 | やまのいも 生 | <0.5 |
| CE-2 | こめ 白米 | 8.8 | VG-1 | キャベツ 生 | <0.5 |
| CE-3 | こめ 白米 | 8.6 | VG-2 | たまねぎ 生 | <0.5 |
| CE-4 | こめ 白米 | 6.5 | VG-5 | トマト 生 | 0.9 |
| CE-5 | こめ 白米 | 6.2 | VG-8 | にんじん 根、生 | <0.5 |
| CE-6 | こめ 玄米 | 25 | VG-9 | なす 生 | <0.5 |
| CE-7 | こめ 玄米 | 30 | VG-13 | ほうれんそう 生 | 12 |
| CE-8 | こめ 玄米 | 28 | FR-1 | うんしゅうみかん 生 | 7.1 |
| CE-9 | こめ 玄米 | 25 | FR-4 | りんご 生 | <0.5 |
| CE-10 | こめ 玄米 | 24 | BV-1 | せん茶 茶 | 4.5 |
| CE-11 | こめ 発芽玄米 |
31 | BV-4 | せん茶 浸出液 |
<0.5 |
| CE-14 | こむぎ 全粒粉 |
120 | BV-8 | ウーロン茶 浸出液 | <0.5 |
| CE-15 | おおむぎ 押麦 |
36 | BV-10 | 紅茶 浸出液 | <0.5 |
| CE-16 | そば そば粉 | <0.5 | BV-11 | コーヒー 豆 | 170 |
| CE-19 | そば 乾麺 | 5.7 | BV-12 | コーヒー 浸出液 |
3.7 |
| CE-20 | あわ 精白粒 | 51 | BV-13 | コーヒー インスタント |
720 |
| PO-1 | さつまいも 生 | 0.5 |
定量限界:0.5 mg/100g
d)クロロゲン酸
測定結果を表1‐32に示した。
表1‐32 クロロゲン酸の測定結果
単位:mg/100g
| 識別番号 | 食品名 | 5-カフェオイルキナ酸 | 総クロロゲン酸 |
|---|---|---|---|
| PO-1 | さつまいも 生 | 15 | 16 |
| PO-2 | さといも 生 | <1 | <1 |
| PO-3 | やまのいも 生 | <1 | <1 |
| PO-4 | じゃがいも 生 | 5 | 5 |
| VG-1 | キャベツ 生 | <1 | 1 |
| VG-2 | たまねぎ 生 | <1 | <1 |
| VG-5 | トマト 生 | 1 | 2 |
| VG-8 | にんじん 根、生 | 7 | 7 |
| VG-9 | なす 生 | 120 | 130 |
| VG-10 | なす 生 | 160 | 160 |
| VG-11 | なす 生 | 160 | 160 |
| VG-17 | ごぼう 根、生 | 52 | 54 |
| VG-18 | ごぼう 根、生 | 24 | 25 |
| VG-19 | ごぼう 根、生 | 130 | 130 |
| VG-21 | モロヘイヤ 生 | 34 | 55 |
| FR-1 | うんしゅうみかん 生 | <1 | 1 |
| FR-4 | りんご 生 | 14 | 14 |
| FR-13 | プルーン 乾 | 7 | 150 |
| FR-14 | ブルーベリー 生 | 68 | 68 |
| BV-1 | せん茶 茶 | 19 | 30 |
| BV-4 | せん茶 浸出液 | <1 | 2 |
| BV-8 | ウーロン茶 浸出液 | <1 | 2 |
| BV-10 | 紅茶 浸出液 | <1 | 3 |
| BV-11 | コーヒー 豆 | 840 | 1700 |
| BV-12 | コーヒー 浸出液 | 22 | 46 |
| BV-13 | コーヒー インスタント | 2000 | 4800 |
定量限界:1 mg/100g
e) フラボノール類
測定結果を表1‐33に示した。
表1‐33 フラボノール類の測定結果
単位:mg/100g
| 識別 番号 |
食品名 | ケルセチン | ケンフェロール | イソラムネチン | ルチン |
|---|---|---|---|---|---|
| CE-16 | そば そば粉 | 5.2 | <0.5 | <0.5 | 9.2 |
| CE-17 | そば そば粉 | 8.4 | <0.5 | <0.5 | 15 |
| CE-18 | そば そば粉 | 6.7 | <0.5 | <0.5 | 12 |
| CE-19 | そば 乾麺 | 2.2 | <0.5 | <0.5 | 2.9 |
| PU-1 | あずき 全粒、乾 | 6.1 | <0.5 | <0.5 | − |
| PU-2 | えんどう 全粒、乾 | <0.5 | 2.2 | <0.5 | − |
| PU-3 | ささげ 全粒、乾 | 19 | <0.5 | <0.5 | − |
| VG-1 | キャベツ 生 | <0.5 | <0.5 | <0.5 | − |
| VG-2 | たまねぎ 生 | 25 | <0.5 | 0.9 | − |
| VG-3 | たまねぎ 生 | 9.6 | <0.5 | <0.5 | − |
| VG-4 | たまねぎ 生 | 10 | <0.5 | <0.5 | − |
| VG-5 | トマト 生 | 0.5 | <0.5 | <0.5 | − |
| VG-8 | にんじん 根、生 | <0.5 | <0.5 | <0.5 | − |
| VG-9 | なす 生 | <0.5 | <0.5 | <0.5 | − |
| VG-12 | ピーマン 青、生 | 1.6 | <0.5 | <0.5 | − |
| VG-13 | ほうれんそう 生 | <0.5 | <0.5 | <0.5 | − |
| VG-16 | レタス 生 | 0.7 | <0.5 | <0.5 | − |
| VG-20 | ケール 生 | 6.1 | 31 | <0.5 | − |
| VG-21 | モロヘイヤ 生 | 19 | 2.0 | <0.5 | − |
| VG-23 | しそ 生 | 分析不能※ | <0.5 | <0.5 | − |
| VG-25 | アスパラガス 生 | 5.0 | <0.5 | <0.5 | 9.8 |
| FR-1 | うんしゅうみかん 生 | 1.3 | 0.9 | 1.3 | − |
| FR-4 | りんご 生 | <0.5 | <0.5 | <0.5 | − |
| FR-14 | ブルーベリー 生 | 12 | 0.9 | 0.7 | − |
| BV-1 | せん茶 茶 | 180 | 220 | <0.5※ | − |
| BV-4 | せん茶 浸出液 | 2.2 | 2.5 | <0.5 | − |
| BV-8 | ウーロン茶 浸出液 | 1.5 | 0.6 | <0.5 | − |
| BV-10 | 紅茶 浸出液 | 2.9 | 1.1 | <0.5 | − |
※:夾雑成分の影響のため、分析不能とした。 ‐:測定対象外
定量限界:0.5 mg/100g
f) フラボン類
測定結果を表1‐34に示した。
表1‐34 フラボン類の測定結果
単位:mg/100g
| 識別番号 | 食品名 | ルテオリン | アピゲニン |
|---|---|---|---|
| VG-1 | キャベツ 生 | <0.5 | <0.5 |
| VG-2 | たまねぎ 生 | <0.5 | <0.5 |
| VG-5 | トマト 生 | <0.5 | <0.5 |
| VG-8 | にんじん 根、生 | <0.5 | <0.5 |
| VG-9 | なす 生 | <0.5 | <0.5 |
| VG-12 | ピーマン 青、生 | 4.1 | <0.5 |
| VG-13 | ほうれんそう 生 | <0.5 | <0.5 |
| VG-16 | レタス 生 | <0.5 | <0.5 |
| VG-22 | パセリ 生 | <0.5 | 480 |
| VG-23 | しそ 生 | 3.8 | 2.5 |
| VG-24 | セロリー 生 | <0.5 | <0.5 |
| VG-25 | アスパラガス 生 | <0.5 | <0.5 |
| VG-28 | きゅうり 生 | <0.5 | <0.5 |
| FR-1 | うんしゅうみかん 生 | <0.5 | <0.5 |
| FR-4 | りんご 生 | <0.5 | <0.5 |
| BV-1 | せん茶 茶 | 2.4 | <5※ |
| BV-4 | せん茶 浸出液 | <0.5 | <0.5 |
| BV-8 | ウーロン茶 浸出液 | <0.5 | <0.5 |
| BV-10 | 紅茶 浸出液 | <0.5 | <0.5 |
※:夾雑成分の影響より、定量限界を5 mg/100gとした。
定量限界:0.5 mg/100g
g)フラバノン類
測定結果を表1‐35に示した。
表1‐35 フラバノン類の測定結果
単位:mg/100g
| 識別番号 | 食品名 | ヘスペリジン | ナリンジン | ヘスペレチン | ナリンゲニン |
|---|---|---|---|---|---|
| VG-1 | キャベツ 生 | − | − | ※ | ※ |
| VG-2 | たまねぎ 生 | − | − | ※ | ※ |
| VG-5 | トマト 生 | − | − | ※ | ※ |
| VG-8 | にんじん 根、生 | − | − | ※ | ※ |
| VG-9 | なす 生 | − | − | ※ | ※ |
| VG-12 | ピーマン 青、生 | − | − | ※ | ※ |
| VG-13 | ほうれんそう 生 | − | − | ※ | ※ |
| FR-1 | うんしゅうみかん 生 | 120 | − | ※ | ※ |
| FR-2 | うんしゅうみかん 生 | 150 | − | ※ | ※ |
| FR-3 | うんしゅうみかん 生 | 160 | − | ※ | ※ |
| FR-4 | りんご 生 | − | − | ※ | ※ |
| FR-6 | いよかん 生 | 56 | − | ※ | ※ |
| FR-7 | バレンシアオレンジ 生 | 65 | − | ※ | ※ |
| FR-8 | グレープフルーツ ルビー 生 | 1.6 | 48 | ※ | ※ |
| FR-9 | レモン 生 | 320 | - | ※ | ※ |
| FR-10 | ゆず 生、皮 | 110 | 70 | ※ | ※ |
| FR-11 | ゆず 生、果汁 | 9.3 | 13 | ※ | ※ |
| BV-1 | せん茶 茶 | − | − | ※ | ※ |
| BV-4 | せん茶 浸出液 | − | − | ※ | ※ |
| BV-8 | ウーロン茶 浸出液 | − | − | ※ | ※ |
‐:測定対象外
※:フラバノン(加水分解)の妥当性確認試験の結果が基準を満たさなかったため、ヘスペレチン及びナリンゲニンの分析を中止した。
h)クルクミン
測定結果を表1‐36に示した。
表1‐36 クルクミンの測定結果
単位:mg/100g
| 識別番号 | 食品名 | 測定結果 |
|---|---|---|
| OT-2 | カレー カレー粉 | 190 |
| OT-3 | カレー カレールー | 13 |
| OT-4 | 秋うこん 乾、粉末 | 1200 |
| OT-5 | 春うこん 乾、粉末 | 58 |
| OT-6 | 黒うこん 乾、粉末 | 0.2 |
i)カロテノイド類
測定結果を表1‐37及び表1‐38に示した。
表1‐37 カロテノイドの測定結果(1)
単位:mg/100g
| 識別番号 | 食品名 | ルテイン | ゼアキサンチン | リコペン | アスタキサンチン |
|---|---|---|---|---|---|
| VG-1 | キャベツ 生 | 0.07 | <0.02 | − | − |
| VG-5 | トマト 生 | 0.06 | <0.02 | 4.6 | − |
| VG-6 | トマト 生 | − | − | 4.5 | − |
| VG-7 | トマト 生 | − | − | 3.5 | − |
| VG-8 | にんじん 根、生 | 0.2 | <0.02 | − | − |
| VG-12 | ピーマン 青、生 | 1.1 | <0.02 | − | − |
| VG-13 | ほうれんそう 生 | 4.7 | 0.09 | − | − |
| VG-14 | ほうれんそう 生 | 9.8 | 0.12 | − | − |
| VG-15 | ほうれんそう 生 | 7.9 | 0.15 | − | − |
| VG-16 | レタス 生 | 0.33 | <0.02 | − | − |
| VG-29 | えだまめ 冷凍 | 0.46 | <0.02 | − | − |
| VG-30 | かぼちゃ 生 | 5.6 | 0.59 | − | − |
| VG-31 | 金時人参 根、生 | 0.1 | 0.04 | 11 | − |
| FS-1 | えび 生、殻つき | − | − | − | 5.4 |
| FS-2 | しろさけ イクラ | − | − | − | 0.87 |
| FS-3 | ぎんざけ | − | − | − | 0.97 |
‐:測定対象外 定量限界:0.02 mg/100g
表1‐38 カロテノイドの測定結果(2)
単位:mg/100g
| 識別番号 | 食品名 | ルテイン | ゼアキサンチン | リコペン | アスタキサンチン |
|---|---|---|---|---|---|
| FS-4 | べにざけ | − | − | − | 2.0 |
| FS-5 | しろさけ | − | − | − | 0.16 |
| FR-8 | グレープフルーツ ルビー 生 |
− | − | 0.50 | − |
| FR-12 | かき 熟、生 | 0.02 | 0.25 | 0.31 | − |
| FR-15 | すいか 生 | − | − | 2.6 | − |
| FR-18 | パパイヤ 生 | 0.05 | 0.02 | 1.0 | − |
| BV-1 | せん茶 茶 | 52 | 2.7 | − | − |
‐:測定対象外
j) γ‐アミノ酪酸
測定結果を表1‐39に示した。
表1‐39 γ‐アミノ酪酸の測定結果
単位:mg/100g
| 識別番号 | 食品名 | 測定結果 | 識別番号 | 食品名 | 測定結果 |
|---|---|---|---|---|---|
| CE-6 | こめ 玄米 | 2 | VG-6 | トマト 生 | 30 |
| CE-7 | こめ 玄米 | 2 | VG-7 | トマト 生 | 68 |
| CE-8 | こめ 玄米 | 3 | VG-8 | にんジん 根、生 | 5 |
| CE-9 | こめ 玄米 | 5 | VG-16 | レタス 生 | 5 |
| CE-10 | こめ 玄米 | <1 | VG-25 | アスパラガス 生 | 6 |
| CE-11 | こめ 発芽玄米 | 9 | VG-26 | アスパラガス 生 | 8 |
| CE-12 | こめ 発芽玄米 | 21 | VG-27 | アスパラガス 生 | 9 |
| CE-13 | こめ 発芽玄米 | 9 | VG-30 | かぼちゃ 生 | 46 |
| PO-4 | じゃがいも 生 | 34 | FR-1 | うんしゅうみかん 生 | 71 |
| PO-5 | じゃがいも 生 | 50 | FR-5 | いちご 生 | 1 |
| PO-6 | じゃがいも 生 | 36 | FR-16 | バナナ 生 | 20 |
| PU-9 | だいず 全粒、乾 | 11 | FR-17 | メロン 生 | 72 |
| VG-1 | キャベツ 生 | 22 | FR-18 | パパイヤ 生 | 48 |
| VG-5 | トマト 生 | 44 |
定量限界:1 mg/100g
3.妥当性確認試験の結果
a)イソフラボン類
イソフラボン類の妥当性確認試験は、総量で行うことが困難なため、ゲニスチン(配糖体)及びゲニステイン(アグリコン)で行った。検出されることが前提である方法のため、定量限界及び検出限界は求めなかった。妥当性確認試験の結果を表1‐40及び表1‐41に示した。
表1‐40 イソフラボン類(ゲニスチン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| だいず 全粒、乾 |
1回目 | 100.1% | 1.0% | 1.08 | 実施せず | 実施せず |
| 2回目 | 99.7% | |||||
| 3回目 | 100.9% | |||||
| 4回目 | 102.2% | |||||
| 5回目 | 101.6% | |||||
| 平均 | 100.9% | − | − |
表1‐41 イソフラボン類(ゲニステイン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| だいず 全粒、乾 |
1回目 | 92.2% | 1.2% | 0.97 | 実施せず | 実施せず |
| 2回目 | 89.3% | |||||
| 3回目 | 90.8% | |||||
| 4回目 | 90.4% | |||||
| 5回目 | 89.7% | |||||
| 平均 | 90.5% | − | − |
b) カテキン類
妥当性確認試験の結果を表1‐42〜表1‐44に示した。
表1‐42 カテキン類(カテキン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| りんご 生 | 1回目 | 101.2% | 0.8% | 1.00 | 0.5 mg/100g (S/N比 33.2) |
0.13 mg/100g (S/N比 7.9) |
| 2回目 | 103.1% | |||||
| 3回目 | 101.6% | |||||
| 4回目 | 101.2% | |||||
| 5回目 | 101.0% | |||||
| 平均 | 101.6% | − | − |
表1‐43 カテキン類(エピガロカテキンガレート)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| 紅茶 茶 | 1回目 | 101.0% | 2.7% | 0.97 | 0.5 mg/100g (S/N比 53.1) |
0.16 mg/100g (S/N比 16.7) |
| 2回目 | 102.0% | |||||
| 3回目 | 102.1% | |||||
| 4回目 | 95.9% | |||||
| 5回目 | 98.4% | |||||
| 平均 | 99.9% | − | − |
表1‐44 カテキン類(エピガロカテキン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| 紅茶 茶 | 1回目 | 107.0% | 1.4% | 実施せず | 0.5 mg/100g (S/N比 41.2) |
0.16 mg/100g (S/N比 15.6) |
| 2回目 | 107.4% | |||||
| 3回目 | 109.8% | |||||
| 4回目 | 105.7% | |||||
| 5回目 | 107.2% | |||||
| 平均 | 107.4% | − | − |
c)フェルラ酸
妥当性確認試験の結果を表1‐45に示した。
表1‐45 フェルラ酸の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| こめ 玄米 |
1回目 | 92.2% | 1.9% | 1.00 | 0.5 mg/100g (S/N比 20.8) |
0.13 mg/100g (S/N比 7.9) |
| 2回目 | 89.6% | |||||
| 3回目 | 92.3% | |||||
| 4回目 | 91.2% | |||||
| 5回目 | 94.5% | |||||
| 平均 | 92.0% | − | − | |||
| せん茶 茶 | 1回目 | 97.6% | 1.4% | 0.99 | ||
| 2回目 | 99.6% | |||||
| 3回目 | 98.1% | |||||
| 4回目 | 97.8% | |||||
| 5回目 | 100.8% | |||||
| 平均 | 98.8% | − | − | |||
| キャベツ 生 | 1回目 | 98.5% | 0.6% | 0.94 | ||
| 2回目 | 97.8% | |||||
| 3回目 | 98.7% | |||||
| 4回目 | 98.5% | |||||
| 5回目 | 97.2% | |||||
| 平均 | 98.1% | − | − |
d) クロロゲン酸
妥当性確認試験の結果を表1‐46に示した。
表1‐46 クロロゲン酸(5‐カフェオイルキナ酸)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| じゃがいも 生 | 1回目 | 103.9% | 0.6% | 0.96 | 1 mg/100g (S/N比10.7) |
0.2 mg/100g (S/N比 3.2) |
| 2回目 | 105.0% | |||||
| 3回目 | 104.3% | |||||
| 4回目 | 103.3% | |||||
| 5回目 | 103.9% | |||||
| 平均 | 104.1% | − | − | |||
| なす 生 | 1回目 | 99.2% | 3.6% | 1.00 | ||
| 2回目 | 103.6% | |||||
| 3回目 | 96.5% | |||||
| 4回目 | 104.0% | |||||
| 5回目 | 105.2% | |||||
| 平均 | 101.7% | − | − | |||
| 紅茶 浸出液 |
1回目 | 107.3% | 0.9% | 0.96 | ||
| 2回目 | 107.7% | |||||
| 3回目 | 105.6% | |||||
| 4回目 | 105.7% | |||||
| 5回目 | 107.0% | |||||
| 平均 | 106.7% | − | − |
e)フラボノール類
妥当性確認試験の結果を表1‐47及び表1‐48に示した。
表1‐47 フラボノール類(ケルセチン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| そば そば粉 |
1回目 | 92.9% | 2.8% | 1.09 | 0.5 mg/100g (S/N比17.8) |
0.15 mg/100g (S/N比 6.1) |
| 2回目 | 93.3% | |||||
| 3回目 | 96.4% | |||||
| 4回目 | 99.3% | |||||
| 5回目 | 97.4% | |||||
| 平均 | 95.9% | − | − | |||
| りんご 生 | 1回目 | 92.3% | 3.6% | 1.05 | ||
| 2回目 | 85.9% | |||||
| 3回目 | 86.1% | |||||
| 4回目 | 83.9% | |||||
| 5回目 | 87.6% | |||||
| 平均 | 87.2% | − | − | |||
| アスパラガス 生 | 1回目 | 72.2% | 6.6% | 0.98 | ||
| 2回目 | 78.8% | |||||
| 3回目 | 74.3% | |||||
| 4回目 | 78.3% | |||||
| 5回目 | 85.6% | |||||
| 平均 | 77.8% | − | − |
表1‐48 フラボノール類(ルチン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| そば そば粉 |
1回目 | 95.6% | 1.3% | 1.00 | 0.5 mg/100g (S/N比 14.8) |
0.2 mg/100g (S/N比 5.2) |
| 2回目 | 94.7% | |||||
| 3回目 | 96.4% | |||||
| 4回目 | 93.1% | |||||
| 5回目 | 94.6% | |||||
| 平均 | 94.9% | − | − | |||
| アスパラガス 生 | 1回目 | 98.8% | 1.3% | 1.02 | ||
| 2回目 | 96.1% | |||||
| 3回目 | 98.1% | |||||
| 4回目 | 97.7% | |||||
| 5回目 | 95.9% | |||||
| 平均 | 97.3% | − | − |
f)フラボン類
妥当性確認試験の結果を表1‐49に示した。
表1‐49 フラボン類(ルテオリン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| ピーマン 青、生 | 1回目 | 82.3% | 8.6% | 0.95 | 0.5 mg/100g (S/N比12.6) |
0.15 mg/100g (S/N比 4.1) |
| 2回目 | 74.0% | |||||
| 3回目 | 82.6% | |||||
| 4回目 | 71.6% | |||||
| 5回目 | 88.3% | |||||
| 平均 | 79.8% | − | − |
g)フラバノン類
妥当性確認試験の結果を表1‐50及び表1‐51に示した。
表1‐50 フラバノン類(ヘスペリジン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| うんしゅうみかん 生 | 1回目 | 103.4% | 1.3% | 1.00 | 0.5 mg/100g (S/N比10.5) |
0.13 mg/100g (S/N比3.4) |
| 2回目 | 104.7% | |||||
| 3回目 | 106.0% | |||||
| 4回目 | 102.6% | |||||
| 5回目 | 105.0% | |||||
| 平均 | 104.3% | − | − |
表1‐51 フラバノン類(ヘスペレチン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| うんしゅうみかん 生 | 1回目 | 69.6% | 3.4% | 0.99 | 0.5 mg/100g (S/N比15.2) |
0.05 mg/100g (S/N比3.3) |
| 2回目 | 64.1% | |||||
| 3回目 | 66.6% | |||||
| 4回目 | 69.6% | |||||
| 5回目 | 67.6% | |||||
| 平均 | 67.5% | − | − |
真度が基準を下回ったため、ヘスペレチンは分析対象外とした。
h)クルクミン
妥当性確認試験の結果を表1‐52に示した。
表1‐52 クルクミンの妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性※ (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| 秋うこん 乾、粉末 | 1回目 | 85.5% | 0.8% | 1.00 | 0.5 mg/100g (S/N比 19.3) |
0.1 mg/100g (S/N比 5.1) |
| 2回目 | 87.2% | |||||
| 3回目 | 85.9% | |||||
| 4回目 | 85.7% | |||||
| 5回目 | 85.7% | |||||
| 平均 | 86.0% | − | − |
i) カロテノイド類
妥当性確認試験の結果を表1‐53〜表1‐56に示した。
表1‐53 カロテノイド類(リコペン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| すいか 生 |
1回目 | 105.1% | 3.1% | 0.96 | 0.02 mg/100g (S/N比 15.7) |
実施せず |
| 2回目 | 103.4% | |||||
| 3回目 | 101.8% | |||||
| 4回目 | 103.4% | |||||
| 5回目 | 101.9% | |||||
| 平均 | 103.1% | − | − | |||
| トマト 生 |
1回目 | 100.4% | 1.1% | 1.00 | ||
| 2回目 | 101.6% | |||||
| 3回目 | 99.9% | |||||
| 4回目 | 99.9% | |||||
| 5回目 | 100.3% | |||||
| 平均 | 100.4% | − | − |
検出限界については、定量限界以上の数値が出ることが前提の分析方法のため、実施しなかった。
表1‐54 カロテノイド類(ルテイン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| ほうれんそう 生 | 1回目 | 100.4% | 2.0% | 1.01 | 0.02 mg/100g (S/N比 17.7) |
実施せず |
| 2回目 | 95.1% | |||||
| 3回目 | 100.4% | |||||
| 4回目 | 98.0% | |||||
| 5回目 | 97.8% | |||||
| 平均 | 98.3% | − | − | |||
| にんじん 根、生 | 1回目 | 96.1% | 1.8% | 0.97 | ||
| 2回目 | 97.0% | |||||
| 3回目 | 97.0% | |||||
| 4回目 | 95.0% | |||||
| 5回目 | 100.3% | |||||
| 平均 | 97.1% | − | − | |||
| せん茶 茶 |
1回目 | 95.0% | 3.0% | 1.01 | ||
| 2回目 | 89.0% | |||||
| 3回目 | 97.8% | |||||
| 4回目 | 96.4% | |||||
| 5回目 | 95.2% | |||||
| 平均 | 94.7% |
検出限界については、定量限界以上の数値が出ることが前提の分析方法のため、実施しなかった。
表1‐55 カロテノイド類(ゼアキサンチン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| ほうれんそう 生 | 1回目 | 97.3% | 1.8% | 1.02 | 0.02 mg/100g (S/N 18.2) |
実施せず |
| 2回目 | 91.8% | |||||
| 3回目 | 94.4% | |||||
| 4回目 | 93.6% | |||||
| 5回目 | 93.3% | |||||
| 平均 | 94.1% | − | − | |||
| にんじん 根、生 | 1回目 | 90.6% | 3.2% | 1.00 | ||
| 2回目 | 97.7% | |||||
| 3回目 | 96.6% | |||||
| 4回目 | 97.1% | |||||
| 5回目 | 100.4% | |||||
| 平均 | 96.5% | − | − | |||
| せん茶 茶 |
1回目 | 89.8% | 3.5% | 1.03 | ||
| 2回目 | 80.2% | |||||
| 3回目 | 87.7% | |||||
| 4回目 | 86.5% | |||||
| 5回目 | 89.4% | |||||
| 平均 | 86.7% | − | − |
検出限界については、定量限界以上の数値が出ることが前提の分析方法のため、実施しなかった。
表1‐56 カロテノイド類(アスタキサンチン)の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| べにざけ | 1回目 | 92.7% | 2.9% | 1.02 | 0.02 mg/100g (S/N 17.6) |
実施せず |
| 2回目 | 90.4% | |||||
| 3回目 | 93.8% | |||||
| 4回目 | 87.3% | |||||
| 5回目 | 94.2% | |||||
| 平均 | 91.7% | − | − |
検出限界については、定量限界以上の数値が出ることが前提の分析方法のため、実施しなかった。
j) γ‐アミノ酪酸
妥当性確認試験の結果を表1‐57に示した。
表1‐57 γ‐アミノ酪酸の妥当性確認試験の結果
| 食品名 | 繰り返し | 真度 (回収率) |
併行精度 (相対標準偏差) |
特異性 (条件1.÷条件2.) |
定量限界 (S/N比) |
検出限界 (S/N比) |
|---|---|---|---|---|---|---|
| トマト 生 | 1回目 | 101.6% | 1.6% | 1.01 | 1 mg/100g (S/N比 17.0) |
実施せず |
| 2回目 | 98.9% | |||||
| 3回目 | 100.1% | |||||
| 4回目 | 102.4% | |||||
| 5回目 | 98.5% | |||||
| 平均 | 100.3% | − | − | |||
| こめ 発芽玄米 | 1回目 | 98.9% | 3.9% | 0.94 | ||
| 2回目 | 99.8% | |||||
| 3回目 | 101.8% | |||||
| 4回目 | 104.4% | |||||
| 5回目 | 108.9% | |||||
| 平均 | 102.7% | − | − |
検出限界については、定量限界以上の数値が出ることが前提の分析方法のため、実施しなかった。
お問合せ先
科学技術・学術:科学技術・学術に関する基本的政策
-- 登録:平成21年以前 --