- 現在位置
- トップ > 政策・審議会 > 審議会情報 > 科学技術・学術審議会 > 資料3‐2 地球上の生命を育む水のすばらしさの更なる認識と新たな発見を目指して > 第4章 水の特性を生かした様々な活用 2 超臨界水
第4章 水の特性を生かした様々な活用 2 超臨界水
2 超臨界水 ― 高温高圧下で特異なふるまいをする水 東京大学環境安全研究センター助教授 大島 義人
(要旨)
水の場合、臨界点(臨界温度は374℃、臨界圧力は22.1Mpa(218気圧))の近くでは、わずかな圧力変化により密度が連続的に大きく変化する。例えば、溶媒として「ものを溶かす」能力(溶解力)は、水の密度と密接に相関することから、同じ温度であっても、ほんの少し圧力を変えるだけで、溶解力を急激に変化させることができる。密度に相関する他の物性値(粘度、熱伝導率など)についても同様で、原理的には、圧力と温度だけを操作因子として、様々な水の物性を幅広くコントロールすることが可能になる。
また、気体と液体の中間である超臨界状態を化学反応の「場」とすることで、化学反応の速度を極めて大きくすることが期待できる。更に、「超臨界水」は有機物を溶かすことができるため、工業的にも重要な有機合成を行う上で、従来の有機溶媒に代替する新しい溶媒としても期待される。また、何より水自体は自然界に豊富に存在する無毒で安価な溶媒であり、今後、環境調和型技術への指向がより一層強まっていくことが予想される中で、「超臨界水」を溶媒とする化学反応は、低リスク・低環境負荷を実現するための基盤技術の一つとして注目されるべきである。
また、ほとんどの有機物は、超臨界水酸化反応という高温高圧の水中で「ものを燃やす」反応によって、秒単位の極めて短い時間でほぼ100パーセント完全に分解し、二酸化炭素を生成する。この反応は、1.反応速度が非常に大きい、2.自らの反応熱で温度を維持することができるため、省エネルギー化が期待できる、3.水中の燃焼なので、温度の暴走や爆発などの危険性が低い、4.排ガスの処理が不要となり、省スペース化が期待できるなどといった特徴を持っている。
より実用的な技術に向けて、解決すべき課題も残されているが、高温高圧という特殊な環境であるとはいえ、「水」でありながら固体、液体、気体とは全く異なる性格を発現する「超臨界水」は十分魅力的であり、持続的社会を実現するための基盤技術の一つとして大いに期待される。
2‐1 超臨界水とは何か
(1)水の相挙動について
物質には「固体」、「液体」、「気体」の三態があることはよく知られている。水であれば、温度と圧力によって、「氷」、「(液体の)水」、「水蒸気」という、見かけや性質が異なった姿をとる。図1に水の相図を示す。この図を見れば、置かれている温度や圧力によって、水がどの状態をとるのかがわかる。例えば、大気圧(1気圧)において温度を上げていく(例えば、図1上で点aから点線に沿って右にたどっていく)と、温度が低いところではしばらく固体であり、0℃を境に液体の水の状態に移行し、100℃を超えると気体(水蒸気)となる。ここで、100℃で横切った線は気液平衡線と呼ばれ[1]、この線上にあたる温度・圧力では、気体と液体が両方同時に存在することになる(やかんの中に沸騰するお湯と水蒸気が同時に存在する現象に相当する。)
さて、この気液平衡線を右上にたどっていくと、あるところで突然途切れていることに気づく。この途切れている点を、水の臨界点といい、この温度、圧力を、それぞれ臨界温度、臨界圧力と呼ぶ[2]。水の場合、臨界温度は374℃、臨界圧力は22.1MPa(218気圧)である。臨界温度よりも低い温度では、気体の水を圧縮していく(図1で気体の領域から垂直に上にたどる)と、どこかの圧力で気液平衡線と交わり、液化が始まる。しかし、臨界温度を超える温度では、どんなに圧縮しても気液平衡線とは交わることがなく、液化は起こらないのである。
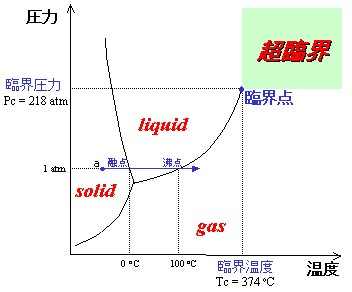
図1 水の相図(P‐T線図)
図2に、水の相挙動を別な表現で表した図を示す。この図は、縦軸に圧力をとり、横軸に体積をとって、各温度における圧力の体積依存性を示している。図中の点線は気液平衡線に相当し、この点線で区切られた下側は、気体と液体が共存する領域である。また、点線の山の頂点が、臨界点に相当する。
例えば、室温のように温度の低い状態(T1)で、気体(圧力が低い)状態から徐々に体積を減少させていくと、圧力は上昇する。やがて、あるところで点線とぶつかり、その後、再び点線と交わるまでは横軸と平衡に移動していく。つまり、この間は体積は小さくなるが、圧力は変わらないことになり、いわゆる「液化」が起こっていることに相当する。液化が終わってから、さらに体積を小さくすると、再び圧力は上昇する。
一方、非常に高い温度(T2)の場合には、等温線は気液平衡線からは遠く離れて、図2の右上に位置する。体積と圧力が反比例に近い関係になることから、等温線は双曲線に近い曲線となる。
では、臨界温度をわずかに上回る温度(T3)で同様の操作を行うとどうなるか。基本的には、液化する場合と似たような等温線になるが、操作する温度が臨界温度を上回っているため、点線とは交わることがなく、気液平衡線のやや上側をかすめるように変化する。その際、体積変化に伴って圧力はわずかずつではあるが単調に上昇し続ける(液化の場合は圧力が一定で変化しない)。すなわち、臨界点(臨界圧力)の近傍では、わずかな圧力変化によって、体積が非常に大きく、しかも連続的に変化するのである。また、体積の逆数が密度であることを考慮すると、密度についても微小な圧力変化で大きく連続的に変わることになる。詳細は後述するが、この特徴は、超臨界水の工学的応用を考える上で、非常に重要な意味を持っているのである。
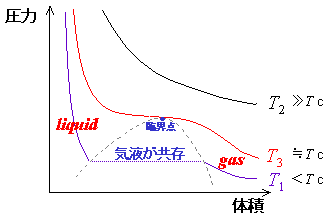
図2 水の相図(P‐V線図)
(2)超臨界水の定義と特徴
一般に、超臨界水とは「温度と圧力がそれぞれ臨界温度、臨界圧力を上回る状態にある水」と定義され、相図(図1)でいうと、臨界点の右上の領域に相当する[3]。このように書くと、超臨界領域に突入した途端に、気体や液体とは異なる「第4の相」が出現することを想像されるかもしれないが、実際には目に見える特別な現象の変化が起こるわけではない[4]。また、先ほども述べたように、臨界点から離れてはるかに高い温度になると、(定義上は超臨界に相当する条件であっても)流体は気体とほぼ同じような振る舞いを示す。その意味では、「超臨界水」とは臨界温度と臨界圧力を超える高温高圧の水の便宜的な呼称であって、(気液平衡線のように)明確な物理的現象の変化に対応した境界によって区別されている訳ではないのである。
では、超臨界状態にある水には、気体や液体の水と比較して、どのような特徴があるのだろうか。超臨界状態の水は、温度が高いため分子が大きな運動エネルギーを持っている(分散力)という点では気体のようでもあり、また圧力が高いため分子同士が集まって安定化する力(凝集力)が働く点では液体のようでもあると言える。従って、超臨界を「気体や液体と似ても似つかない全く別の状態」と考えるよりも、「密度の高い水蒸気」、あるいは「気体と液体の両方の性質、あるいは中間的な性質を持った流体」として捉える方が正しい考え方であろう。実際に、このことは超臨界水の物性値(表1)にも現れており、密度や粘度、拡散係数など、いずれの物性についても、超臨界水は気体と液体の中間的な値をとる。
表1 超臨界水の物性値
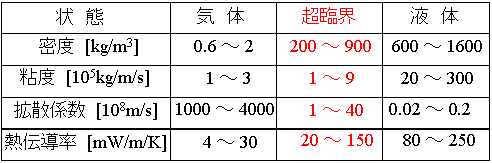
ところが、「超臨界」としての特徴は、ただ物性値が気体と液体の中間であるということだけではない。先ほど、「臨界点近傍の温度では、微小な圧力変化により密度が連続的に大きく変化する」と述べたが、例えば、溶媒として「ものを溶かす」能力(溶解力)などの様々な物性値は、水の密度と密接に相関することが知られている。すなわち、同じ温度であっても、ほんの少し圧力を変えるだけで、溶解力を急激に変化させることができるのである。密度に相関する他の物性値についても同様で、原理的には、圧力と温度だけを操作因子として、様々な水の物性を幅広くコントロールすることが可能になるのである。
このような特徴は、超臨界水に限らず、超臨界流体全般に当てはまる特徴であるが、超臨界水の場合には、さらに興味深い特徴がある。図3に、水のイオン積及び誘電率の温度依存性を示す[5]。ここで、イオン積とは水が解離して生成するH+イオンの濃度とOH-イオンの濃度の積のことで、この値が大きいほど水中に存在するH+やOH-のイオン濃度が高いことを意味している。図3を見ると、イオン積は300℃くらいまで徐々に増加するが、臨界温度付近で急激に減少し、400℃では約10-23となる。例えば、常温の水では、H+の濃度によって酸性とかアルカリ性といった性質が発現するわけだが、高温高圧の状態では、温度の変化に対応して、水の酸(あるいはアルカリ)としての性質も大きく影響を受けるのである。
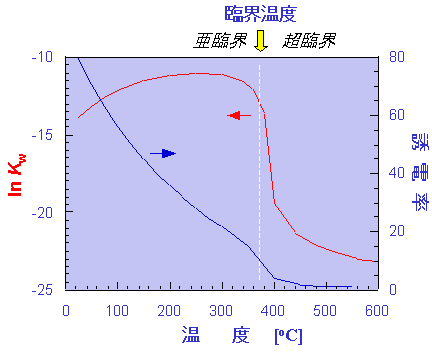
図3 水のイオン積と誘電率の温度変化(25Mpa)
一方、誘電率についても、高温高圧の水は、常温のそれと明らかに異なっている。誘電率とは、溶媒の極性と関係する物性値で、誘電率の大きな状態では、極性の大きな物質(例えば食塩のような無機物)をよく溶かし、逆に極性の小さな物質(多くの有機物など)はほとんど溶解しない。混じり合わないことの比喩で「水と油」といった表現をすることがあるが、これはまさに、常温の水の誘電率が高いこと(約80、図3参照)と関係している。ところが、温度の上昇とともに、誘電率は徐々に減少し、超臨界状態では2~5と非常に小さい値となる。このような状態では、常温の水とは反対に「水と油」はよく混じり合い、逆に無機塩は水にほとんど溶解しないのである。
以上見てきたように、超臨界水は、液体の水や水蒸気とは異なる性質を持ち、しかも温度と圧力を操作することによって、その性質をコントロールすることができるのである。超臨界水を「魔法の水」と呼ぶのは少々大げさかもしれないが、このような特徴をうまく利用することができれば、従来の形態とは異なる、新しい「水の応用」の可能性も十分に期待できるのである。
2-2 超臨界水中の化学反応
「水」はしばしば化学反応の溶媒として用いられる。化学反応における溶媒の役割については、詳しい説明を次章に譲るが、簡単に言うと、溶媒は反応を行う「場」を提供するのである。日常の生活の中でも、物事の進み具合が「場」の雰囲気によって影響を受けることがしばしばあるが、化学反応でも同様に、「場」を作る溶媒の種類や性質によって、化学反応の進み方が直接的あるいは間接的に影響を受けるのである。では、仮に超臨界水を「場」とする反応を行ったとすると、液体の水や水蒸気を「場」とした時の反応と比べて、どのような違いが期待されるのだろうか。
まず始めに、化学反応が進む速度について考えてみる。化学反応が起こるためには、まず反応する分子同士が出会うことが必要である。雑踏の中で待ち合わせをすると、なかなか相手のいるところにたどり着くことができないのと同じで、反応の「場」に存在する分子が多いほど、目的とする分子同士の衝突は起こりにくくなる。少し難しい言い方をすると、密度や圧力が高いほど、拡散が遅くなるのである。
一方、「場」全体で一秒間にどれだけの分子が反応するかを考えれば、当然「場」に存在する反応分子の数が多いほど、全体で反応する回数(確率)も大きくなる。これは、密度や圧力が高いほど、反応の速度が大きくなると言い換えることができる。
この二つの関係を、図で表現したものが、図4である。この図は、拡散の速度及び反応の速度が、密度にどのような影響を受けるかを単純化して表現したものである。図において、右に行くほど密度が高い状態を表しており、例えば、図の左側が気体、右側が液体に相当すると考えてもよい。先に述べたように、拡散の速度は密度の上昇に伴って低下するので、図では右肩下がりの線となる。一方、反応の速度は右肩上がりの線となる。化学反応が出会い(拡散)→反応の手順で起こるとすれば、化学反応全体の速度は、その遅い方の過程の速度で決まってしまうので、この図の場合には、気相においては拡散の速度が、液相においては反応の速度が、それぞれ全体の化学反応の速度を支配することになる[6]。その結果、全体の反応速度には、気相と液相の中間に極大ができると予想される。すなわち、気体と液体の中間である超臨界状態を反応の「場」とすることで、化学反応の速度に極大が現れることが期待できることになる。もちろん現実には、すべての化学反応についてこのような単純なモデルが適用できるわけではないが、ある種の反応では、実際にこのような速度の反転現象が起こることが実証されている。
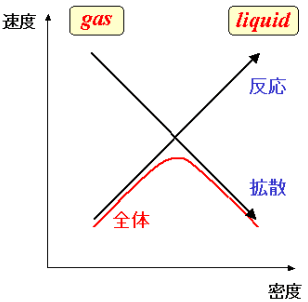
図4 拡散の速度と反応の速度
次に、超臨界水の物性と関連させて、反応の「場」としての特徴を考えてみる。先ほども述べたように、化学反応は「場」の雰囲気に影響を受けることは、溶媒の種類を変えることによって、化学反応の進み方に違いが現れることに相当する。実際、目的とする反応をどのような溶媒中で行うかによって、生成する物質の種類や量が大きく変わる例は少なくない。現在工業化されている多くの化学プロセスでは、生産効率や安全性を高めるために、それぞれの開発段階において、多種多様な溶媒を試行錯誤的(もう少しスマートなやり方かもしれないが)に試験し、その中から最適な溶媒を選定するといった作業が行われてきたことは想像に難くない。
ここに、超臨界水を溶媒として使うことを考えてみよう。まず、(水には限らないが)超臨界流体には、「温度や圧力による物性の連続的変化」という特徴があることは先に述べた通りである。水という単一の物質でも、温度や圧力を操作することにより、溶媒としての物性値を、様々に変化させることができるのである。例えば、石油化学プロセスなどで主要な反応となる有機化学反応などの場合、通常の水では「油」を溶解することができないため、水を反応の溶媒に用いることはあり得ないことになるが、有機物を溶かすことのできる「超臨界水」であれば、少なくとも溶媒中に反応する物質を溶解するといった条件はクリアすることが可能となる。もっと極端に言えば、溶媒の候補として考えられる様々な物質を準備し、それらを順番に試験するといった煩雑な作業の代わりに、水の温度と圧力を変えるだけで、目的にかなった物性を持つ溶媒環境を実現できるのである。また、何より水自体は自然界に豊富に存在する無毒で安価な溶媒である。例えば、溶媒としての能力は高くても毒性の高い有機溶媒などは、使用に際して環境に悪影響を及ぼすリスクや、製品に残存して健康被害を及ぼすリスクなどを考えると、決して好ましい溶媒とは評価されない。今後、環境調和型技術への指向がより一層強まっていくことが予想される中で、「超臨界水」を溶媒とする化学反応は、低リスク・低環境負荷を実現するための基盤技術の一つとして注目されるべきである。
2-3 超臨界水酸化反応
前項では、超臨界水の化学反応の溶媒としての特徴について述べたが、これらの特徴を利用した代表的な技術として、「超臨界水酸化反応」とよばれる有害物質の分解技術が挙げられる。超臨界水酸化反応は、1990年代に入って研究が活発に行われ、新しい廃棄物処理技術として社会的にも注目を集めている技術である。本項では、「超臨界水酸化反応による廃棄物処理」の原理や特徴やなどについて簡単に述べる。
(1)超臨界水酸化反応とは
「超臨界水酸化反応」とは、超臨界条件にある水中で行う酸化反応のことである。例えば「ものが燃える」という現象も酸化反応の一つであり、有機化合物を燃やす(完全に酸化する)と二酸化炭素が生成する。実は、超臨界水酸化反応とは高温高圧の水中で「ものを燃やす」反応なのである。「水中でものが燃える」というと、いささか奇異に聞こえるかもしれないが、実際にほとんどの有機物は、超臨界水酸化反応によって、秒単位の極めて短い時間でほぼ100パーセント完全に分解し、二酸化炭素を生成するのである。
(2)超臨界水酸化反応による廃棄物処理技術の特徴
このように、反応が高速で進行する超臨界水酸化反応を、新しい廃棄物処理技術として利用する研究が活発に行われている。有害な有機物の無害化を目指した水中の酸化反応には、先行技術として「湿式酸化法」と呼ばれる方法がある。「湿式酸化法」とは、分解したい物質(主に有機物)を溶解させた水に、空気中の酸素を溶解させて、液体の水の中で酸化反応を進行させる方法であり、超臨界水酸化と比べて低温、低圧のより温和な条件で行われることが特徴である。この方法の問題点としては、液体の水への有機物の溶解度が低いこと、気相に存在する酸素が液体の水に溶解する過程に時間がかかること、温度が低いため反応の速度が大きくならず[7]、また安定な中間生成物からの酸化が進まないこと[8]、などが指摘されてきた。
これに対し、超臨界水酸化反応による廃棄物処理プロセスの特徴として、次のような点が挙げられる。
ア 反応速度が非常に大きい。
超臨界水は、通常の水に比べて有機物をよく溶かすため、反応する物質の濃度を上げることができる。また、酸素(空気)とも均一に良く混ざるため、湿式酸化法のような気相から液相への溶解を考慮しなくて良い。なにより、反応温度が湿式酸化よりも高いので、反応速度が大きく、完全酸化生成物である二酸化炭素まで酸化が進行する。これらの要因により、湿式酸化法よりも速く完全な無害化処理が可能となるのである。
イ 自らの反応熱で温度を維持することができるため、省エネルギー化が期待できる。
ものが燃えると発熱する。超臨界水酸化反応では、反応の進行に伴って発生する熱(反応熱)だけで、反応温度を維持するために必要な熱エネルギーをまかなうことができる。つまり、水の臨界温度を上回るような高温プロセスであるにもかかわらず、外部からの加熱を必要とせず、反応熱だけで操作温度を維持することができるのである。
ウ 水中の燃焼なので、温度の暴走や爆発などの危険性が低い。
発熱量が大きな物質や爆発性の高い物質を、焼却炉のように空気中で燃焼させると、急激な温度上昇や爆発の危険があることは自明である。これに対し、超臨界水酸化反応は、基本的に比熱の大きな水が大量に存在する中での反応なので、仮に燃焼に伴う発熱が起こったとしても、水によってエネルギーが「吸収」され、温度の暴走や爆発が起こる危険性は低いことが期待される。
エ 排ガスの処理が不要となり、省スペース化が期待できる。
超臨界水酸化反応では、通常の燃焼プロセスで発生するNOxやSOxといった有害なガスがほとんど発生しないことが特徴である。従って、通常の焼却法では必要不可欠である排ガス処理工程を大幅に省略することができ、煙突を必要としないコンパクトな装置ですむことになる。特に都市部のように地価の高い地域では、省スペース化は処理コストの削減に直結する大きなメリットとなりうるのである。
(3)本技術に用いられる反応器の例(MODARプロセス)
超臨界水酸化反応に用いられる反応器の例を図5に示す。この反応器はMODAR型反応器と呼ばれるもので、超臨界水の特徴を考慮して、いくつかの優れた設計が施されている。
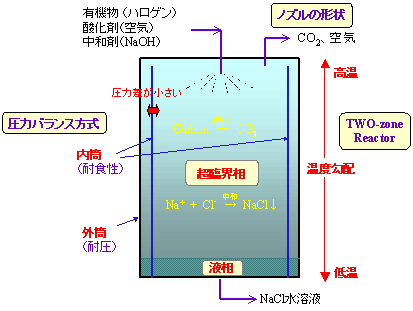
図5 MODAR型反応器の特徴
反応器には、溶媒となる「水」、分解したい「有機物」、酸化剤である「空気(酸素)」が、ノズルを通じて反応器上部から導入される。有機物がハロゲンを含んでいる場合には、その中和剤としてアルカリ(主に水酸化ナトリウムが用いられる)水溶液も一緒に導入される。反応器の上部は臨界温度を超える温度になっているので、ノズルから吹き出された
混合物は、瞬時に超臨界水酸化反応が起こる条件に達する。有機物は短時間で二酸化炭素まで酸化され、反応に関係しなかった空気などと一緒に、反応器上部の出口から排出される。ここで、ノズルの形状には高度な工夫が施されており、導入された有機物の完全分解に必要かつ十分な時間だけ反応器にとどまるような工夫がなされている。また、ハロゲンは中和剤のアルカリと反応して、塩を生成する。
MODAR型反応器の大きな特徴の一つに、生成する塩の回収方法が挙げられる。例えば塩素原子を含むような有機物を分解する場合には、中和剤である水酸化ナトリウムなどのアルカリと反応し、塩化ナトリウムなどの塩を生成するが、前述の通り、超臨界水には無機物が溶解しにくいため、反応器全体が超臨界状態の水であれば塩の析出が起こってしまうことになる。この問題を解決するために、MODAR反応器では、反応器の上下方向に温度勾配がつけられている。つまり、反応器上部が超臨界水、下部が液体の水となり、同一の反応器に、性質が異なる二つの「場」を設けているのである[9]。このような工夫によって、超臨界部で生成した塩を下部に落とし、液体の水に溶解させることによって、水溶液として回収するのである。
もう一つの特徴として、圧力バランス方式と呼ばれる二重管構造が挙げられる。これはハロゲンによる腐食を防ぐための対策である。ハロゲンを含む有機物を処理する場合、反応器が腐食される可能性があるため、反応器の材質を慎重に選ぶ必要があるが、一般に耐腐食性に富んだ材料は、機械的強度が低く、高価であるため、そのような材料で反応器全体を作製することはコスト的に難しく、安全性にも乏しい。これに対し、MODAR反応器では、反応器全体(外側)に耐圧性の高い材料を、また腐食環境にさらされる内筒に耐食性の高い材料をそれぞれ用い、さらに内筒と外筒の間に反応圧力よりも少しだけ高い圧力の空気を充填している。このような工夫により、外筒が腐食性の環境に触れる心配がなく、また内筒には差圧分しか圧力がかからないため、高価な材料の使用量を抑えることができるのである。
(4)本技術の適用例
超臨界水酸化反応を用いた廃棄物の処理や無害化については、これまでの数多くの基礎研究が行われており、ほとんどの有機化合物について非常に高い効率で完全に分解無害化できることが実証されてきた。特に、酢酸やフェノール、アンモニアといった有害物質は、化学的に安定であるため分解しにくい物質として知られているが、これらの物質についても、処理条件は若干厳しくなるものの技術的には十分に適用可能であることが明らかにされている。これらの基礎的研究の裏付けをもとに、実際の排水や廃棄物への応用についても検討が進められており、これまでに、化学工場の廃液や半導体工場の洗浄水などの工業廃水に対して、この技術を用いた処理が実用化された例がある。また、生活排水や下水汚泥などへの適用や、ダイオキシンやPCBなどの内分泌攪乱物質(いわゆる環境ホルモン)の分解についても、研究が進められている。
大学や研究機関などで行われる研究を通じて発生する実験廃液や廃棄物についても、超臨界水酸化技術の新しい適用対象の一つと考えられる。近年の科学技術の深化と多様化に対応して、大学などの研究機関において行われる研究も、新規な物質や技術の開発を目指す傾向にある。これに呼応して、扱われる化学物質も必然的に多様化するため、実験廃棄物についても、毒性の高い物質を含む複雑多種にわたる化学物質の混合物として発生する傾向が強まりつつある。しかも、これらの研究機関から排出される廃液処理量は、工業廃水と比較すると少量であるため、大規模な処理設備を作ることは必ずしも経済的に得策とは言えない。環境汚染の深刻化に対応して、様々な法的規制も厳しくなる現状を考えると、大学等の研究機関から発生する微量な有害化学物質を、排出される場所において完全かつ効率よく無害化できる技術を開発することは、廃棄物対策の原則である原点処理の観点からも重要であると言える。今後、廃棄物処理対策は大規模集約型から小規模分散型に方針転換されることが予想されるが、超臨界水酸化反応は、その方向性にかなう対策技術の一つとして期待される[10]。
(5)本技術の課題
以上述べたように、廃棄物の分解、無害化に有効な手法として期待される超臨界水酸化技術であるが、より実用的な技術に向けて、解決すべき課題も残されているのが現状である。
超臨界水酸化反応は、基本的に有機化合物を対象とする反応であるため、従来焼却によって処理されてきた廃棄物に対しては十分に有効であるが、無機化合物をベースとする廃棄物の処理には必ずしも適した方法とは言えない。また、水中に微量に含まれる有害物を高速かつ完全に無害化することは得意であるが、処理量が大きい対象や濃度が高い廃液などの大規模な処理は必ずしも得意ではない。このような系については、他の処理方法と組み合わせて用い、前段階で無害化しきれない部分を超臨界水酸化によって補完するような処理システムで対応することになろう。
耐圧や耐腐食性材料の開発や、高温・高圧で操作することのできる機器(圧縮機、ポンプ、熱交換器など)など、装置面での開発が遅れていることも、実用化を推進する上での課題の一つである。また、高圧を扱うことによる厳しい法的規制が、技術の汎用化にハードルとなっていることも事実である。
技術的に見ると、反応に及ぼす添加物や混合物の影響といった工学的情報が、必ずしも十分に整備されていない点が挙げられる。これらの知見は、実装置の設計において必要不可欠な情報であり、実験的なデータの蓄積と体系化を目指した研究の進展が望まれる。さらに、高温高圧という厳しい反応条件を緩和して、より効率的で安全性の高い技術に改良するための工夫が必要である。例えば、固体触媒などを導入することによって、操作温度の低温化が可能になれば、省コストや省エネルギー、安全性や装置の耐久性の向上などにつながり、この技術の汎用化に大きく貢献すると考えられる。
2-4 超臨界水を用いた環境調和型技術
前項では、新規な廃棄物処理技術としての「超臨界水酸化反応」について紹介したが、超臨界水の特徴を利用し、近年の環境問題に適応した新技術の開発が、広い範囲にわたって活発に進められている。図6には、環境調和型の新しい技術として「超臨界水」の応用が期待できるいくつかの例を示してある。先ほど紹介した超臨界水酸化反応による廃棄物処理や、有機塩素化合物などの汚染物質を土壌から抽出・分離する技術は、有害化学物質によって汚染された環境を修復するための技術として特徴づけられる。また、質の低い石炭など未利用化石燃料を超臨界水中で燃焼させ発電に利用する技術や、バイオマスを超臨界水中でガス化し、水素としてエネルギー回収を計る技術などは、エネルギー問題に対する新技術の開発を目指したアプローチである。PETやポリウレタンなどのポリマーを超臨界水中で分解してモノマーを回収する技術は、ケミカルリサイクルの形で資源の有効利用を目指す研究として位置づけられる。この他、超臨界水における無機物の溶解度の変化を利用した晶析や微粒子合成なども、超臨界水の特徴をうまく利用した新しい機能材料合成技術として注目される。
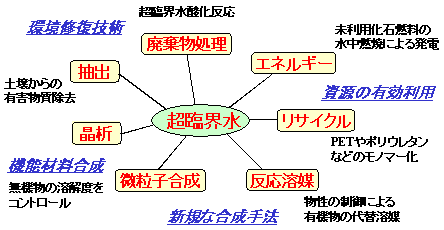
図6 超臨海水の応用が期待される環境調和型技術
このように、「超臨界水」を利用した環境調和型技術が、幅広い分野に渡って検討されている。現在、化学工学の分野を中心に、個々のシーズ技術を実用的なプロセスに展開するための技術的検討が行われている一方、これらの技術の共通基盤となる要素技術の整備や体系化が積極的に進められている。高温高圧という特殊な環境であるとはいえ、「水」でありながら固体、液体、気体とは全く異なる性格を発現する「超臨界水」は十分魅力的であり、持続的社会を実現するための基盤技術の一つとして大いに期待される。
(参考文献)
1.「超臨界流体の科学と技術」(齋藤 正三郎監修)、三共ビジネス(1996).
2.「超臨界流体反応法の基礎と応用」(碇屋 隆雄監修)、シーエムシー出版(1998).
3.「超臨界流体のすべて」(荒井 康彦監修)、テクノシステム(2002).
[1] 0℃において横切った線は「固-液平衡線」と呼ばれる。
[2] 臨界点に相当する条件での水の体積、密度を、それぞれ「臨界体積」、「臨界密度」という。水の場合、臨界体積は56.3cc/mol、臨界密度は0.32g/ccである。
[3] ちなみに、温度か圧力のいずれか一方が臨界値を超えている状態を、亜臨界状態と呼ぶことがある。
[4] 厳密に言うと、見た目にも変化が起こり、流体がゆらゆらとかげろうのようにゆれて見えると言われている。また、臨界点に極めて近い条件では、光が全く透過しなくなる(臨界タンパク光と呼ばれる)現象が起こる。これらはいずれも光の散乱に起因する。すなわち、超臨界(特に臨界点に近い)条件にある流体をミクロ的に見ると、局所的に分子が集まってクラスターと呼ばれる密度の高い状態ができるため、いわば流体に不均一性(ムラ)が生じ、光散乱が起こるのである。
[5] 水中では、水分子(H2O)のごく一部がイオンに解離してH+とOH-の形で存在しているが、イオン積とはH+とOH-の濃度の積のことであり、この値が大きいほどイオンに解離しているものの割合が高いことになる。室温付近の水は、水1リットル中にH+とOH-がそれぞれ10-7モルあるので、イオン積は10-14となる。
[6] 複数の過程が連続して(逐次的に)起こり、そのうちの一つが非常に時間のかかる過程だったとする。その場合、全体に要する時間はその時間のかかる過程に依存し、他の過程に要する時間は無視できる。このように、全体の速度を決めるような遅い過程のことを「律速過程」という。本文で、拡散の速度が全体の速度を支配することを「拡散律速」、反応の速度が全体の速度を支配することを「反応律速」という。
[7] 通常の化学反応は、温度が高いほど速く進む。超臨界水酸化反応では、処理速度が秒のオーダーであるのに対し、湿式酸化法では、分~時間のオーダーで進行する。
[8] 湿式酸化法の場合、多くの有機化合物は、酢酸までは酸化されるが、酢酸が安定な化合物であるために二酸化炭素まで酸化されにくく、結果として酢酸の生成割合が高くなる。湿式酸化法では、酢酸からの酸化を促進するために、触媒を用いるのが通常である。
[9] 二つの「場」を作っていることから、MODAR反応器は「Two-zone reactor」と呼ばれている。
[10] このような背景をふまえ、2002年東京大学において、超臨界水酸化技術を用いた「実験廃棄物処理施設」が建設されることになった。この施設は、実験廃棄物を超臨界水酸化プロセスで処理する初めての試みであり、世界に先駆けた国産環境技術の開発という観点からも注目される。
お問合せ先
科学技術・学術政策局政策課
-- 登録:平成21年以前 --