- 現在位置
- トップ > 科学技術・学術 > 研究費、研究開発評価 > 文部科学省の競争的資金一覧 > 科学研究費補助金 > 科学研究費補助金「特別推進研究」の追跡評価(試行)について > 「特別推進研究」研究期間終了後の効果・効用、波及効果に関する自己評価書
「特別推進研究」研究期間終了後の効果・効用、波及効果に関する自己評価書
- 研究代表者氏名
佐方 功幸(九州大学・大学院理学研究院・教授) - 研究分担者氏名
中條 信成(九州大学・大学院理学研究院・助手)
古野 伸明(九州大学・大学院理学研究院・助手) - 研究課題名
「初期発生における細胞周期制御の研究」 - 課題番号
10102009 - 補助金交付額(直接経費のみ)
平成10年度 57,000千円 平成11年度 51,000千円 平成12年度 54,000千円 平成13年度 45,000千円 平成14年度 45,000千円
【研究期間終了後の効果・効用、波及効果に関する内容】
1.特別推進研究の研究期間終了後、研究代表者自身の研究がどのように発展したか。
特別推進研究によってなされた研究が、本書類作成時点までの間にどのように発展しているか、次の(1)~(4)の項目ごとに具体的かつ明確に記述してください。
(1)概要
平成10年度から平成14年度まで、九州大学大学院理学研究院において、ツメガエル卵を用いて「初期発生における細胞周期制御の研究」という研究課題で特別推進研究を行なった。その後、同研究機関において、同じくツメガエル卵を用いて特別推進研究でなされた研究を発展させてきた。具体的には、特別推進研究で得られた発見・知見を元に、in vivo(発生系)およびin vitro(無細胞系)の系で、様々な細胞周期制御因子(Wee1,Plk,Mosなど)やチェックポイント制御因子(Chk1,Cdc25Aなど)の構造と機能およびそれらの制御機構を解析してきた。そして、その結果得られた新たな発見や知見をEMBO,PNAS,Nature誌等に発表してきた。現在では、これらの研究に加え、神経分化や細胞老化における細胞周期制御の研究も推進している。
(2)論文発表、国際会議等への招待講演における発表など
論文発表(原著論文)
- Furuno, N. Kawasaki, A. Sagata, N. Expression of cell-cycle regulators during Xenopus oogenesis. Gene Expr. Patterns, 3, 165-168 (2003).
- Goda, T., Nakajo, N., Sagata, N. Kobayashi, H. The RRASK motif in Xenopus cyclin B2 is required for the substrate recognition of Cdc25C by the cyclin B-Cdc2 complex. J. Biol. Chem., 278, 19032-19037 (2003).
- Yoshitome, S., Furuno, N., Hashimoto, E. Sagata, N. The C-terminal seven amino acids in the cytoplasmic retention signal region of cyclin B2 are required for normal bipolar spindle formation in Xenopus oocytes and embryos. Mol. Cancer Res., 1, 589-597 (2003).
- Yoshitome, S., Nakamura, H., Nakajo, N, Okamoto, K., Sugimoto, I., Kohara, H., Kitayama, K., Igarashi, K. Ito, S. Sagata, N., Hashimoto, E. Mr 25,000 protein (pp25), a substrate for protein Ser/Thr kinase, is identified as a part of Xenopus laevis vitellogenin B1. Dev. Growth & Differ., 45, 283-294 (2003).
- Katsuragi, Y., Sagata, N. Regulation of Chk1 by autoinhibition and ATR-mediated phosphorylation. Mol. Biol. Cell, 15, 1680-1689 (2004).
- Uto, K., Inoue, D., Shimuta, K., Nakajo, N., Sagata, N. Chk1, but not Chk2, inhibits Cdc25 phosphatases by a novel common mechanism. EMBO J., 23, 3386-3396 (2004).
- Kanemori, Y., Uto, K., Sagata, N. β-TrCP recognizes a previously undescribed nonphosphorylated destruction motif in Cdc25A and Cdc25B phosphatases. Proc. Natl. Acad. Sci. USA, 102, 6279-6284 (2005).
- Inoue, D. Sagata, N. The Polo-like kinase Plx1 interacts with and inhibits Myt1 after fertilization of Xenopus eggs. EMBO J., 24, 1057-1067 (2005).
- Ohe, M., Inoue, D., Kanemori, Y., Sagata, N. Erp1/Emi2 is essential for the meiosis
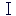 to meiosis
to meiosis  transition in Xenopus oocytes. Dev. Biol., 303, 157-164 (2007).
transition in Xenopus oocytes. Dev. Biol., 303, 157-164 (2007). - Okamoto, K., Sagata, N. Mechanism for inactivation of the mitotic inhibitory kinase Wee1 at M phase. Proc. Natl. Acad. Sci. USA, 104, 3753-3758 (2007).
- Inoue, D., Ohe, M., Kanemori, Y., Nobui, T., Sagata, N. A direct link of the Mos- MAPK pathway to Erp1/Emi2 in meiotic arrest of Xenopus eggs. Nature, 446, 1100-1104 (2007).
- Setoyama, D., Yamashita, M., Sagata, N. Mechanism of degradation of CPEB during Xenopus oocyte maturation. Proc. Natl. Acad. Sci. USA 104, 18001-18006 (2007).
- Ueno,H., Nakajo, N., Watanabe,M., Isoda, M. Sagata, N. FoxM1-driven cell division is required for neuronal differentiation in early Xenopus embryos. Nature Cell Biol., submitted.
- Isoda, M., Kanemori, Y., Sagata, N. The ERK-MAPK pathway phosphorylates and targets Cdc25A/Cdc25B phosphatases for SCFβ-TrCP-dependent degradation. EMBO J., submitted.
論文発表(邦文総説等)
- 佐方功幸,志牟田健,宇都克裕,井上大悟,中條信成(2003)初期発生における細胞周期のチェックポイント制御.「細胞周期研究の新局面」(野島博,中山敬一,田矢洋一 編)実験医学増刊 21,48-54.(羊土社)
- 宇都克裕,志牟田健,中條信成,井上大悟,佐方功幸(2004)チェックポイント制御と初期発生に依存したCdc25Aの分解とその機構.「タンパク質修飾・分解と細胞機能」(田中啓二,西道隆臣 編)実験医学増刊 22,213-218.(羊土社)
- 佐方功幸(2004)初期胚発生における細胞周期・増殖の制御.「発生における細胞増殖制御」(竹内隆,岸本健雄 編)40-50.(シュプリンガー・フェアラーク東京)
- 井上大悟、佐方功幸(2005)卵減数分裂周期の制御機構.「キーワードで理解する細胞周期イラストマップ」(中山敬一 編)109-115.(羊土社)
- 佐方功幸(2005)減数分裂の制御機構:その核心に迫る.「細胞周期研究の最先端」(中山敬一 編)実験医学増刊 23,124-129.(羊土社)
- 井上大悟、兼森芳紀、佐方功幸(2005)卵減数分裂を特徴づける細胞周期制御.「細胞周期研究の最先端」(中山敬一 編)実験医学増刊 23,150-158.(羊土社)
- 兼森芳紀、佐方功幸(2005)SCFβ-TrCPによって認識される非リン酸化型分解モチーフの発見.細胞工学 24,708-709.(秀潤社)
- 兼森芳紀、佐方功幸(2006)SCFβ-TrCPによる細胞周期/チェックポイント因子の制御. 蛋白質核酸酵素増刊 51,1386-1390.(共立出版)
- 大江宗理、井上大悟、佐方功幸(2007)未受精卵における分裂停止のしくみを解明.メディカルバイオ 7月号,16-17(オーム社)
- 井上大悟、大江宗理、佐方功幸(2007)ツメガエル未受精卵における第二減数分裂中期停止の機構解明.細胞工学 26,924-926(秀潤社)
- 佐方功幸(2007)細胞周期と細胞分裂.「医学のための細胞生物学」(永田和宏・塩田浩平 編)印刷中(南山堂)
国際会議への招待講演における発表
- Noriyuki Sagata: Regulation of Chk1 by autoinhibition and ATR-mediated phosphorylation. COE International Symposium(大津市)(2003年11月)
- Noriyuki Sagata: Chk1 regulation of Cdc25A in Xenopus embryos. UK-Japan Cell Cycle Meeting(奈良)(2004年4月)
- Noriyuki Sagata: Checkpoint control of the midblastula transition in Xenopus. 10th International Xenopus Meeting (Woods Hole, Massachusetts, USA)(2004年9月)
- Noriyuki Sagata: Inactivation of Myt1 by Plk1 upon fertilization of Xenopus eggs. EMBO Workshop “Meiotic Divisions and Checkpoints”(Corsica, France)(2005年3月)[都合により出席不可]
その他、国内会議での招待講演、国内外学会での発表
- 国内会議での招待講演・・・計13件
- 国内外学会発表・・・計40件
(3)研究費の取得状況(研究代表者として取得しているもののみ)
科学研究費補助金(文部科学省)
- 研究種目名
- 特定領域研究(細胞増殖制御)
- 研究課題名
- 初期発生における正および負の細胞周期制御の研究
- 研究期間
- 平成19年度~平成23年度
- 研究期間全体の配分額
- 1億3,650万円
他の研究費
- 制度担当府省
- 独立行政法人 科学技術振興機構
- 制度名
- 戦略的創造研究推進事業(CREST(クレスト))
- 研究課題名
- 細胞周期/チェックポイント制御たんぱく質の構造と機能の解析
- 研究期間
- 平成15年度~平成20年度
- 研究期間全体の配分額
- 2億8,210万円
(4)特別推進研究の研究成果を背景に生み出された新たな発見・知見
特別推進研究の成果を元に新たな発見、知見が数多くあったが、以下にその代表的なものついて記す。
<<チェックポイントキナーゼChk1によるCdc25Aの新規阻害機構の発見>>
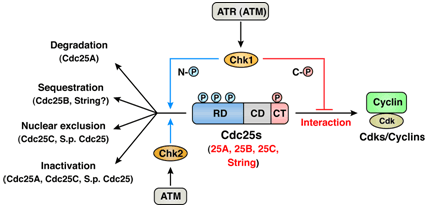
Cdc25ホスファターゼは、サイクリン依存性キナーゼ(Cdks)を活性化することで、細胞周期の進行を促進させる役割を持っている。脊椎動物では、DNA傷害等に応答し、Chk1とChk2がCdc25AのN末端領域をリン酸化し、その分解を誘導する。本研究で、Chk1,Chk2の内Chk1のみがツメガエルCdc25AのC末端(Thr504)をリン酸化し、同ホスファターゼと様々なCdk-サイクリンとの相互作用を阻害することが明らかになった。重要なことに、この阻害はCdc25Aの分解よりも早く起こり、複製チェックポイントでより必須の役割を果たすことが判明した。更に、ヒトから酵母までの他の様々なCdc25にもThr504に相当する部位が存在し、これらのChk1によるリン酸化でも様々なCdk-サイクリンとの相互作用が阻害されることが分った。以上の結果から、Chk1が様々なCdc25を新規の共通機構で阻害することが初めて明らかになった(EMBO J., 2004に掲載)。
<<SCFβ-TrCPユビキチンリガーゼによって認識される非リン酸化型分解モチーフの発見>>
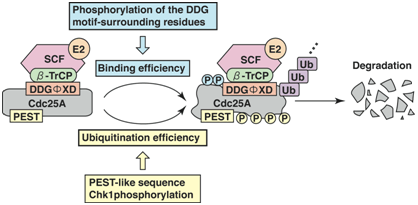
SCFβ-TrCPユビキチンリガーゼのF-boxタンパク質であるβ-TrCPは様々な基質中の2重にリン酸化されたDSGモチーフ(DpSGΦXpS)を認識する。β-TrCPはヒトCdc25AのDSGモチーフにもChk1依存的なリン酸化で結合する。本研究で、ツメガエルおよびヒト両方のCdc25Aが、β-TrCPによって認識される、新規な非リン酸化型DDGモチーフ(DDGΦXD)を持つことが明らかになった。DDGモチーフはツメガエルCdc25Aの唯一の機能的β-TrCP結合部位であり、ヒトCdc25Aでも重要な結合部位であることが判明した。また、DDGモチーフはヒトCdc25Bを含む他種の様々なタンパク質にも存在し、それらの機能的β-TrCP結合部位であることが分った。更に、これらのタンパク質のユビキチン化にはβ-TrCPの結合のみでなく、他の領域やリン酸化も必要なことが判明した。この研究で、β-TrCPが非リン酸化型DDGモチーフも認識することが初めて示された(PNAS, 2005に掲載)。
<<脊椎動物未受精卵の分裂停止におけるMos/MAPK経路の標的の同定>>
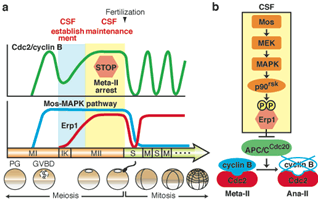
脊椎動物の未受精卵は第二減数分裂中期(Meta-![]() )で停止している。このMeta-
)で停止している。このMeta-![]() 停止にはMos/MAPKキナーゼ経路が関与しているが、その最終標的は長い間不明であった。最近、ツメガエル卵のMeta-
停止にはMos/MAPKキナーゼ経路が関与しているが、その最終標的は長い間不明であった。最近、ツメガエル卵のMeta-![]() 停止にErp1(サイクリンBのユビキチンリガーゼAPC/Cの阻害因子)が直接的に関わっていることが示されたが、Mos/MAPK経路とは独立に働くとされた。しかし、本研究で、予想に反し、Mos/MAPK経路がErp1を標的にしていることが判明した。すなわち、Mos/MAPK経路の下流キナーゼp90rskがErp1を直接的にリン酸化し、その安定性や活性を亢進させることでMeta-
停止にErp1(サイクリンBのユビキチンリガーゼAPC/Cの阻害因子)が直接的に関わっていることが示されたが、Mos/MAPK経路とは独立に働くとされた。しかし、本研究で、予想に反し、Mos/MAPK経路がErp1を標的にしていることが判明した。すなわち、Mos/MAPK経路の下流キナーゼp90rskがErp1を直接的にリン酸化し、その安定性や活性を亢進させることでMeta-![]() 停止(APC/Cの阻害)を引き起こすことが示された。また、Mos/MAPK/p90rsk/Erp1経路が第一及び第二減数分裂の転移にも必須であることが示された。これらの研究で、永年の謎であったMeta-
停止(APC/Cの阻害)を引き起こすことが示された。また、Mos/MAPK/p90rsk/Erp1経路が第一及び第二減数分裂の転移にも必須であることが示された。これらの研究で、永年の謎であったMeta-![]() 停止の分子経路が明らかになった(Nature, 2007に掲載)。
停止の分子経路が明らかになった(Nature, 2007に掲載)。
<<FoxMIの神経前駆細胞の増殖及び分化への関与の発見>>
この研究はごく最近なされたものであり、転写因子FoxMIがツメガエル胚の神経板に特異的に発現し、神経前駆細胞の増殖・分化に関与することを明らかにした(Nature Cell Biol.に投稿中)。
2.特別推進研究の研究成果が他の研究者による活用された状況はどうか。
本書類作成時点までの間に、特別推進研究の研究成果が他の研究者に活用された状況について、次の(1)、(2)の項目ごとに具体的かつ明確に記述してください。
(1)学界への貢献の状況
特別推進研究で得られたツメガエル卵での成果をいくつかに分類し(A~F)、それぞれのその後の学界へのインパクトや貢献について以下に記す。
- 卵減数分裂周期への核内物質の必要性(Iwashita et al., PNAS, 1998)
この研究では卵母細胞の核内物質の卵減数分裂周期への必須な役割を示したが、その後他のグループによってラット、マウス、ブタ等でも検証され、その役割のモデルが一般的に受入れられつつある。 - 卵母細胞におけるChk1の活性とその局在性及び機能制御(Nakajo et al., Dev.Biol., 1999; Oe et al., Dev.Biol., 2001)
これらの研究では、Chk1がその基本活性(Cdc25の阻害)によって卵母細胞の第一減数分裂(Pro-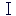 )に関与していること、その経路が細胞質のみで起こること、またChk1の基本活性が自己抑制的に制御されることを示した。これらの結果は、その後の(PKA等による)Pro-
)に関与していること、その経路が細胞質のみで起こること、またChk1の基本活性が自己抑制的に制御されることを示した。これらの結果は、その後の(PKA等による)Pro-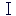 停止のより詳細な分子機構の解明、(ヒト細胞を含む)正常細胞周期におけるChk1の役割、及びそのチェックポイント時における活性制御機構の解明等に有意に寄与した。
停止のより詳細な分子機構の解明、(ヒト細胞を含む)正常細胞周期におけるChk1の役割、及びそのチェックポイント時における活性制御機構の解明等に有意に寄与した。 - Nek2の新規アイソフォームの発見とその中心体形成への関与(Uto et al., Dev. Biol., 1999; Uto and Sagata, EMBO J., 2000)
これらの研究では、中心体キナーゼであるNek2に母性型と胚性型のスプライス変異体(それぞれNek2B,Nek2Aと命名)が存在することを初めて示し、Nek2BはNek2Aより代謝的に安定で卵割時の中心体形成に関与することを示した。この研究の後、ヒト/マウスを含みNek2A,Nek2Bの用語が一般的に使われるようになり、それらの機能差や発現(分解)制御機構の解明につながり、本研究の成果は中心体サイクルの理解に大きく貢献した。 - Wee1のアイソフォームの発見とその初期発生細胞周期制御への関与(Nakajo et al., Gene & Dev., 2000; Okamoto et al., EMBO J., 2002)
これらの研究では、Cdc2の阻害因子Wee1に母性型と胚性型(それぞれWee1A,Wee1Bと命名)が存在し、Wee1Aの発現制御が卵減数分裂制御に、Wee1Bのそれが原腸胚以降の体細胞分裂制御に関わることを示した。また、Wee1BはWee1Aより代謝的に安定であることを示した。これらの成果は、その後の(マウス卵等を含む)Wee1Aの卵減数分裂における役割及び発現制御機構の解明、(ヒトを含む)Wee1Bの体細胞における活性及び発現(分解)制御機構の解明等に少なからぬ貢献をした。 - 中期胞胚遷移(MBT)におけるDNA複製チェックポイントのChk1による制御(Shimuta et al., EMBO J., 2002)
本研究では、中期胞胚遷移(MBT)における複製チェックポイントでChk1が一過性に活性化し、Cdc25Aを直接リン酸化し、分解誘導することを示した。この研究は、生理な複製チェックポイント下で実際にChk1が活性化すること、Chk1がCdc25Aを直接リン酸化・分解誘導することを初めて示したものである。この研究成果は、その後の(ショウジョウバエ等を含む)発生過程における生理的なチェックポイントにおけるChk1の役割の解明、(ヒト細胞を含む)Chk1によるCdc25Aのリン酸化部位の同定、その活性及び分解の制御機構の解明等々、一般的なチェックポイント制御の理解に大きく寄与した(これらの先駆けとなるmini review: N Sagata, Science, 2002を参照)。 - 受精時におけるMos mRNA(伝令リボ核酸)の翻訳制御(Ueno and Sagata, Dev. Biol., 2002)
本研究では、受精時におけるMos mRNA(伝令リボ核酸)の翻訳停止にAUUUAモチーフが関わっていることを明らかにした。AUUUAモチーフは一般にmRNA(伝令リボ核酸)の分解に関わるが、本成果は、同モチーフが翻訳停止にも関わることを初めて示したものとしてreview誌での引用が多く、今後の関連分野への貢献が期待される。
(2)論文引用状況
以下、特別推進研究の研究期間中と終了後の論文の「要旨」と「引用数」を、それぞれ上位10報程度(年代順)のものについて記す。
調査日 2007年12月25日
研究期間中に発表された論文
- Iwashita, J. Hayano, Y., Sagata, N. Essential role of germinal vesicle material in the meiotic cell cycle of Xenopus oocytes. Proc. Natl. Acad. Sci. USA, 95, 4392-4397 (1998). 「ツメガエル卵母細胞の卵核胞(核)内容物が卵減数分裂周期に必須であることを示した論文」25件
- Yoshitome, S. Furuno, N., Sagata, N. Overexpression of the cytoplasmic retention signal region of cyclin B2, but not of cyclin B1, inhibits bipolar spindle formation in Xenopus oocytes. Biol. Cell, 9, 509-518 (1998). 「サイクリンB2の細胞質保留シグナルがツメガエル卵の二極性紡錘体形成に必要なことを示した論文」20件
- Nakajo, N. Oe, T. Uto, K. Sagata, N. Involvement of Chk1 kinase in prophase I arrest of Xenopus oocytes. Dev. Biol., 207, 432-444 (1999). 「Chk1がCdc25の阻害を介してツメガエル卵母細胞のPro-
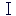 停止に必要なことを示した論文」37件
停止に必要なことを示した論文」37件 - Uto, K. Nakajo, N. Sagata, N. Two structural variants of Nek2 kinase, termed Nek2A and Nek2B, are differentially expressed in Xenopus tissues and development. Dev. Biol., 208, 456-464 (1999). 「Nek2に2つのスプライス変異体があり、ツメガエル組織、発生で異なる発現をすることを示した論文」26件
- Nakajo, N. Yoshitome, S. Iwashita, J. Iida, M. Uto, K. Ueno, S. Okamoto, K. Sagata, N. Absence of Wee1 ensures the meiotic cell cycle in Xenopus oocytes. Genes & Dev., 14, 328-338 (2000). 「Wee1の第一減数分裂期における欠如がツメガエル卵減数分裂の進行に必要なことを示した論文」61件
- Uto, K., Sagata, N. Nek2B, a novel maternal form of Nek2 kinase, is essential for the assembly or maintenance of centrosomes in early Xenopus embryos. EMBO J., 19, 1816-1826 (2000). 「母性型Nek2(Nek2B)がツメガエル卵割期の中心体形成に必要なことを示した論文」49件
- Oe, T., Nakajo, N., Katsuragi, Y., Okazaki, K., Sagata, N. Cytoplasmic occurrence of the Chk1/Cdc25 pathway and regulation of Chk1 in Xenopus oocytes. Dev. Biol., 229, 250-261 (2001). 「ツメガエル卵Pro-
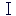 停止においてChk1が細胞質内でCdc25を阻害することを示した論文」30件
停止においてChk1が細胞質内でCdc25を阻害することを示した論文」30件 - Okamoto, K., Nakajo, N., Sagata, N. The existence of two distinct Wee1 isoforms in Xenopus: implications for the developmental regulation of the cell cycle. EMBO J.,21, 2472-2484 (2002). 「Wee1に母性型と胚性型があり、後者がツメガエルッ原腸胚以降に機能することを示した論文」19件
- Shimuta, K., Nakajo, N., Uto, K., Hayano, Y., Okazaki, K., Sagata, N. Chk1 is activated transiently and targets Cdc25A for degradation at the Xenopus midblastula transition, EMBO J., 21, 3694-3703 (2002). 「Chk1がツメガエル胚のMBTで一過性に活性化し、Cdc25Aのリン酸化・分解誘導を引き起こすことを示した論文」45件
- Ueno, S., Sagata, N. Requirement for both EDEN and AUUUA motifs in translational arrest of Mos mRNA upon fertilization of Xenopus eggs. Dev. Biol., 250, 156-167 (2002). 「Mos mRNA(伝令リボ核酸)のAUUUAモチーフがツメガエル卵受精時での翻訳停止に必要なことを示した論文」13件
- Sagata, N. Untangling checkpoints. Science, 298, 1905-1907 (2002). 「DNA傷害・複製チェックポイント時におけるChk1・Chk2によるCdc25Aの分解誘導機構に関するミニレビュー」13件
研究期間終了後に発表された論文
- Furuno, N. Kawasaki, A. Sagata, N. Expression of cell-cycle regulators during Xenopus oogenesis. Gene Expr. Patterns, 3, 165-168 (2003). 「ツメガエル卵形成における様々な細胞周期制御因子の発現パターンに関する論文」4件
- Yoshitome, S., Nakamura, H., Nakajo, N, Okamoto, K., Sugimoto, I., Kohara, H., Kitayama, K., Igarashi, K. Ito, S. Sagata, N., Hashimoto, E. Mr 25,000 protein (pp25), a substrate for protein Ser/Thr kinase, is identified as a part of Xenopus laevis vitellogenin B1. Dev. Growth & Differ., 45, 283-294 (2003). 「これまでツメガエル卵でpp25として知られていた蛋白をビテロゲニンB1として同定した論文」8件
- Katsuragi, Y., Sagata, N. Regulation of Chk1 by autoinhibition and ATR-mediated phosphorylation, Mol. Biol. Cell, 15, 1680-1689 (2004). 「Chk1の活性が自己抑制とATRによるリン酸化で制御されることを示した論文」13件
- Uto, K., Inoue, D., Shimuta, K., Nakajo, N., Sagata, N. Chk1, but not Chk2, inhibits Cdc25 phosphatases by a novel common mechanism, EMBO J., 23, 3386-3396 (2004). 「Chk1,Chk2のうちChk1のみが様々なCdc25種のC末端をリン酸化し、活性阻害することを示した論文」24件
- Kanemori, Y., Uto, K., Sagata, N. β-TrCP recognizes a previously undescribed nonphosphorylated destruction motif in Cdc25A and Cdc25B phosphatases. Proc. Natl. Acad. Sci. USA, 102, 6279-6284 (2005). 「SCFβ-TrCPユビキチンリガーゼがCdc25A/Bの新規モチーフを認識することを示した論文」20件
- Inoue, D. Sagata, N. The Polo-like kinase Plx1 interacts with and inhibits Myt1 after fertilization of Xenopus eggs. EMBO J., 24, 1057-1067 (2005). 「ツメガエルのPolo様キナーゼが受精時にMyt1をリン酸化・不活性化することを示した論文」9件
- Ohe, M., Inoue, D., Kanemori, Y., Sagata, N. Erp1/Emi2 is essential for the meiosis
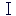 to meiosis
to meiosis  transition in Xenopus oocytes. Dev. Biol., 303, 157-164 (2007). 「APC/C阻害因子のErp1がツメガエル卵の第一/第二減数分裂移行に必須なことを示した論文」5件
transition in Xenopus oocytes. Dev. Biol., 303, 157-164 (2007). 「APC/C阻害因子のErp1がツメガエル卵の第一/第二減数分裂移行に必須なことを示した論文」5件 - Okamoto, K., Sagata, N. Mechanism for inactivation of the mitotic inhibitory kinase Wee1 at M phase. Proc. Natl. Acad. Sci. USA, 104, 3753-3758 (2007). 「M期においてWee1の活性がCdc2によるリン酸化とPin1の結合によって負に制御されることを示した論文」3件
- Inoue, D., Ohe, M., Kanemori, Y., Nobui, T., Sagata, N. A direct link of the Mos- MAPK pathway to Erp1/Emi2 in meiotic arrest of Xenopus eggs. Nature, 446, 1100-1104 (2007). 「ツメガエル未受精卵の分裂停止でMos/MAPK経路の下流キナーゼp90rskがErp1を標的にすることを示した論文」7件
3.その他、効果・効用等の評価に関する情報。
次の(1)、(2)の項目ごとに、該当する内容について具体的かつ明確に記述してください。
(1)研究成果の社会への還元の状況
我々の特別推進研究及びその後の研究は全て基礎的な研究であり、未だ直接的な社会への還元には至っていない。しかし、これらの成果は、以下いくつかの例で示すように社会還元の可能性が充分にあるものであると考えている。
・核内物質の卵減数分裂(卵成熟)への必要性の研究(Iwashita et al., PNAS, 1998)
この研究では、卵母細胞の核内物質が正常な卵成熟(卵が受精可能な状態になる過程)に必須であること、その機能のモデル等を示した。この成果は家畜動物(ブタなど)でも検証されつつあり、畜産、クローン動物の生産などへの基礎情報の一つになっている。
・Chk1,Cdc25A,Wee1の機能ドメインと活性制御に関する研究(Oe et al., Dev. Biol., 2001; Okamoto et al., EMBO J., 2002; Shimuta et al., EMBO J., 2002; Katsuragi and Sagata,Mol. Biol. Cell, 2004; Uto et al., EMBO J., 2004; Kanemori et al., PNAS, 2005; Okamoto and Sagata, PNAS, 2007)
これらの一連の研究では、Chk1,Cdc25A,及びWee1の活性制御部位の同定とその分子機構を明らかにした。Chk1はDNA傷害・複製チェックポイントの主役の1つであり、そのエフェクターとしてのCdc25AやWee1は重要な細胞周期制御因子である。従って、Chk1,Cdc25A,Wee1等の発現や活性の人為的な制御は細胞増殖異常の病気であるがん等の治療に有効と考えられている。Chk1,Cdc25A,Wee1の機能ドメインとその制御機構を明らかにした我々の研究は、それらの分子を標的にした創薬等の基礎情報になり、今後社会への還元につながると考えている。
・未受精卵の分裂停止に関する分子機構の研究(Ohe et al., Dev. Biol., 2007; Inoue et al., Nature 2007)
これらの研究では、ツメガエル未受精卵のMeta-![]() 停止に至る分子経路をMos/MEK/MAPK/p90rsk/Erp1経路として同定した。また最近、他のグループと共同でマウス卵でも同様な経路がMeta-
停止に至る分子経路をMos/MEK/MAPK/p90rsk/Erp1経路として同定した。また最近、他のグループと共同でマウス卵でも同様な経路がMeta-![]() 停止に働くことを明らかにした。マウスではMos/MAPK経路の不全で卵巣奇型腫が生ずることが知られている。従って、脊椎動物未受精卵の分裂停止の分子経路を明らかにした我々の成果は、将来、ヒトの不妊・卵巣奇型腫等の診断や治療などに還元される可能性が充分にあると考えている。
停止に働くことを明らかにした。マウスではMos/MAPK経路の不全で卵巣奇型腫が生ずることが知られている。従って、脊椎動物未受精卵の分裂停止の分子経路を明らかにした我々の成果は、将来、ヒトの不妊・卵巣奇型腫等の診断や治療などに還元される可能性が充分にあると考えている。
(2)研究計画に関与した若手研究者の成長の状況
平成10~14年度の間の特別推進研究に関与した職員、ポスドク、大学院生のうち、その後研究職、教育職に就いた者について、特別推進研究に参加した期間、参加終了時の身分、その後の進路・動向、現在の研究・教育内容を以下に記す。
| 氏名 | 研究参加期間 | 参加終了時の身分 | 進路・現職 | 現在の研究・教育内容 |
|---|---|---|---|---|
| 古野伸明 | 平成12~13年度 | 助手 | 広島大学大学院理学研究科 両生類研究施設・准教授 | 両生類卵形成 |
| 中條信成 | 平成10~14年度 | 助手 | 九州大学大学院理学研究院・助教 | 両生類形態形成 |
| 宇都克裕 | 平成10~14年度 | ポスドク(学振PD) | JST CREST(クレスト)研究員 から 日本ベーリンガーインゲルハイム 川西医薬研究所 研究員 | 神経関係 |
| 志牟田健 | 平成10~14年度 | ポスドク(学術研究員) | 国立感染症研究所細菌第一部 研究員 | 病原菌生化学 |
| 岩下淳 | 平成10~11年度 | ポスドク(学振PD) | 秋田県立大学生物資源科学部 応用生物科学科・助教 | アメーバの分裂 |
| 早野善政 | 平成10~11年度 | 博士課程3年 | 福岡県警・科学捜査研究所・研究員 | 法医学 |
| 吉留賢 | 平成10~12年度 | 博士課程1年 | 鹿児島大学医学部・助手 から 鳥取大学医学部生命科学科・助教 | 両生類卵の分裂 |
| 大江智也 | 平成10~12年度 | 修士課程2年 | アステラス製薬株式会社・筑波研究センター 研究員 | 脳活性物質 |
| 猪原綾 | 平成11~14年度 | 修士課程2年 | バイエル薬品株式会社 研究員 | がん関係 |
| 溝上陽子 | 平成11~14年度 | 修士課程2年 | 佐賀県立 高校 教師(生物) | 生物教育 |
| 上野秀一 | 平成10~14年度 | 博士課程3年(学振DC1) | 山口大学大学院 医学系研究科 応用分子生命科学系・助教 | 両生類卵の分裂 |
| 岡本健吾 | 平成10~14年度 | 博士課程3年(学振DC1) | 学振PD から 九州大学大学院理学研究院生物科学部門・助手 から 高崎健康福祉大学 薬学部 薬学科・助教 | 転写因子制御 |
| 葛城美徳 | 平成11~14年度 | 博士課程1年 | 学術研究員 から JST CREST(クレスト)研究員から新潟大学 教育研究院 医歯学系遺伝子制御講座・助教 | マウス遺伝学 |
| 井上大悟 | 平成12~14年度 | 修士課程2年 | 学振DC1 から JST CREST(クレスト)研究員 から 九州大学大学院理学研究院生物科学部門 学術研究員 | 両生類卵成熟 |
| 佐野亜希子 | 平成12~14年度 | 修士課程2年 | 大鵬薬品工業株式会社・飯能研究センター 研究員 | がん関係 |
| 毛利宜子 | 平成12~14年度 | 修士課程2年 | 三栄原エフエフアイ株式会社・東京支社 研究員 | 香料関係 |
-- 登録:平成21年以前 --