| 1. |
医療分野における規制の整理 |
| |
| ・ |
医療機関では医療機器の調整や画像診断の補助のために校正用線源や吸収補正用線源が用いられています。 |
| ・ |
これらの校正用線源や吸収補正用線源には障害防止法の規制対象のものがあります。また、今後、新たに規制対象となる線源があることが想定されます。 |
| ・ |
これらのうち、吸収補正用線源は医療法の規制対象とすることが措置されており、薬事法に基づいて承認された医療機器の線源について、医療法への一元化がなされれば現場ではより適正に管理することが可能であると考えられます。 |
| ・ |
このため、核医学診療など医療で用いられている線源については、薬事法、医療法による規制と障害防止法の規制の対象外とするのが適切であると思われます。 |
| ・ |
これを実現するには、政令第1条第3号の薬事法第2条第4項に規定する医療機器で文部科学大臣が厚生労働大臣または農林水産大臣と協議して指定するものに装備されているものという規定を利用するのがよいと考えられます。ただし、その前提として、これに対応する薬事法の整備が不可欠であり、調整が必要だと思われます。 |
| ・ |
また、医療機器の校正用線源、吸収補正用線源を設計承認機器とするよう関係業界に働きかけるのも有益である可能性があると考えられます。 |
| ・ |
このような措置が実現すると、厚生労働省における薬事法の改正を待つことなく、来年に迫った政令省令改正への当面の措置として、簡易な届出で設計承認機器が使用できるようになるため、医療現場での無用な混乱を回避できることが期待されます。また、装置に装備された線源に関する保管の要件については、それを徹底する共に(夜間も使用中であるとして、耐火性やセキュリテイ上万全でないままに装置に装備していることを認めているとすると安全確保上問題があるように思われます)、無理矢理に外して別の貯蔵施設で保管する必要がなく実効性のある保管がなされるように装置設計するよう政策誘導するのがよいと思われます。 |
| ・ |
一方、放射線治療で使用される治療用線源やライナックについて、今後とも放射線障害防止法の規制から薬事法や医療法の規制へ一元化することを検討すべきであると思われます。ただし、一元化には薬事法および医療法での規制の整備が必要だと思われます。
|
|
| 2. |
使用の許可と届出の区分の考え方 |
| |
| ・ |
各事業所における非密封線源に関する使用許可がいるか否かの判定において、下限数量の1/100以下の核種については加算の対象にしないことは放射線安全上も妥当であると思われます。 |
| ・ |
一方、密封線源に関して線源を集合した場合の扱いについては、機器装備前と記載されています。しかし、使用後の線源を回収する事業者があり、そのような事業所内で線源が集合することも考えられるとすると、このような想定についても措置しておくのが安全確保には有用ではないかと思われます。
|
|
| 3. |
移動使用の範囲の拡大 |
| |
| ・ |
移動使用の範囲の拡大は、放射線や放射性物質の有効利用に欠かせないものであり改正案に賛成します。 |
| 1) |
対象について |
| ・ |
A型輸送が可能な数量とするとのご説明は理解できるものであり妥当であると思います。ただし、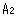 値を上限とするとあるのは、リスクを考えると特別形については 値を上限とするとあるのは、リスクを考えると特別形については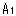 を上限としないことの説明が困難であるように感じました。 を上限としないことの説明が困難であるように感じました。 |
| ・ |
可能であれば、「放射性同位元素の区分に応じ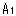 , ,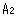 値を上限」とされることを検討されてはいかがでしょうか。 値を上限」とされることを検討されてはいかがでしょうか。 |
| ・ |
ただし、10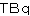 を超える数量についても移動使用を認める場合には施設検査との関係の整理が必要だと思われます。 を超える数量についても移動使用を認める場合には施設検査との関係の整理が必要だと思われます。 |
| ・ |
いずれにしても、改正案に示されたように移動使用に関しある上限を設けることは理解できますが、移動使用と輸送は異なるので法令適用上の混乱を防止するには、説明が必要だと思われます。 |
| 2) |
発生装置等について |
| ・ |
医療法施行規則では、使用場所の制限の例外の規定により、手術室で放射線発生装置を移動使用できるように措置されています。 |
| ・ |
また、放射性医薬品、照射器具等においても、一時的に管理区域を設定し、使用室以外で使用できるように措置されています。 |
| ・ |
このような利用において、障害防止法の手続きに混乱が生じないように法令適用の考え方を整理されることを提案します。
|
|
| 4. |
新しい点検制度 |
| |
| ・ |
密封線源取り扱い事業所では「機器1台で10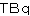 以上の線源」を施設検査の対象とするとあります。 以上の線源」を施設検査の対象とするとあります。 |
| ・ |
一方、これまでの議論では、IAEA TECDOC-1344の放射線源のカテゴリー分けを参考にしてはどうかとされてきました。 |
| ・ |
規制の簡素化という側面では、検討中の案は評価できるのかもしれません。 |
| ・ |
しかし、これまでの議論を踏まえると、核種ごとの特性を考慮してD値を定め、利用されている各機器についてD値の何倍かを調査してカテゴリーを分け検査の対象を決定するようにルール化するのが妥当ではないかと考えられます。
|
|
| 5. |
設計認証の具体的制度 |
| |
| ・ |
「4.認証の基準」の「品質検査の条件」において「製品の線量当量率を測定により確認すること」とあります。 |
| ・ |
しかし、漏洩線量が著しく低く容易に測定できないものもあると考えられます。 |
| ・ |
また、計測機器校正用の線源は、放射能値や放射線放出率で値付けされているものがあり、必ずしも、「線量当量率」の測定が適正な品質検査であるとは限りません。 |
| ・ |
このため、必要に応じて機器からの漏洩線量が設計の範囲であることを確認する測定を行うこととするのはいかがでしょうか。
|
|
| 6. |
下限数量以下の非密封線源の使用 |
| |
| ・ |
規制免除レベルを下回る放射性物質は、規制の枠外であり、その使用後の廃棄については、基本的には、規制対象外とすることで不都合はないと思われます。 |
| ・ |
ただし、規制免除レベルを下回る放射性物質の使用において何らかの理由により廃棄時に廃棄の基準を上回るのであれば、それについても何ら規制の対象にしないというのは安全確保上、もしかしたら、不都合なことがあるのかもしれません。 |
| ・ |
しかし、この判断が、他の放射性廃棄物を有しているかどうかで異なることに合理性があるとは考えがたいと思われます。 |
| ・ |
「問題」であるとすると具体的に問題の所在を明らかにして対処法を考えるのがよいと思います(まずは「汚染された物」の定義を示されるとよいと思います)。 |
| ・ |
また、PET核種の廃棄物対応で、放射性廃棄物としての規制の対象としないとした議論が、クリアランスとは異なるという説明は、理屈の上では成り立つとは思いますが素直ではないので、クリアランスレベル導入後に再整理するのがよいと思います。 |
| ・ |
事業所の概念については整理することが必要であり、座長からも指摘があったように、規制のあり方の観点から必要に応じて現状も調査し、対応策を検討するのがよいと思います。
|
|
| 10. |
その他の規制の合理化等 |
| |
| ・ |
一定期間以上という条件を外すかその短縮を検討されてはいかがでしょうか(1週間というご提案には必ずしも合理性がないと思われるので)。 |
| ・ |
予防規程に定める所内ルールに、一時的な管理区域解除の設定方法を明記するように規定されてはいかがでしょうか。確実に一時的な管理区域解除ができるのであれば、健康診断の義務の免除だけでなく立入の記録の記帳の義務も解除できると思われます。 |
|